名校
解题方法
1 . 回答下列问题:
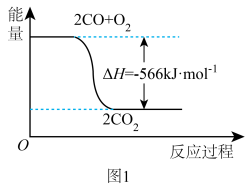
(1)已知常温下CO转化成 的能量关系如图1所示。写出该反应的热化学方程式:
的能量关系如图1所示。写出该反应的热化学方程式:____________ 。
(2) 和
和 混合可作火箭推进剂,已知:0.5 mol
混合可作火箭推进剂,已知:0.5 mol  和足量氧气反应生成
和足量氧气反应生成 和
和 ,放出310.6 kJ的热量;
,放出310.6 kJ的热量;
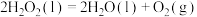
 kJ/mol。
kJ/mol。
① 和
和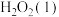 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
②将上述反应设计成原电池如图2所示,KOH溶液作为电解质溶液。
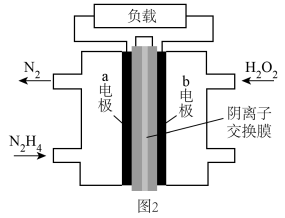
则a极电极反应式__________ 。
(3)实验室用50 mL 0.50 mol⋅L⁻¹盐酸与50 mL某浓度的NaOH溶液在如图3所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。

①该装置缺少一种玻璃仪器,该仪器的名称为______ 。
②实验室提供了0.50 mol⋅L⁻¹和0.55 mol⋅L⁻¹两种浓度的NaOH溶液,应最好选择______ mol⋅L⁻¹的NaOH溶液进行实验。
③在测定中和反应的反应热的实验中,下列叙述正确的是______ 。
a.测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度
B.中和反应的试验中,应快速将NaOH溶液一次倒入盛盐酸的小烧杯中
C.可以用氢氧化钾代替氢氧化钠,浓硫酸代替稀盐酸
D.在测定中和反应的反应热实验中,每完成一次反应热热测定,至少需要读三次温度。
(1)已知常温下CO转化成
 的能量关系如图1所示。写出该反应的热化学方程式:
的能量关系如图1所示。写出该反应的热化学方程式:
(2)
 和
和 混合可作火箭推进剂,已知:0.5 mol
混合可作火箭推进剂,已知:0.5 mol  和足量氧气反应生成
和足量氧气反应生成 和
和 ,放出310.6 kJ的热量;
,放出310.6 kJ的热量;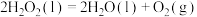
 kJ/mol。
kJ/mol。①
 和
和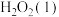 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为②将上述反应设计成原电池如图2所示,KOH溶液作为电解质溶液。

则a极电极反应式
(3)实验室用50 mL 0.50 mol⋅L⁻¹盐酸与50 mL某浓度的NaOH溶液在如图3所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。

①该装置缺少一种玻璃仪器,该仪器的名称为
②实验室提供了0.50 mol⋅L⁻¹和0.55 mol⋅L⁻¹两种浓度的NaOH溶液,应最好选择
③在测定中和反应的反应热的实验中,下列叙述正确的是
a.测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度
B.中和反应的试验中,应快速将NaOH溶液一次倒入盛盐酸的小烧杯中
C.可以用氢氧化钾代替氢氧化钠,浓硫酸代替稀盐酸
D.在测定中和反应的反应热实验中,每完成一次反应热热测定,至少需要读三次温度。
您最近一年使用:0次
名校
解题方法
2 . 资源化利用CO2,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。回答下列问题。
(1)理论研究表明,在101 kPa和298 K下,HCN(g) HNC(g)异构化反应过程的能量变化如图所示:计算可得HCN(g)
HNC(g)异构化反应过程的能量变化如图所示:计算可得HCN(g) HNC(g) ΔH=
HNC(g) ΔH=_______ kJ/mol。HCN与HNC稳定性较强的是_______ 。
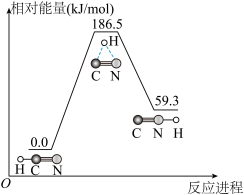
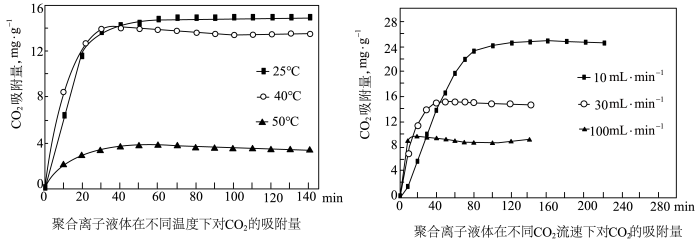
(2)聚合离子液体是目前广泛研究的CO2吸附剂。结合下图 分析聚合离子液体吸附CO2的有利条件是_______ 。
(3)生产尿素:
工业上以CO2、NH3为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步:2NH3(g)+CO2(g)⇌ H2NCOONH4(s) △H = - 159.5 kJ·mol-1
第二步:H2NCOONH4(s)⇌CO(NH2)2(s)+ H2O(g) △H = +116.5 kJ·mol-1
①写出上述合成尿素的热化学方程式_______ 。
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入4mol NH3和1mol CO2,实验测得反应中各组分物质的量随时间的变化如下图所示:
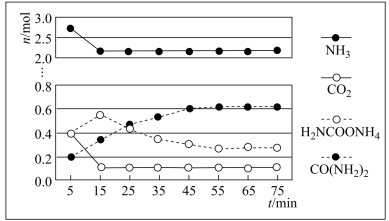
已知总反应的快慢由慢的一步反应决定,则合成尿素总反应的快慢由第_______ 步反应决定,总反应进行到_______ min时到达平衡。
(4)合成乙酸:
中国科学家首次以CH3OH、CO2和H2为原料高效合 成乙酸,其反应路径如下图所示:
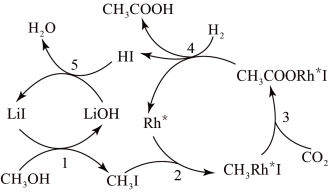
①原料中的CH3OH可通过电解法由CO2制取,用稀硫酸作电解质溶液,写出生成CH3OH的电极反应式_______ 。
②根据图示 ,写出总反应的化学方程式_______ 。
(1)理论研究表明,在101 kPa和298 K下,HCN(g)
 HNC(g)异构化反应过程的能量变化如图所示:计算可得HCN(g)
HNC(g)异构化反应过程的能量变化如图所示:计算可得HCN(g) HNC(g) ΔH=
HNC(g) ΔH=
(2)聚合离子液体是目前广泛研究的CO2吸附剂。

(3)生产尿素:
工业上以CO2、NH3为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步:2NH3(g)+CO2(g)⇌ H2NCOONH4(s) △H = - 159.5 kJ·mol-1
第二步:H2NCOONH4(s)⇌CO(NH2)2(s)+ H2O(g) △H = +116.5 kJ·mol-1
①写出上述合成尿素的热化学方程式
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入4mol NH3和1mol CO2,实验测得反应中各组分物质的量随时间的变化如下图所示:

已知总反应的快慢由慢的一步反应决定,则合成尿素总反应的快慢由第
(4)合成乙酸:
中国科学家首次以CH3OH、CO2和H2为原料高效合 成乙酸,其反应路径如下图所示:

①原料中的CH3OH可通过电解法由CO2制取,用稀硫酸作电解质溶液,写出生成CH3OH的电极反应式
②
您最近一年使用:0次
2023-02-23更新
|
187次组卷
|
2卷引用:福建省福州市八县(市、区)一中2022-2023学年高二上学期期末联考化学试题
解题方法
3 . 氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
(1)已知: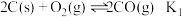

 (其中
(其中 、
、 、
、 为对应化学反应的平衡常数)
为对应化学反应的平衡常数)
①则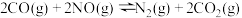 的平衡常数为K,则
的平衡常数为K,则
_______ (用 、
、 、
、 表示)。
表示)。
②在一个恒温恒容的密闭容器中发生反应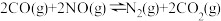 。能表明反应已达到平衡状态的标志有
。能表明反应已达到平衡状态的标志有_______ (填字母)。
A.混合气体的压强保持不变 B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.气体的总质量保持不变
E.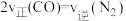 F.
F. 内生成
内生成 同时消耗
同时消耗
(2)向容积为 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应 ,
, 和
和 的物质的量变化如表所示。
的物质的量变化如表所示。
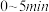 内,以
内,以 表示的平均反应速率
表示的平均反应速率
_______ ,最终达平衡时 的浓度
的浓度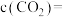
_______ ,平衡时 的转化率
的转化率
_______ ,写出该反应平衡常数的表达式
_______ ,并求该温度 下的平衡常数
下的平衡常数
_______ 。
(1)已知:
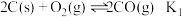

 (其中
(其中 、
、 、
、 为对应化学反应的平衡常数)
为对应化学反应的平衡常数)①则
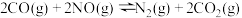 的平衡常数为K,则
的平衡常数为K,则
 、
、 、
、 表示)。
表示)。②在一个恒温恒容的密闭容器中发生反应
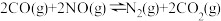 。能表明反应已达到平衡状态的标志有
。能表明反应已达到平衡状态的标志有A.混合气体的压强保持不变 B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.气体的总质量保持不变
E.
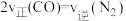 F.
F. 内生成
内生成 同时消耗
同时消耗
(2)向容积为
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应 ,
, 和
和 的物质的量变化如表所示。
的物质的量变化如表所示。| 条件 | 保持温度为 | ||||||
时间/ | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
物质的量/ | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
物质的量/ | 0 | 0.30 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
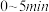 内,以
内,以 表示的平均反应速率
表示的平均反应速率
 的浓度
的浓度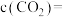
 的转化率
的转化率

 下的平衡常数
下的平衡常数
您最近一年使用:0次
2023-02-18更新
|
135次组卷
|
3卷引用:福建省福州市三校2022-2023学年高二上学期期中联考化学试题
福建省福州市三校2022-2023学年高二上学期期中联考化学试题广西北海市2022-2023学年高二上学期期末考试化学试题(已下线)专题04 可逆反应、化学平衡状态、化学平衡常数【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
4 . 金属钛( )在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
)在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
(1)目前生产钛的方法之一是将金红石( )转化为
)转化为 ,再进一步还原
,再进一步还原 得到钛。
得到钛。 转化为
转化为 有直接氯化法和碳氯化法。在
有直接氯化法和碳氯化法。在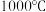 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:
直接氯化: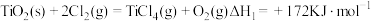 ,
,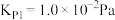
碳氯化: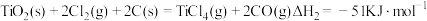 ,
,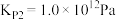
运用以上数据分析,你认为以上两个方法更优越的是__________ ,理由是__________ 。
(2)已知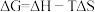 ,
, 和
和 类似,只取决于反应体系的始态和终态。根据如图回答问题。
类似,只取决于反应体系的始态和终态。根据如图回答问题。

①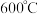 时,反应
时,反应
________ 自发进行(填“能”或“不能”)。
②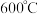 时,
时,
________  。
。
(3)钛酸锂是一种理想的嵌入型电极材料。某新型钛酸锂电池与普通石墨烯锂电池相比,电位比较高,安全性相较好,工作原理如图所示。
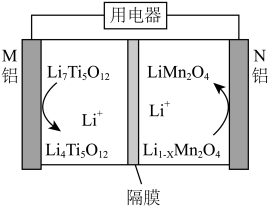
①电池的正极为______ (填“M”或“N”)
②放电时, 通过隔膜向
通过隔膜向______ 极(填“M”或“N”)移动。
③放电时,电极N的电极反应式为______ 。
 )在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
)在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:(1)目前生产钛的方法之一是将金红石(
 )转化为
)转化为 ,再进一步还原
,再进一步还原 得到钛。
得到钛。 转化为
转化为 有直接氯化法和碳氯化法。在
有直接氯化法和碳氯化法。在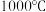 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:直接氯化:
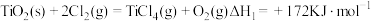 ,
,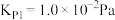
碳氯化:
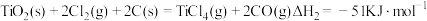 ,
,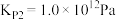
运用以上数据分析,你认为以上两个方法更优越的是
(2)已知
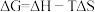 ,
, 和
和 类似,只取决于反应体系的始态和终态。根据如图回答问题。
类似,只取决于反应体系的始态和终态。根据如图回答问题。
①
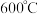 时,反应
时,反应
②
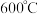 时,
时,
 。
。(3)钛酸锂是一种理想的嵌入型电极材料。某新型钛酸锂电池与普通石墨烯锂电池相比,电位比较高,安全性相较好,工作原理如图所示。

①电池的正极为
②放电时,
 通过隔膜向
通过隔膜向③放电时,电极N的电极反应式为
您最近一年使用:0次
名校
解题方法
5 . 一碳化学技术是指以分子中只含一个碳原子的化合物如一氧化碳、二氧化碳、甲烷、甲醇等为原料,用化工的方法制造产品的化学体系的总称,一碳化学技术的应用对构建生态文明社会具有重要的意义。
(1) 和
和 在催化剂作用下可发生以下两个反应:
在催化剂作用下可发生以下两个反应:
I、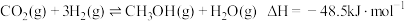
II、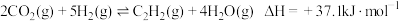
反应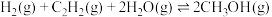 的
的
___________ 。升高温度,反应速率先增大后减小的原因是___________ , 含量
含量___________ (填“增多”或“不变”或“减少”)。
(2)在压强、 、
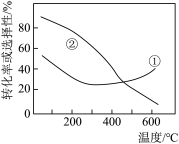
、 的起始投料一定的条件下,发生反应I、II,实验测得
的起始投料一定的条件下,发生反应I、II,实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。
已知:
其中曲线②表示___________ 平衡时的选择性;温度高于 时,曲线①随温度升高而升高的原因是
时,曲线①随温度升高而升高的原因是___________ ;为同时提高 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为___________ (填标号)。
A.低温、低压 B.低温、高压 C.高温、高压 D.高温、低压。
(1)
 和
和 在催化剂作用下可发生以下两个反应:
在催化剂作用下可发生以下两个反应:I、
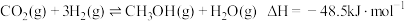
II、
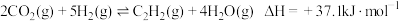
反应
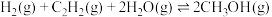 的
的
 含量
含量(2)在压强、
 、
、 的起始投料一定的条件下,发生反应I、II,实验测得
的起始投料一定的条件下,发生反应I、II,实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。
已知:

其中曲线②表示
 时,曲线①随温度升高而升高的原因是
时,曲线①随温度升高而升高的原因是 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为A.低温、低压 B.低温、高压 C.高温、高压 D.高温、低压。
您最近一年使用:0次
解题方法
6 . 工业上利用天然气制备 ,还可得到
,还可得到 、
、 等化工产品。一定条件下,有关反应如下:
等化工产品。一定条件下,有关反应如下:
反应1:
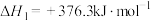
反应2: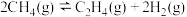
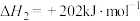
回答下列问题:
(1)相同条件下,反应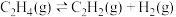
 ,
,
_______  。
。
(2)实验测得反应1的速率方程: ,
,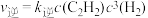 (
( 、
、 分别为正、逆反应速率常数)。
分别为正、逆反应速率常数)。
①结合速率的影响因素,推测速率常数k的影响因素有_______ (填标号)。
A.温度 B.浓度 C.催化剂 D.固体表面性质
②T℃下反应达到平衡时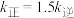 ,该温度下平衡常数
,该温度下平衡常数
_______ 。
(3)向恒温恒容密闭容器中充入适量 ,同时发生上述反应1和反应2,在不同催化剂
,同时发生上述反应1和反应2,在不同催化剂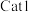 、
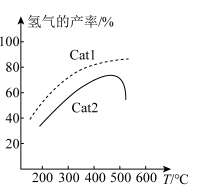
、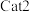 作用下,测得单位时间内
作用下,测得单位时间内 的产率与温度的关系如图所示。在其他条件相同时,催化效率较高的是
的产率与温度的关系如图所示。在其他条件相同时,催化效率较高的是_______ (填“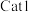 ”或“
”或“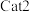 ”)。在
”)。在 作用下,温度高于500℃时,
作用下,温度高于500℃时, 的产率降低的可能原因是
的产率降低的可能原因是_______ 。
(4)一定温度下,总压强恒定为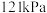 时,向密闭容器中充入
时,向密闭容器中充入 和
和 的混合气体(
的混合气体( 不参与反应),同时发生反应1和反应2,测得
不参与反应),同时发生反应1和反应2,测得 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如下图所示。
的物质的量分数的关系如下图所示。
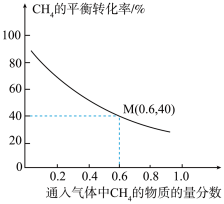
①随着通入气体中 的物质的量分数增大,
的物质的量分数增大, 的平衡转化率降低的主要原因是
的平衡转化率降低的主要原因是_______ 。
②已知M点对应的乙炔的选择性为75%(乙炔的选择性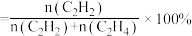 )。该温度下,反应2的平衡常数
)。该温度下,反应2的平衡常数
_______  (结果保留2位有效数字)。(提示:用平衡时气体分压计算的平衡常数为
(结果保留2位有效数字)。(提示:用平衡时气体分压计算的平衡常数为 ,
, 。)
。)
 ,还可得到
,还可得到 、
、 等化工产品。一定条件下,有关反应如下:
等化工产品。一定条件下,有关反应如下:反应1:

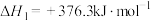
反应2:
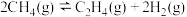
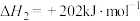
回答下列问题:
(1)相同条件下,反应
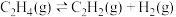
 ,
,
 。
。(2)实验测得反应1的速率方程:
 ,
,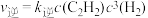 (
( 、
、 分别为正、逆反应速率常数)。
分别为正、逆反应速率常数)。①结合速率的影响因素,推测速率常数k的影响因素有
A.温度 B.浓度 C.催化剂 D.固体表面性质
②T℃下反应达到平衡时
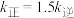 ,该温度下平衡常数
,该温度下平衡常数
(3)向恒温恒容密闭容器中充入适量
 ,同时发生上述反应1和反应2,在不同催化剂
,同时发生上述反应1和反应2,在不同催化剂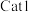 、
、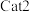 作用下,测得单位时间内
作用下,测得单位时间内 的产率与温度的关系如图所示。在其他条件相同时,催化效率较高的是
的产率与温度的关系如图所示。在其他条件相同时,催化效率较高的是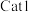 ”或“
”或“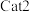 ”)。在
”)。在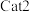 作用下,温度高于500℃时,
作用下,温度高于500℃时, 的产率降低的可能原因是
的产率降低的可能原因是
(4)一定温度下,总压强恒定为
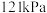 时,向密闭容器中充入
时,向密闭容器中充入 和
和 的混合气体(
的混合气体( 不参与反应),同时发生反应1和反应2,测得
不参与反应),同时发生反应1和反应2,测得 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如下图所示。
的物质的量分数的关系如下图所示。
①随着通入气体中
 的物质的量分数增大,
的物质的量分数增大, 的平衡转化率降低的主要原因是
的平衡转化率降低的主要原因是②已知M点对应的乙炔的选择性为75%(乙炔的选择性
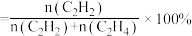 )。该温度下,反应2的平衡常数
)。该温度下,反应2的平衡常数
 (结果保留2位有效数字)。(提示:用平衡时气体分压计算的平衡常数为
(结果保留2位有效数字)。(提示:用平衡时气体分压计算的平衡常数为 ,
, 。)
。)
您最近一年使用:0次
解题方法
7 . Ⅰ、工业上利用 和
和 在催化剂作用下合成甲醇
在催化剂作用下合成甲醇 。
。
已知相关物质的摩尔燃烧焓(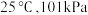 ):数据如下表所示:
):数据如下表所示:
(1)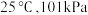 时,由
时,由 和
和 合成
合成 的热化学方程式为
的热化学方程式为___ 。
Ⅱ、某研究小组以甲醇—空气燃料电池为电源,用石墨电极持续电解 溶液,装置如下图所示。
溶液,装置如下图所示。
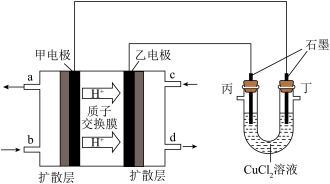
实验现象记录如下:
(2)甲电极的电极反应式为___________ ;当通入 (折算为标准状况下)甲醇蒸汽,测得电路中转移
(折算为标准状况下)甲醇蒸汽,测得电路中转移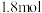 电子,则甲醇的利用率为
电子,则甲醇的利用率为___________ 。
(3)通电前 溶液呈酸性的原因:
溶液呈酸性的原因:___________ (用离子方程式表示)。
(4) 时丁电极的电极反应式为
时丁电极的电极反应式为___________ 。
(5)从丁电极刮取白色固体(含少量红色固体),经检验含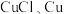 。针对
。针对 固体是如何产生的,某兴趣小组提出两种假设。
固体是如何产生的,某兴趣小组提出两种假设。
假设1:由电极反应产生: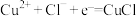
假设2:由反应___________ 产生(用离子方程式表示)。
(6)镀铜工业中,电镀液以 、
、 为主,同时含
为主,同时含 和添加剂。过多的
和添加剂。过多的 会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量
会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量 (微溶)固体能有效解决该问题,反应的离子方程式为
(微溶)固体能有效解决该问题,反应的离子方程式为___________ 。
 和
和 在催化剂作用下合成甲醇
在催化剂作用下合成甲醇 。
。已知相关物质的摩尔燃烧焓(
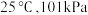 ):数据如下表所示:
):数据如下表所示:| 物质 |  |  | 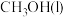 |
摩尔燃烧焓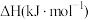 |  |  |  |
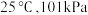 时,由
时,由 和
和 合成
合成 的热化学方程式为
的热化学方程式为Ⅱ、某研究小组以甲醇—空气燃料电池为电源,用石墨电极持续电解
 溶液,装置如下图所示。
溶液,装置如下图所示。
实验现象记录如下:
| 时刻 | 实验现象 | |
| 通电前 |  溶液呈绿色,显酸性 溶液呈绿色,显酸性 | |
 | 丙电极产生气体 | 丁电极底部出现少量红色固体,电极周围溶液变棕黑色 |
 | 丙电极产生气体 | 丁电极产生白色固体 |
| … | …… | |
 | 丙电极产生气体 | 丁电极产生气体 |
 (折算为标准状况下)甲醇蒸汽,测得电路中转移
(折算为标准状况下)甲醇蒸汽,测得电路中转移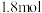 电子,则甲醇的利用率为
电子,则甲醇的利用率为(3)通电前
 溶液呈酸性的原因:
溶液呈酸性的原因:(4)
 时丁电极的电极反应式为
时丁电极的电极反应式为(5)从丁电极刮取白色固体(含少量红色固体),经检验含
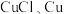 。针对
。针对 固体是如何产生的,某兴趣小组提出两种假设。
固体是如何产生的,某兴趣小组提出两种假设。假设1:由电极反应产生:
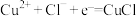
假设2:由反应
(6)镀铜工业中,电镀液以
 、
、 为主,同时含
为主,同时含 和添加剂。过多的
和添加剂。过多的 会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量
会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量 (微溶)固体能有效解决该问题,反应的离子方程式为
(微溶)固体能有效解决该问题,反应的离子方程式为
您最近一年使用:0次
8 . 煤燃烧后的主要产物是CO、CO2.回答下列问题:
(1)已知:①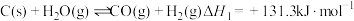 ;
;
②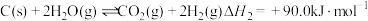 ;
;
③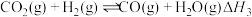 。
。

_______  ,在反应①的体系中加入催化剂,
,在反应①的体系中加入催化剂,
_______ (填“增大”“减小”或“不变”)。
(2)以CO2为原料可制备甲醇: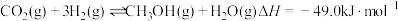 ,向1L的恒容密闭容器中充入1molCO2(g)和3molH2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图1所示。
,向1L的恒容密闭容器中充入1molCO2(g)和3molH2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图1所示。
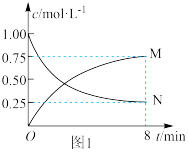
①图1中N表示的是_______ (填化学式);0~8min内,以氢气表示的平均反应速率v(H2)=_______  (结果保留两位有效数字)。
(结果保留两位有效数字)。
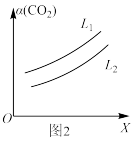
②在一定条件下,体系中CO2的平衡转化率( )与L和X的关系如图2所示,L和X分别表示温度或压强。X表示的物理量是
)与L和X的关系如图2所示,L和X分别表示温度或压强。X表示的物理量是_______ (填“温度”或“压强”),L1_______ (填“>”或“<”)L2。
(3)向一体积为20L的恒容密闭容器中通入1molCO2发生反应: ,在不同温度下各物质的体积分数变化如图3所示。
,在不同温度下各物质的体积分数变化如图3所示。
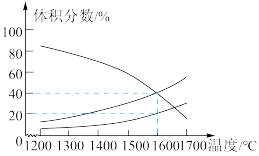
1600℃时反应达到平衡,则此时反应的平衡常数K=_______ 。
(1)已知:①
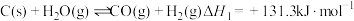 ;
;②
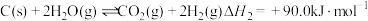 ;
;③
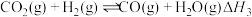 。
。
 ,在反应①的体系中加入催化剂,
,在反应①的体系中加入催化剂,
(2)以CO2为原料可制备甲醇:
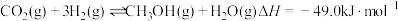 ,向1L的恒容密闭容器中充入1molCO2(g)和3molH2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图1所示。
,向1L的恒容密闭容器中充入1molCO2(g)和3molH2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图1所示。
①图1中N表示的是
 (结果保留两位有效数字)。
(结果保留两位有效数字)。②在一定条件下,体系中CO2的平衡转化率(
 )与L和X的关系如图2所示,L和X分别表示温度或压强。X表示的物理量是
)与L和X的关系如图2所示,L和X分别表示温度或压强。X表示的物理量是
(3)向一体积为20L的恒容密闭容器中通入1molCO2发生反应:
 ,在不同温度下各物质的体积分数变化如图3所示。
,在不同温度下各物质的体积分数变化如图3所示。
1600℃时反应达到平衡,则此时反应的平衡常数K=
您最近一年使用:0次
2023-01-08更新
|
131次组卷
|
2卷引用:福建省宁德市2022-2023学年高二上学期期末居家检测化学试题
名校
9 . 合成氨是人类科学技术上的一项重大突破,氨有广泛的应用。
已知:N2(g)+3H2(g) 2NH3(g) ∆H1=-a kJ∙mol-1;
2NH3(g) ∆H1=-a kJ∙mol-1;
2H2(g)+O2(g) 2H2O(l) ∆H2=-b kJ∙mol-1
2H2O(l) ∆H2=-b kJ∙mol-1
(1)有研究报道,在常温、常压、光照条件下,N2在特殊催化剂表面与H2O反应可生成NH3。则由N2与H2O反应生成NH3的热化学方程式是___________ 。
(2)工业上主要以N2(g)、H2(g)为原料气合成NH3。
①将物质的量之比为1:3的N2和H2充入2L的密闭容器中,在一定条件下达到平衡,测得平衡时数据如下:
该条件下H2的转化率为___________ (可用分数表示),平衡常数K=___________ (可用分数表示)。
②若按以下浓度投料,其它反应条件与①相同,起始时反应进行的方向为___________ (填“正向”、“逆向”或“无法判断”)。
③L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。
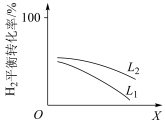
i.X代表的物理量是___________ 。
ii.判断L1、L2的大小关系,并简述理由___________ 。
已知:N2(g)+3H2(g)
 2NH3(g) ∆H1=-a kJ∙mol-1;
2NH3(g) ∆H1=-a kJ∙mol-1;2H2(g)+O2(g)
 2H2O(l) ∆H2=-b kJ∙mol-1
2H2O(l) ∆H2=-b kJ∙mol-1(1)有研究报道,在常温、常压、光照条件下,N2在特殊催化剂表面与H2O反应可生成NH3。则由N2与H2O反应生成NH3的热化学方程式是
(2)工业上主要以N2(g)、H2(g)为原料气合成NH3。
①将物质的量之比为1:3的N2和H2充入2L的密闭容器中,在一定条件下达到平衡,测得平衡时数据如下:
物质 | N2 | H2 | NH3 |
平衡时物质的量/mol | 0.2 | 0.6 | 0.2 |
②若按以下浓度投料,其它反应条件与①相同,起始时反应进行的方向为
物质 | N2 | H2 | NH3 |
起始浓度(mol/L) | 0.5 | 1.5 | 0.5 |

i.X代表的物理量是
ii.判断L1、L2的大小关系,并简述理由
您最近一年使用:0次
名校
解题方法
10 . 某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
请回答下列问题:
(1)为减少SO2的排放,常采取的措施如下:将煤转化为清洁气体燃料。
已知:H2(g)+ O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1;
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1;
C(s)+ O2(g)=CO(g) ΔH=-110.5 kJ·mol-1。
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1。
写出焦炭与水蒸气反应的热化学方程式:_______ 。
(2)汽车尾气的转化:
①NO在催化条件下分解,反应在恒温密闭容器中下进行:2NO(g) N2(g)+O2(g) ΔH=-180.8 kJ·mol-1;某温度下,NO平衡转化率为10.0%,该温度下的平衡常数为
N2(g)+O2(g) ΔH=-180.8 kJ·mol-1;某温度下,NO平衡转化率为10.0%,该温度下的平衡常数为_______ ,若某时刻n(NO)、n(N2)、n(O2)分别为2.0mol、1.0mol、0.50mol,此时反应_______ (填序号)。
a.向逆反应方向进行 b.向正反应方向进行 c.达到平衡状态
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:_______ 。
(3)清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池,一定条件下用CO和H2合成CH3OH:CO(g) +2H2(g) CH3OH(g) ΔH=-99kJ·mol-1。向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同条件下容器内的压强(P:kPa)随时间(min)的变化关系如图中I、Ⅱ、Ⅲ曲线所示:
CH3OH(g) ΔH=-99kJ·mol-1。向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同条件下容器内的压强(P:kPa)随时间(min)的变化关系如图中I、Ⅱ、Ⅲ曲线所示:

①Ⅱ和I相比,改变的反应条件是_______ ;
②若反应I的温度(T1),反应Ⅲ的温度(T3),则T1_______ T3(填“小于”、“大于”或“等于”),简要说明判断依据:_______ 。
请回答下列问题:
(1)为减少SO2的排放,常采取的措施如下:将煤转化为清洁气体燃料。
已知:H2(g)+
 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1;
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1;C(s)+
 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1。
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1。写出焦炭与水蒸气反应的热化学方程式:
(2)汽车尾气的转化:
①NO在催化条件下分解,反应在恒温密闭容器中下进行:2NO(g)
 N2(g)+O2(g) ΔH=-180.8 kJ·mol-1;某温度下,NO平衡转化率为10.0%,该温度下的平衡常数为
N2(g)+O2(g) ΔH=-180.8 kJ·mol-1;某温度下,NO平衡转化率为10.0%,该温度下的平衡常数为a.向逆反应方向进行 b.向正反应方向进行 c.达到平衡状态
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
(3)清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池,一定条件下用CO和H2合成CH3OH:CO(g) +2H2(g)
 CH3OH(g) ΔH=-99kJ·mol-1。向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同条件下容器内的压强(P:kPa)随时间(min)的变化关系如图中I、Ⅱ、Ⅲ曲线所示:
CH3OH(g) ΔH=-99kJ·mol-1。向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同条件下容器内的压强(P:kPa)随时间(min)的变化关系如图中I、Ⅱ、Ⅲ曲线所示:
①Ⅱ和I相比,改变的反应条件是
②若反应I的温度(T1),反应Ⅲ的温度(T3),则T1
您最近一年使用:0次
2022-12-21更新
|
75次组卷
|
2卷引用:福建省莆田哲理中学2022-2023学年高二上学期期中考试化学试题



