1 . 在298K、101kPa下,将4.4gCO2通入150mL1mol·L-1KOH溶液中充分反应(不考虑气体逸出),测得反应放出akJ的热量,已知该条件下,0.5molCO2通入1L1mol·L-1KOH溶液中充分反应放出bkJ的热量。则下列表示CO2与KOH溶液反应生成KHCO3溶液的热化学方程式书写正确的是
| A.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-2(5b-a)kJ·mol-1 |
| B.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-2(5a-4b)kJ·mol-1 |
| C.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-(20b-a)kJ·mol-1 |
| D.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-2(10a-b)kJ·mol-1 |
您最近一年使用:0次
2023-01-30更新
|
205次组卷
|
9卷引用:河南省创新发展联盟2021-2022学年高二上学期9月联考化学试题
河南省创新发展联盟2021-2022学年高二上学期9月联考化学试题贵州省遵义市2021 2022学年高二上学期第一次月考化学试题河南省温县第一高级中学2021-2022学年高二上学期10月月考化学试题安徽省六安市第一中学2022届高三上学期第三次月考化学试题(已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)(已下线)期末综合测试卷01-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179
11-12高二下·北京·期中
名校
解题方法
2 . 已知反应:①
 ,
,
②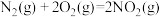
 ,
,
③
 ,
,
则反应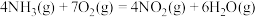 的
的 为
为

 ,
,②
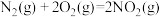
 ,
,③

 ,
,则反应
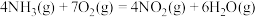 的
的 为
为A.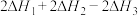 | B. |
C.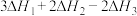 | D.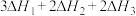 |
您最近一年使用:0次
2023-01-20更新
|
604次组卷
|
54卷引用:吉林省延边朝鲜族自治州汪清县汪清第四中学2021-2022学年高二上学期第二次阶段考试化学试题
吉林省延边朝鲜族自治州汪清县汪清第四中学2021-2022学年高二上学期第二次阶段考试化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期第二次月考化学试题2015-2016学年山东省济宁任城区高二上学期统考化学试卷2017届河北省武邑中学高三上学期第一次调研化学试卷【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期10月月考化学试题吉林省长春市田家炳实验中学2018-2019学年高二上学期第一学程检测化学试题【全国百强校】山西省太原市第五中学2018-2019学年高二(理)上学期10月月考化学试题【全国百强校】江西省金溪县第一中学2018-2019学年高二上学期12月月考化学试题吉林省乾安县第七中学2018-2019学年高一下学期第二次质量检测化学试题宁夏长庆高级中学2019-2020学年高二上学期第一次月考化学试题安徽省砀山县第二中学2020届高三上学期第四次月考化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期12月月考化学试题河南省鹤壁市高中2019-2020学年高一下学期第一次段考化学试题安徽省合肥市第九中学2020-2021学年高二上学期第一次月考化学试题(已下线)【浙江新东方】48安徽省六安市舒城育才学校2020-2021学年高二12月月考化学试题黑龙江省大庆中学2021-2022学年高二上学期开学考试化学试题天津市南开中学2021-2022学年高二上学期期中检测化学试题江西省吉安市永新中学2021-2022学年高二上学期期中考试化学(理科)试题湖南省涟源市第二中学2021-2022学年高二上学期期中考试化学试题黑龙江省牡丹江市海林市朝鲜族中学2022-2023学年高二上学期第一次月考化学试题黑龙江省哈尔滨市第七十三中学校2022-2023学年高二上学期第一次月考化学试题陕西省宝鸡市千阳县中学2022-2023学年高二上学期第一次月考(理)化学试题广东省深圳实验学校高中部2022-2023学年高二上学期第一阶段考试化学试题吉林省洮南市第一中学2022-2023学年高二上学期第一次(10月)月考化学试题甘肃省靖远县第二中学2021-2022学年高二上学期期中考试化学(理)试题吉林省长春市九台区营城第一高级中学2022-2023学年高二上学期第一次月考化学试题辽宁省沈阳市郊校2022-2023学年高一下学期4月联考化学试题河北省邢台市2022-2023学年高一下学期6月月考化学试题(已下线)2011-2012学年北京市101中学高二下学期期中考试化学试卷(已下线)2014届黑龙江省哈六中高三上学期期中考试化学试卷辽宁省庄河市高级中学2016-2017学年高一下学期期中考试化学试题【全国校级联考】安徽省淮北十二中、濉溪二中2017-2018学年高一下学期期中联考化学试题吉林省长春汽车经济开发区第六中学2017-2018学年高一下学期期末考试化学试题黑龙江省双鸭山市第一中学2019-2020学年高二上学期期中考试化学试题福建省永泰县第一中学2019-2020学年高二上学期期中考试化学试题云南省迪庆州香格里拉中学2019-2020学年高二上学期期末考试化学试题【懂做原理题】2020届高三化学选修4二轮专题练——盖斯定律的应用【选择提升24题】2020届高三化学知识点强化训练—盖斯定律(已下线)1.1.3 反应焓变的计算 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1(已下线)【南昌新东方】9.湾里一中 梁莎鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第1节 化学反应的热效应 课时4 反应焓变的计算人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 第二节 反应热的计算 课时1 盖斯定律云南省楚雄师范学院附属中学2020-2021学年高二上学期期中考试化学试题(已下线)1.2.2 化学反应焓变的计算-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)辽宁省辽河油田第二高级中学2022-2023学年高二上学期开学考试化学试题海南省琼海市嘉积第二中学2021-2022学年高二下学期教学质量监测(期末考)化学试题安徽省怀宁县第二中学2021-2022学年高三上学期期末考试化学试题湖北省2022-2023学年高三上学期期末考试化学试题(已下线)专题02 盖斯定律、反应热的计算【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)江西省抚州市2023-2024学年高二上学期学生学业质量监测化学试题青海省西宁北外附属新华联外国语高级中学2023-2024学年高二上学期期中考试化学试题江西省南昌十九中2022-2023学年高二上学期期末考试化学试卷 湖南省长沙市德成学校2023-2024学年高二上学期1月期末化学试题
3 . 合成气是一种以H2和CO为主的化工原料气,其用途广泛、廉价、清洁,可以合成许多化工产品。
(1)由CH4、CO2制合成气的主要反应有:
I.CH4(g)+2O2(g) CO2(g)+2H2O(g) △H1=-820.6kJ•mol-1
CO2(g)+2H2O(g) △H1=-820.6kJ•mol-1
II.CH4(g)+CO2(g) 2CO(g)+2H2(g) △H2=+247.3kJ•mol-1
2CO(g)+2H2(g) △H2=+247.3kJ•mol-1
III.CH4(g)+H2O(g) CO(g)+3H2(g) △H3=+206.1kJ•mol-1
CO(g)+3H2(g) △H3=+206.1kJ•mol-1
IV.CO2(g)+H2(g) CO(g)+H2O(g) △H4
CO(g)+H2O(g) △H4
①△H4=______ kJ•mol-1。
②用Ni基双金属催化反应III,反应的活化能降低,△H3______ (填“变大”、“变小”或“不变”)。
(2)一定条件下,向1L密闭容器中充入等物质的量的CO2和CH4,在催化剂作用下只发生反应II,反应控制其它条件不变,改变温度(T)对合成气中甲烷质量分数的影响如图:

若充入amolCH4,经过2小时后达到A点,2小时内用CH4表示的平均反应速率v(CH4)=______ mol•L-1•h-1(用含a的式子表示)。假设A为平衡态,此时压强为1MPa,则该反应的平衡常数Kp=______ (MPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)不同温度下,向体积为VL的含少量O2的密闭容器中按照n(CO2):n(CH4)=1投料,实验测得平衡时 随温度(T)的变化关系如图1所示:
随温度(T)的变化关系如图1所示:

①压强p1、p2、p3由大到小的顺序为_____ 。
②压强为p2时,随着温度升高, 先增大后减小。解释温度Tm前后,随着温度升高
先增大后减小。解释温度Tm前后,随着温度升高 变化的原因分别是
变化的原因分别是______ 。
③根据图1、图2分析,为提高CO的选择性(即CO在合成气中的体积分数)可采取的措施是______ (填字母)。
A.提高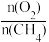 比例 B.降低
比例 B.降低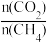 比例 C.高温、高压 D.低温、低压
比例 C.高温、高压 D.低温、低压
(1)由CH4、CO2制合成气的主要反应有:
I.CH4(g)+2O2(g)
 CO2(g)+2H2O(g) △H1=-820.6kJ•mol-1
CO2(g)+2H2O(g) △H1=-820.6kJ•mol-1II.CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H2=+247.3kJ•mol-1
2CO(g)+2H2(g) △H2=+247.3kJ•mol-1III.CH4(g)+H2O(g)
 CO(g)+3H2(g) △H3=+206.1kJ•mol-1
CO(g)+3H2(g) △H3=+206.1kJ•mol-1IV.CO2(g)+H2(g)
 CO(g)+H2O(g) △H4
CO(g)+H2O(g) △H4①△H4=
②用Ni基双金属催化反应III,反应的活化能降低,△H3
(2)一定条件下,向1L密闭容器中充入等物质的量的CO2和CH4,在催化剂作用下只发生反应II,反应控制其它条件不变,改变温度(T)对合成气中甲烷质量分数的影响如图:

若充入amolCH4,经过2小时后达到A点,2小时内用CH4表示的平均反应速率v(CH4)=
(3)不同温度下,向体积为VL的含少量O2的密闭容器中按照n(CO2):n(CH4)=1投料,实验测得平衡时
 随温度(T)的变化关系如图1所示:
随温度(T)的变化关系如图1所示:
①压强p1、p2、p3由大到小的顺序为
②压强为p2时,随着温度升高,
 先增大后减小。解释温度Tm前后,随着温度升高
先增大后减小。解释温度Tm前后,随着温度升高 变化的原因分别是
变化的原因分别是③根据图1、图2分析,为提高CO的选择性(即CO在合成气中的体积分数)可采取的措施是
A.提高
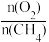 比例 B.降低
比例 B.降低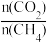 比例 C.高温、高压 D.低温、低压
比例 C.高温、高压 D.低温、低压
您最近一年使用:0次
解题方法
4 . 砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式_______ 。该反应需要在加压下进行,原因是_______ 。
(2)已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_______ 。
(3)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应: (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
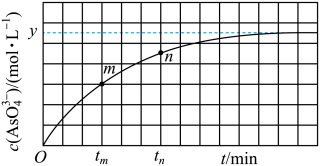
①下列可判断反应达到平衡的是_______ (填标号)。
a.溶液的pH不再变化 b.v(I−)=2v( )
)
c. c( )/c(
)/c( )不再变化 d. c(I−)=y mol·L−1
)不再变化 d. c(I−)=y mol·L−1
②tm时v逆_______ tn时v逆(填“大于”“小于”或“等于”),理由是_______ 。
③tm若平衡时溶液的pH=14,则该反应的平衡常数K为_______ 。
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
(2)已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+
 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH22As(s)+
 O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =
(3)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应:
 (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化 b.v(I−)=2v(
 )
)c. c(
 )/c(
)/c( )不再变化 d. c(I−)=y mol·L−1
)不再变化 d. c(I−)=y mol·L−1②tm时v逆
③tm若平衡时溶液的pH=14,则该反应的平衡常数K为
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题
(1)在25℃,101kpa下,1g甲醇( )燃烧生成
)燃烧生成 和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________ 。
(2)已知几种化学键的键能数据如表所示:
请写出氨气与溴蒸气反应的热化学方程式:___________ 。
(3)已知:
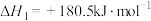

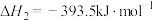
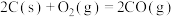
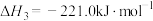
若某反应的平衡常数表达式为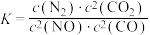 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式___________ 。
(4)根据图示信息写出热化学方程式:___________ 。
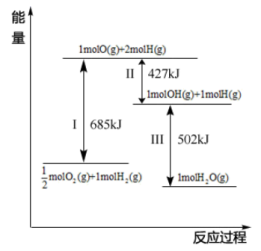
(5)已知:C(s)、CO(g)和 完全燃烧的热化学方程式分别为
完全燃烧的热化学方程式分别为




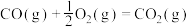
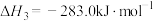
请你根据以上数据,写出C(s)与水蒸气反应生成CO和 的热化学方程式:
的热化学方程式:___________ 。
(1)在25℃,101kpa下,1g甲醇(
 )燃烧生成
)燃烧生成 和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为(2)已知几种化学键的键能数据如表所示:
| 化学键 | N—H |  | Br—Br | H—Br |
键能/ | 391 | 946 | 194 | 366 |
(3)已知:

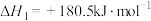

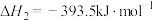
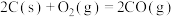
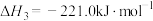
若某反应的平衡常数表达式为
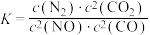 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(4)根据图示信息写出热化学方程式:

(5)已知:C(s)、CO(g)和
 完全燃烧的热化学方程式分别为
完全燃烧的热化学方程式分别为



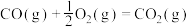
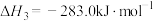
请你根据以上数据,写出C(s)与水蒸气反应生成CO和
 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 完成下列问题
(1)断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B键的键能。下表列出了一些化学键的键能E:
请回答下列问题:
①下图表示某反应的能量变化关系,则此反应为_______ (填“吸热”或“放热”)反应,其中ΔH=_______ (用含有a、b的关系式表示)。
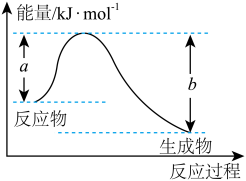
②若上图示中表示反应H2(g)+ O2(g)=H2O(g) ΔH=-242 kJ·mol-1,则b=
O2(g)=H2O(g) ΔH=-242 kJ·mol-1,则b=_______ kJ·mol-1,x=_______ kJ·mol-1。
(2)已知下列反应:
2CO(g)+O2(g)=2CO2(g ) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1
试回答:
①CO的燃烧热ΔH=_______ 。
②在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为_______ 。
(1)断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B键的键能。下表列出了一些化学键的键能E:
| 化学键 | H-H | O=O | O-H |
| E/kJ·mol-1 | 436 | x | 463 |
①下图表示某反应的能量变化关系,则此反应为

②若上图示中表示反应H2(g)+
 O2(g)=H2O(g) ΔH=-242 kJ·mol-1,则b=
O2(g)=H2O(g) ΔH=-242 kJ·mol-1,则b=(2)已知下列反应:
2CO(g)+O2(g)=2CO2(g ) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1试回答:
①CO的燃烧热ΔH=
②在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为
您最近一年使用:0次
7 . 二氧化碳加氢合成二甲醚(CH3OCH3)具有重要的现实意义和广阔的应用前景。该方法主要涉及下列反应:
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
反应Ⅲ:2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5kJ·mol-1
下列说法不正确的是
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
反应Ⅲ:2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5kJ·mol-1
下列说法不正确的是
| A.CO2大量排放可导致温室效应 |
| B.干冰升华吸热是因为CO2分子中共价键发生断裂 |
C.反应I的平衡常数可表示为K = |
| D.反应2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)的ΔH= -122.5kJ·mol-1 |
您最近一年使用:0次
2023-01-03更新
|
160次组卷
|
2卷引用:广东省深圳市龙华中学2022届高三上学期10月月考试化学试题
8 . 为了解决能源的可再生及将 变废为宝等问题科学家借鉴自然界的光合作用原理通过“人工”光合作用合成了甲醇等液态燃料,因此甲醇又被称为液态太阳燃料。液态太阳燃料的合成及应用如图甲所示。请回答:
变废为宝等问题科学家借鉴自然界的光合作用原理通过“人工”光合作用合成了甲醇等液态燃料,因此甲醇又被称为液态太阳燃料。液态太阳燃料的合成及应用如图甲所示。请回答:
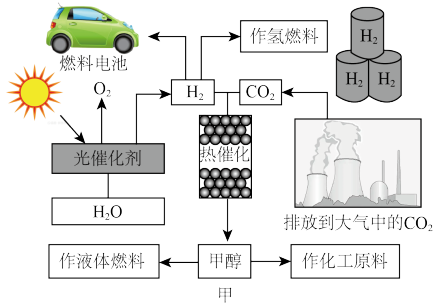
(1)联系自然界的光合作用原理,并结合图甲,写出“人工”光合作用的化学方程式:___________ ;在图示转化过程中,太阳能除了储存在甲醇中,还储存在___________ (填化学式)中。
(2)图中热催化过程的反应原理为 。已知:2H2 +O2 (g)= 2H2O(g) △H1= -483.6kJ/mol ;2CH3OH(g) + 3O2 (g)
。已知:2H2 +O2 (g)= 2H2O(g) △H1= -483.6kJ/mol ;2CH3OH(g) + 3O2 (g)  2CO2(g) + 4H2O(g) △H2= -1352.86kJ/mol,则可求得
2CO2(g) + 4H2O(g) △H2= -1352.86kJ/mol,则可求得
___________ 。
(3)已知H﹣H键能为436KJ/mol,H﹣N键能为391KJ/mol,根据化学方程式:N2(g)+3H2(g)=2NH3(g)△H=﹣92KJ/mol,则N≡N键的键能是___________ 。
(4)已知反应:HCl(g)= H2(g)+
H2(g)+  Cl2(g)△H=+92.3kJ•mol﹣1, 则反应H2(g)+Cl2(g)=2HCl(g)的△H为
Cl2(g)△H=+92.3kJ•mol﹣1, 则反应H2(g)+Cl2(g)=2HCl(g)的△H为___________ 。
 变废为宝等问题科学家借鉴自然界的光合作用原理通过“人工”光合作用合成了甲醇等液态燃料,因此甲醇又被称为液态太阳燃料。液态太阳燃料的合成及应用如图甲所示。请回答:
变废为宝等问题科学家借鉴自然界的光合作用原理通过“人工”光合作用合成了甲醇等液态燃料,因此甲醇又被称为液态太阳燃料。液态太阳燃料的合成及应用如图甲所示。请回答:
(1)联系自然界的光合作用原理,并结合图甲,写出“人工”光合作用的化学方程式:
(2)图中热催化过程的反应原理为
 。已知:2H2 +O2 (g)= 2H2O(g) △H1= -483.6kJ/mol ;2CH3OH(g) + 3O2 (g)
。已知:2H2 +O2 (g)= 2H2O(g) △H1= -483.6kJ/mol ;2CH3OH(g) + 3O2 (g)  2CO2(g) + 4H2O(g) △H2= -1352.86kJ/mol,则可求得
2CO2(g) + 4H2O(g) △H2= -1352.86kJ/mol,则可求得
(3)已知H﹣H键能为436KJ/mol,H﹣N键能为391KJ/mol,根据化学方程式:N2(g)+3H2(g)=2NH3(g)△H=﹣92KJ/mol,则N≡N键的键能是
(4)已知反应:HCl(g)=
 H2(g)+
H2(g)+  Cl2(g)△H=+92.3kJ•mol﹣1, 则反应H2(g)+Cl2(g)=2HCl(g)的△H为
Cl2(g)△H=+92.3kJ•mol﹣1, 则反应H2(g)+Cl2(g)=2HCl(g)的△H为
您最近一年使用:0次
9 . I、
(1)已知:
C(石墨,s)+O2(g)=CO2(g) ΔH1=-akJ∙mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-bkJ∙mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-ckJ∙mol-1
根据盖斯定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变ΔH=___________ (用含有a,b,c的式子表示)
II、一定温度下,向容积为2L的恒容密闭容器中加入等物质的量的H2和I2,发生反应H2(g)+I2(g)⇌2HI(g)ΔH<0.测得不同反应时间容器内H2的物质的量如表;
回答下列问题:
(2)0~20min内HI的平均反应速率为___________ 。
(3)反应达到化学平衡状态时,I2的转化率为___________ ,容器内HI的体积分数为___________ 。
(4)该条件下,能说明上述反应达到化学平衡状态的是___________。(填标号)
(5)该反应在三种不同情况下的化学反应速率分别为:①v(H2)=0.02mol·L-1·s-1,②v(I2)=0.32mol·L-1·min-1,③v(HI)=0.84mol·L-1·min-1.则反应进行的速率由快到慢的顺序为___________ 。
(1)已知:
C(石墨,s)+O2(g)=CO2(g) ΔH1=-akJ∙mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-bkJ∙mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-ckJ∙mol-1
根据盖斯定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变ΔH=
II、一定温度下,向容积为2L的恒容密闭容器中加入等物质的量的H2和I2,发生反应H2(g)+I2(g)⇌2HI(g)ΔH<0.测得不同反应时间容器内H2的物质的量如表;
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(H2)/mol | 1 | 0.75 | 0.65 | 0.6 | 0.6 |
(2)0~20min内HI的平均反应速率为
(3)反应达到化学平衡状态时,I2的转化率为
(4)该条件下,能说明上述反应达到化学平衡状态的是___________。(填标号)
| A.混合气体颜色不再改变 |
| B.容器内压强不再改变 |
| C.H2、I2、HI三种气体体积分数不再改变 |
| D.混合气体密度不再改变 |
您最近一年使用:0次
解题方法
10 . 填空。
(1)①一定温度下,在密闭容器中充入1molN2和3molH2发生反应:N2(g)+3H2(g)⇌2NH3(g) ΔH<0。若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的 ,则N2的转化率a1=
,则N2的转化率a1=_____ ;
②若向该容器中再加入3molH2,达到平衡状态时,N2的转化率为a2,则a2___ a1(填“>”、“<”或“=”)。
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0。在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:
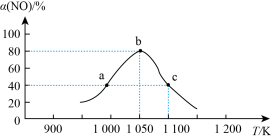
图中a、b、c三点中,达到平衡的点是____ ;温度为1100K时,N2的平衡体积分数为_____ 。
(3)已知同温同压下,下列反应的焓变和平衡常数分别表示为
①2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197kJ·mol-1 K1=a
②2NO(g)+O2(g)⇌2NO2(g) ΔH2=-144kJ·mol-1 K2=b
③NO2(g)+SO2(g)⇌SO3(g)+NO(g) ΔH3=mkJ·mol-1 K3=c
则m的数值为_______ ,c与a、b之间的关系为_______ 。
(4)对于反应2NO(g)+O2(g)⇌2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。

①比较P1、P2的大小关系:P1_______ P2(填“>”、“<”或“=”);ΔH_______ 0
②该反应的平衡常数K的表达式为_______ ,随温度升高,该反应平衡常数变化的趋势是_______ 。(填“增大”、“减小”或“不变”)。
③下列措施中能够同时满足增大反应速率和提高NO转化率的是_______ 。(填写相应字母)
A.使用高效催化剂
B.保持容器体积不变加入惰性气体
C.保持容器体积不变加入O2
D.降低温度
E.压缩容器体积
(1)①一定温度下,在密闭容器中充入1molN2和3molH2发生反应:N2(g)+3H2(g)⇌2NH3(g) ΔH<0。若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的
 ,则N2的转化率a1=
,则N2的转化率a1=②若向该容器中再加入3molH2,达到平衡状态时,N2的转化率为a2,则a2
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0。在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:

图中a、b、c三点中,达到平衡的点是
(3)已知同温同压下,下列反应的焓变和平衡常数分别表示为
①2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197kJ·mol-1 K1=a
②2NO(g)+O2(g)⇌2NO2(g) ΔH2=-144kJ·mol-1 K2=b
③NO2(g)+SO2(g)⇌SO3(g)+NO(g) ΔH3=mkJ·mol-1 K3=c
则m的数值为
(4)对于反应2NO(g)+O2(g)⇌2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。

①比较P1、P2的大小关系:P1
②该反应的平衡常数K的表达式为
③下列措施中能够同时满足增大反应速率和提高NO转化率的是
A.使用高效催化剂
B.保持容器体积不变加入惰性气体
C.保持容器体积不变加入O2
D.降低温度
E.压缩容器体积
您最近一年使用:0次



