1 . 将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。下列说法正确的是
| A.该反应中,热能转化为生成物的内部能量 |
| B.反应物的总能量高于生成物的总能量 |
C.由实验现象可知反应: 一定为吸热反应 一定为吸热反应 |
| D.该反应可以设计成原电池装置 |
您最近一年使用:0次
解题方法
2 . Ⅰ.(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,下图能正确表示该反应中能量变化的是___________ 。
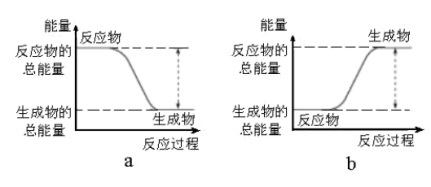
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量___________ kJ。
(2)下列反应中,既属于氧化还原反应,又属于放热反应的是___________
a.盐酸与烧碱溶液反应 b.柠檬酸和碳酸氢钠反应
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.浓硫酸溶于水
Ⅱ.A、B、C、D 四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向___________ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为___________ 。
③装置丙中溶液的pH___________ (填“变大”“变小”或“不变”)。
④四种金属活动性由强到弱的顺序是___________ 。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H-H | O=O | H-O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出热量
(2)下列反应中,既属于氧化还原反应,又属于放热反应的是
a.盐酸与烧碱溶液反应 b.柠檬酸和碳酸氢钠反应
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.浓硫酸溶于水
Ⅱ.A、B、C、D 四种金属按下表中装置进行实验。
| 装置 | 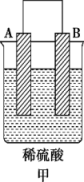 | 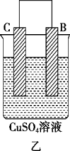 | 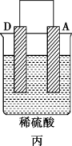 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属活动性由强到弱的顺序是
您最近一年使用:0次
20-21高三下·山东·阶段练习
名校
解题方法
3 . 下列实验操作、实验现象及解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 工业上用SiO2与焦炭在高温条件制备粗硅 | 生成可燃性气体,得到固体粗硅 | 非金属性:C>Si |
| B | 常温下,用pH计分别测定等体积1mol·L−1 CH3COONH4溶液和0.1mol·L−1 CH3COONH4溶液的pH | 测得pH都等于7 | 同温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| C | 向两支试管中各加入4mL 0.01mol·L−1 KMnO4溶液和4mL 0.1mol·L−1 KMnO4溶液,再分别通入足量SO2,分别记录溶液褪色所需的时间 | 0.1mol·L−1 KMnO4溶液褪色所需时间更短 | 其他条件相同时,增大反应物浓度,反应速率增大 |
| D | 往烧杯中加入约20g研细的Ba(OH)2·8H2O晶体和10gNH4Cl晶体,并将烧杯放在滴有水的玻璃片上,用玻璃棒迅速搅拌 | 有刺激性气味气体生成,烧杯底部结冰,与玻璃片粘在一起 | 吸热反应不一定需要加热才能进行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-16更新
|
600次组卷
|
5卷引用:学科网2021年高三3月大联考(山东卷)
(已下线)学科网2021年高三3月大联考(山东卷)山东省青岛第五十八中学2021-2022学年高三上学期期中考试化学试题河北省武邑中学2021届高三二模化学试题河北省石家庄市第二中学2021-2022学年高三上学期10月联考化学试题(已下线)第七单元 化学反应速率与化学平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)
名校
4 . (1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,下图能正确表示该反应中能量变化的是_______ 。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量_______ kJ。
(2)下列反应中,属于放热反应的是_______ ,属于吸热反应的是_______ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D 四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向_______ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为_______ 。
③四种金属活动性由强到弱的顺序是_______ 。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H—H | O=O | H—O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D 四种金属按下表中装置进行实验。
| 装置 | 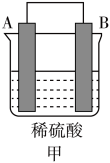 | 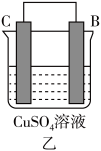 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
您最近一年使用:0次
2021-04-12更新
|
583次组卷
|
2卷引用:山东省泰安市宁阳一中2020-2021学年高一下学期第一次考试化学试题
名校
解题方法
5 . Ⅰ.(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,下图能正确表示该反应中能量变化的是__________ 。
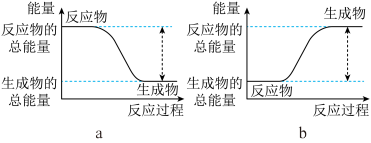
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量_________________ kJ。
(2)下列反应中,属于放热反应的是_________ ,属于吸热反应的是_________ 。
a.盐酸与烧碱溶液反应 b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
Ⅱ.A、B、C、D 四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向_____________ 极(填“正”或“负”)。
②装置乙中正极的电极反应式为_________________________ 。
③装置丙中溶液的pH__________________ (填“变大”“变小”或“不变”)。
④四种金属活动性由强到弱的顺序是___________________________ 。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H—H | O=O | H—O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出热量
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应 b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
Ⅱ.A、B、C、D 四种金属按下表中装置进行实验。
| 装置 | 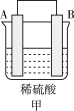 |  |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属活动性由强到弱的顺序是
您最近一年使用:0次
6 . 利用下列装置进行的实验,不能达到预期目的的是
 |  |  | 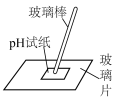 |
| A蒸发FeCl3溶液制备FeCl3固体 | B.探究双氧水分解的热效应 | C.制作水果(柠檬)电池 | D.粗测碳酸钠溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-21更新
|
267次组卷
|
3卷引用:山东省级联考2023-2024学年高二上学期12月月考化学试题
名校
解题方法
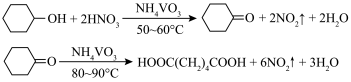
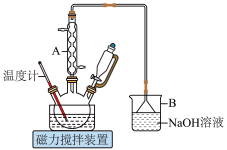
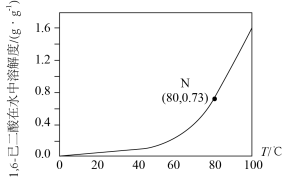
7 . 1,6己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为反应物制备1,6己二酸。反应原理为:
实验步骤如下:
Ⅰ.向三颈烧瓶中加入0.03 g NH4VO3固体和18 mL浓HNO3(略过量),向恒压滴液漏斗中加入6 mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60 ℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90 ℃水浴中加热10 min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100 mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)仪器A的名称为___________ ,其作用是___________ 。
(2)B中发生反应的离子方程式为___________ (其中一种产物为亚硝酸盐)
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为___________ ,滴加环己醇的过程中,若温度过高,可用冷水浴冷却维持50~60 ℃,说明该反应的ΔH___________ 0(填“>”或“<”)。
(4)将步骤Ⅲ补充完整:___________ 。步骤Ⅳ提纯方法的名称为___________ 。如图为1,6己二酸在水中的溶解度曲线,80 ℃时1,6-己二酸水溶液的密度为ρ g·mL-1;该溶液的物质的量浓度为___________ 。
| 试剂 | 相对分子质量 | 密度/(g·mL-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 100 | 0.962 | 25.9 | 161.8 | 可溶于水、乙醇、乙醚 |
| 1,6-己二酸 | 146 | 1.360 | 152 | 330.5 | 微溶于冷水,易溶于乙醇 |
| NH4VO3 | 117 | 2.326 | 210(分解) | — | 微溶于冷水,易溶于热水 |
Ⅰ.向三颈烧瓶中加入0.03 g NH4VO3固体和18 mL浓HNO3(略过量),向恒压滴液漏斗中加入6 mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60 ℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90 ℃水浴中加热10 min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100 mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)仪器A的名称为
(2)B中发生反应的离子方程式为
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为
(4)将步骤Ⅲ补充完整:
| A.46.07% | B.57.08% | C.63.03% | D.74.61% |
您最近一年使用:0次
2024-02-29更新
|
362次组卷
|
8卷引用:重点7 化学实验综合题-2021年高考化学【热点·重点·难点】专练(山东专用)
(已下线)重点7 化学实验综合题-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)东北三省三校(哈师大附中、东北师大附中、辽宁省实验中学)2021届高三第一次联合模拟考试(3月)理综化学试题(已下线)3.5.2 有机合成路线的设计与实施-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)(已下线)05 以分离提纯为主线的有机制备类综合实验 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型三 以分离提纯为主的有机制备类实验-备战2024年高考化学答题技巧与模板构建河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题四川省成都市第七中学林荫校区2023-2024学年高三下学期4月月考理科综合试卷-高中化学
8 . 氯仿( )常用作有机溶剂和麻醉剂,常温下在空气中易被氧化。实验室中可用热还原
)常用作有机溶剂和麻醉剂,常温下在空气中易被氧化。实验室中可用热还原 制备氯仿,装置示意图及有关物质性质如下:
制备氯仿,装置示意图及有关物质性质如下:
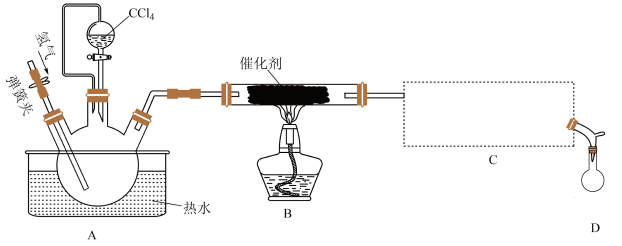
相关实验步骤如下:
①检查装置气密性;②开始通入氢气;③点燃B处酒精灯;④向A处水槽中加入热水,接通C处冷凝装置的冷水;⑤向三颈烧瓶中滴入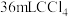 ;⑥反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量
;⑥反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量 溶液和水洗涤,分离出产物加入少量无水
溶液和水洗涤,分离出产物加入少量无水 ,静止后过滤;⑦对滤液进行蒸馏纯化,得到氯仿28.29g。
,静止后过滤;⑦对滤液进行蒸馏纯化,得到氯仿28.29g。
请回答下列问题:
(1)C处应选用冷凝管为___________ (填字母)。

(2)设计②③先后顺序的目的是___________ 。
(3)向A处水槽中加入热水的目的是___________ 。
(4)装置B处反应为可逆反应,停止加热一段时间后,发现催化剂仍保持红热状态,说明B处生成 反应的
反应的
___________ (填“<”或“>”)0,B中发生反应的化学方程式为___________ 。
(5)牛角管支管的作用是___________ 。
(6)该实验中氯仿产率为___________ (保留3位有效数字)。
 )常用作有机溶剂和麻醉剂,常温下在空气中易被氧化。实验室中可用热还原
)常用作有机溶剂和麻醉剂,常温下在空气中易被氧化。实验室中可用热还原 制备氯仿,装置示意图及有关物质性质如下:
制备氯仿,装置示意图及有关物质性质如下:
| 物质 | 相对分子质量 | 密度/( ) ) | 沸点/℃ | 溶解性 |
 | 119.5 | 1.50 | 61.3 | 难溶于水 |
 | 154 | 1.59 | 76.7 | 难溶于水 |
①检查装置气密性;②开始通入氢气;③点燃B处酒精灯;④向A处水槽中加入热水,接通C处冷凝装置的冷水;⑤向三颈烧瓶中滴入
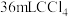 ;⑥反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量
;⑥反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量 溶液和水洗涤,分离出产物加入少量无水
溶液和水洗涤,分离出产物加入少量无水 ,静止后过滤;⑦对滤液进行蒸馏纯化,得到氯仿28.29g。
,静止后过滤;⑦对滤液进行蒸馏纯化,得到氯仿28.29g。请回答下列问题:
(1)C处应选用冷凝管为

(2)设计②③先后顺序的目的是
(3)向A处水槽中加入热水的目的是
(4)装置B处反应为可逆反应,停止加热一段时间后,发现催化剂仍保持红热状态,说明B处生成
 反应的
反应的
(5)牛角管支管的作用是
(6)该实验中氯仿产率为
您最近一年使用:0次
名校
解题方法
9 . 某同学利用如图装置模拟工业生产制备了少量硝酸,请结合所学知识完成下列问题。
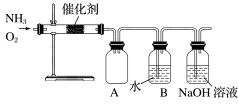
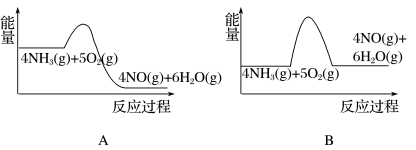
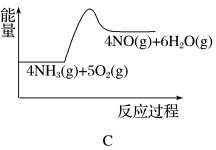
(1)实验时先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到 700℃以上。下列图示中,能够正确表示该反应过程能量变化的是_____ (填字母)。
(2)高温时,2NO2(g)⇌ 2NO(g)+O2(g),因此氨气与氧气反应难以生成 NO2 。根据下列数据计算,当 4molNO2 分解时,反应会________________ (填“吸收”或 “放出”)_____________________ kJ 能量。
NO2(g)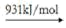 N(g)+2O(g)
N(g)+2O(g)
NO(g)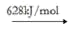 N(g)+O(g)
N(g)+O(g)
O2(g)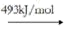 2O(g)
2O(g)
(3)在 2L 的恒温密闭容器中,通入等物质的量的 NO 和 O2 气体,n(NO)随时间的变化如下表:
①反应开始至第 1s 时,NO 的平均反应速率为_____ 。
②在第 5s 时,O2的转化率为_____ 。
③容器中混合气体压强与反应开始时的压强比值为_____ 。
④下列能说明反应已达平衡的是_____ 。
a.单位时间内,每生成一定物质的量浓度的 NO,同时有相同物质的量浓度的O2生成
b.气体混合物物质的量不再改变
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气的密度不再改变

(1)实验时先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到 700℃以上。下列图示中,能够正确表示该反应过程能量变化的是


(2)高温时,2NO2(g)⇌ 2NO(g)+O2(g),因此氨气与氧气反应难以生成 NO2 。根据下列数据计算,当 4molNO2 分解时,反应会
NO2(g)
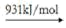 N(g)+2O(g)
N(g)+2O(g)NO(g)
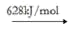 N(g)+O(g)
N(g)+O(g)O2(g)
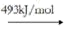 2O(g)
2O(g)(3)在 2L 的恒温密闭容器中,通入等物质的量的 NO 和 O2 气体,n(NO)随时间的变化如下表:
| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0 014 | 0.010 | 0.007 | 0.006 | 0.006 |
①反应开始至第 1s 时,NO 的平均反应速率为
②在第 5s 时,O2的转化率为
③容器中混合气体压强与反应开始时的压强比值为
④下列能说明反应已达平衡的是
a.单位时间内,每生成一定物质的量浓度的 NO,同时有相同物质的量浓度的O2生成
b.气体混合物物质的量不再改变
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气的密度不再改变
您最近一年使用:0次
名校
10 . 下列实验现象中,不能说明相应的化学反应是放热反应的是( )
| 选项 | A | B | C | D |
| 实验 装置 |  | 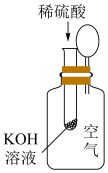 | 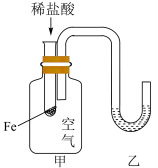 |  |
| 实验现象 | 温度计的示数不断增大 | 反应开始后,气球慢慢胀大 | 反应开始后,甲侧液面低于乙侧液面 | 反应开始后,针筒活塞向右移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-02-11更新
|
608次组卷
|
3卷引用:山东省新泰市第一中学老校区(新泰中学)2023-2024学年高二上学期第一次质量检测化学试题



