山东省邹城市2020-2021学年高一下学期期中质量检测化学试题
山东
高一
期中
2021-05-28
301次
整体难度:
容易
考查范围:
化学与STSE、常见无机物及其应用、认识化学科学、化学反应原理、化学实验基础
一、单选题 添加题型下试题
| A.工业生产玻璃、水泥和陶瓷,均需用石灰石作原料 |
| B.二氧化硫可做漂白剂、防腐剂,还是一种食品添加剂 |
| C.汽车尾气中的氮氧化物与碳氢化合物反应可形成光化学烟雾 |
| D.“超轻海绵”使用的石墨烯是新型无机非金属材料 |
【知识点】 化学对材料制造和应用的作用解读 传统硅酸盐材料 新型无机非金属材料
A.铁片与稀 反应 反应 | B.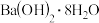 与 与 的反应 的反应 |
| C.红热的碳与水蒸气反应 | D. 与 与 反应 反应 |
【知识点】 氧化还原反应定义、本质及特征解读 吸热反应和放热反应解读
| A.氨水中滴入酚酞变红色,是因为氨水是一种弱碱 |
B.氨水中物质的量浓度最大的粒子是 (除水外) (除水外) |
C.在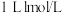 的氨水中含N原子的数目为 的氨水中含N原子的数目为 |
D. 具有一定的还原性,在一定条件下可被 具有一定的还原性,在一定条件下可被 氧化 氧化 |
| A.该反应中,热能转化为生成物的内部能量 |
| B.反应物的总能量高于生成物的总能量 |
C.由实验现象可知反应: 一定为吸热反应 一定为吸热反应 |
| D.该反应可以设计成原电池装置 |
【知识点】 化学能与热能的相互转化解读 吸热反应和放热反应解读 原电池概念及组成
| a | b | c | |
| 反应速率 | 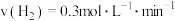 |  | 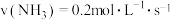 |
A.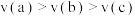 | B.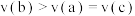 |
C. | D.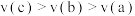 |
【知识点】 化学反应速率与化学计量数之间的关系解读
| 气体(杂质) | 方法 | |
| A | 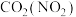 | 通过氢氧化钠溶液 |
| B |  | 通过饱和食盐水 |
| C | 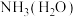 | 通过碱石灰固体 |
| D | 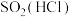 | 通过饱和亚硫酸氢钠溶液 |
| A.A | B.B | C.C | D.D |
【知识点】 物质分离、提纯的常见化学方法解读
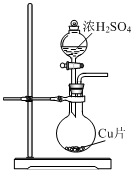
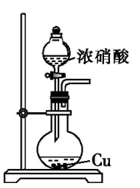
| A.浓硫酸具有吸水性,故可作干燥剂 |
| B.浓硫酸、浓硝酸与金属反应时只体现氧化性 |
| C.常温下可以用铁或铝制容器盛装浓硫酸和浓硝酸 |
D.在稀硫酸中加入铜粉,铜粉不溶解,再加入 固体,铜粉溶解 固体,铜粉溶解 |
A. 通入 通入 溶液中 溶液中 | B. 通入的 通入的 溶液中 溶液中 |
C. 通入 通入 溶液中 溶液中 | D. 通入 通入 溶液中 溶液中 |
 制备纯的
制备纯的 流程如图所示,下列说法不正确的是
流程如图所示,下列说法不正确的是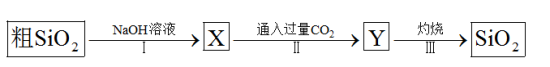
A. 属于酸性氧化物 属于酸性氧化物 |
| B.二氧化硅是将太阳能转变为电能的常用材料 |
| C.若在实验室中完成步骤Ⅲ,应该在坩埚中进行 |
D.步骤Ⅱ反应的离子方程式为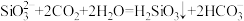 |
【知识点】 二氧化硅 硅酸钠与二氧化碳反应解读
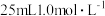 硫酸溶液与过量锌粒反应制取氢气,欲加快化学反应速率而不改变产生氢气的量,下列措施不可行的是
硫酸溶液与过量锌粒反应制取氢气,欲加快化学反应速率而不改变产生氢气的量,下列措施不可行的是| A.升高温度 | B.换用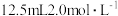 硫酸溶液 硫酸溶液 |
| C.改用等质量的锌粉 | D.滴加较多量硫酸铜 |
【知识点】 浓度对化学反应速率的影响解读 温度对化学反应速率的影响解读
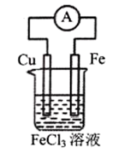
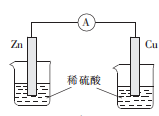
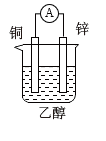
A.总反应方程式为 |
| B.铜为负极,发生氧化反应 |
C.装置工作时,溶液中的 向铁极移动 向铁极移动 |
D.装置工作时每转移 电子,将消耗 电子,将消耗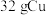 |
 )是有机合成中的重要试剂,由
)是有机合成中的重要试剂,由 与
与 反应制取
反应制取 的反应为:
的反应为: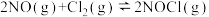 。对该反应下列分析错误的是
。对该反应下列分析错误的是A.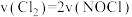 |
| B.使用催化剂是为了增大反应速率,提高生产效率 |
| C.通过调控反应条件,可以提高该反应进行的程度 |
| D.若恒温、恒容,不能根据反应体系中气体的密度保持不变来判断是否达到化学平衡状态 |
【知识点】 化学平衡的移动及其影响因素
 )气溶胶是PM2.5的成分之一、近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
)气溶胶是PM2.5的成分之一、近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图: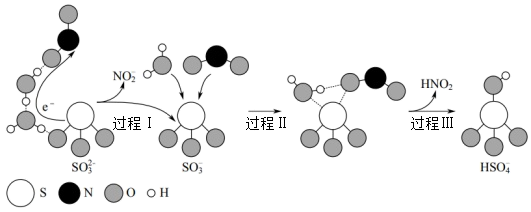
下列说法错误的是
A.过程I中的离子方程式为 |
| B.硫酸盐气溶胶呈酸性 |
| C.过程III的反应没有电子转移 |
| D.雾霾微颗粒中既含有硫酸盐,也含有亚硝酸盐(或硝酸盐) |
【知识点】 氧化还原反应的应用 氧化还原反应方程式的配平解读
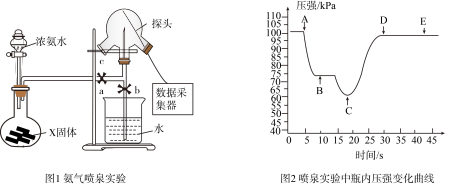
A.图1烧瓶中固体X可以是 或 或 |
| B.工业上,若出现液氨泄漏,喷洒稀盐酸比喷洒水处理效果好 |
C.将湿润的蓝色石蕊试纸置于三颈烧瓶c口,试纸变红,说明 已经集满 已经集满 |
| D.关闭a,封闭c,打开b,引发喷泉实验,三颈烧瓶内压强变化如图2,则C点时喷泉最剧烈 |
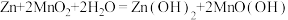 ,[已知
,[已知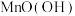 中
中 的化合价为+3]。下列有关说法错误的是
的化合价为+3]。下列有关说法错误的是
| A.薄层纸片的作用为载体和传导体 |
B.该新型电池工作时,电子由 沿内电路流回 沿内电路流回 |
C. 为正极材料,电极反应式为 为正极材料,电极反应式为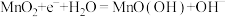 |
D.每转移 电子,负极材料质量增加17g 电子,负极材料质量增加17g |
【知识点】 原电池电极反应式书写解读 锰锌干电池解读
 完全溶于适量浓硝酸中,收集到氮的氧化物(含
完全溶于适量浓硝酸中,收集到氮的氧化物(含 )的混合物,这些气体恰好能
)的混合物,这些气体恰好能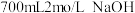 溶液完全吸收,生成只含
溶液完全吸收,生成只含 和
和 的盐溶液,其中
的盐溶液,其中 的物质的量为
的物质的量为A.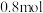 | B.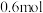 | C.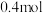 | D. |
二、解答题 添加题型下试题
 制取、收集、吸收,以及
制取、收集、吸收,以及 的还原性探究进行了如下实验设计。
的还原性探究进行了如下实验设计。I.
 的收集和吸收
的收集和吸收(1)若用图甲装置,排空气法收集
 ,气体应从
,气体应从
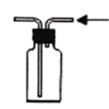
(2)已知
 难溶于
难溶于 。图乙、丙、丁、戊四种装置中,不能用来吸收
。图乙、丙、丁、戊四种装置中,不能用来吸收 的是
的是II.
 的还原性探究利用下列装置,进行
的还原性探究利用下列装置,进行 还原
还原 的反应。
的反应。
已知:
 与
与 反应的生成物为
反应的生成物为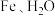 和难溶于水的气体X,且X不被浓硫酸和碱石灰吸收。
和难溶于水的气体X,且X不被浓硫酸和碱石灰吸收。(3)写出A装置发生反应的化学方程式
(4)按气流方向正确的装置连接顺序为A→ → → → →C(填序号,每个装置只用一次)
(5)实验结束时,应首先
①熄灭A装置的酒精灯 ②熄灭B装置的酒精灯
(6)若称取1.6克
 完全反应后,测得生成气体X的体积为
完全反应后,测得生成气体X的体积为 (已折算为标准状况),通过计算推测B中
(已折算为标准状况),通过计算推测B中 与
与 反应的化学方程式为
反应的化学方程式为 与
与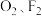 均能发生反应,如图为
均能发生反应,如图为 与
与 发生反应生成
发生反应生成 过程中的能量变化示意图。请回答下列问题:
过程中的能量变化示意图。请回答下列问题: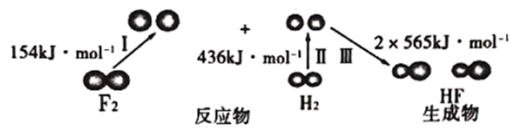
①完成转化I、II
②
 和
和 反应的能量变化图可用
反应的能量变化图可用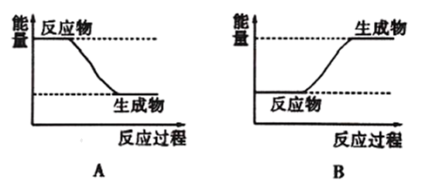
(2)科研人员设想用如图所示装置生产硫酸。
①a电极反应式为
 向
向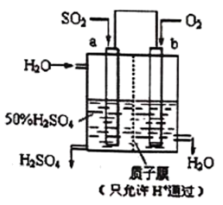
②该小组同学反思原电池的原理,其中观点正确的是
A.原电池反应的过程中可能没有电子发生转移
B.原电池装置一定需要2个活泼性不同的金属电极
C.负极电极材料不一定参加电极反应
D.氧化反应和还原反应可以拆开在两极发生
【知识点】 化学键与化学反应中的能量关系解读 原电池原理理解解读
 )常用作食品漂白剂。其制备工艺流程如图:
)常用作食品漂白剂。其制备工艺流程如图:
已知:反应II包含
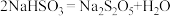 等多步反应。
等多步反应。(1)反应I进行时应先通入的气体是
(2)
 灼烧前粉碎,目的是
灼烧前粉碎,目的是(3)已知
 与稀硫酸反应放出
与稀硫酸反应放出 ,其离子方程式为
,其离子方程式为(4)副产品X的化学式是
(5)为了减少产品
 中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为
中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为①澄清石灰水 ②饱和碳酸氢钠溶液 ③氢氧化钠 ④酸性高锰酸 ⑤稀硫酸
【知识点】 二氧化硫的弱氧化性解读 物质分离、提纯综合应用解读
三、填空题 添加题型下试题

请回答下列问题:
(1)a=
(2)平衡时Y的转化率=
(3)下列叙述中,能说明上述反应达到平衡状态的是
a.气体总物质的量不变 b.单位时间内消耗1molY,同时生成amolZ
c.气体的平均摩尔质量保持不变 d.X和Y的物质的量之比保持不变
II.某探究性学习小组在20℃进行“碘钟”实验,得到的数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
c(S2O )/mol·L-1 )/mol·L-1 | 0.040 | 0.040 | 0.080 | x | 0.040 |
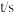 | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
已知:“碘钟”实验化学方程式为
 ,用
,用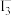 与加入的淀粉溶液显蓝色的时间t来度量反应速率,t越小,反应速率越大。则表中
与加入的淀粉溶液显蓝色的时间t来度量反应速率,t越小,反应速率越大。则表中 的浓度x=
的浓度x=试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 化学对材料制造和应用的作用 传统硅酸盐材料 新型无机非金属材料 | |
| 2 | 0.94 | 浓硫酸的吸水性 硫化氢 亚铁盐溶液的配制与保存 亚硫酸及其盐 | |
| 3 | 0.65 | 氧化还原反应定义、本质及特征 吸热反应和放热反应 | |
| 4 | 0.65 | 氨的还原性 氨水的成分 氨水其他方面的有关计算 | |
| 5 | 0.85 | 化学能与热能的相互转化 吸热反应和放热反应 原电池概念及组成 | |
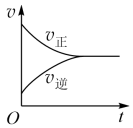
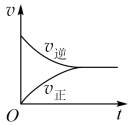
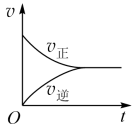
| 6 | 0.85 | 化学平衡建立的过程 | |
| 7 | 0.65 | 化学反应速率与化学计量数之间的关系 | |
| 8 | 0.94 | 原电池 原电池概念及组成 原电池的结构 | |
| 9 | 0.85 | 物质分离、提纯的常见化学方法 | |
| 10 | 0.65 | 硝酸的强氧化性 酸的通性 浓硫酸的吸水性 浓硫酸的强氧化性 | |
| 11 | 0.85 | 二氧化氮与水反应 二氧化硫与二氧化碳的性质区别 其他含铝化合物 | |
| 12 | 0.94 | 二氧化硅 硅酸钠与二氧化碳反应 | |
| 13 | 0.65 | 浓度对化学反应速率的影响 温度对化学反应速率的影响 | |
| 14 | 0.94 | 氯气的实验室制法 一氧化氮的化学性质 硝酸的强氧化性 二氧化硫的制备 | |
| 15 | 0.65 | 原电池原理理解 原电池正负极判断 原电池电极反应式书写 | |
| 16 | 0.65 | 化学平衡的移动及其影响因素 | |
| 17 | 0.65 | 氧化还原反应的应用 氧化还原反应方程式的配平 | |
| 18 | 0.65 | 氨的碱性 氨的喷泉实验 氨气的实验室制法 | |
| 19 | 0.4 | 原电池电极反应式书写 锰锌干电池 | |
| 20 | 0.85 | 基于氧化还原反应守恒规律的计算 二氧化氮与碱液的反应 铜与强氧化性酸的反应 | |
| 二、解答题 | |||
| 21 | 0.85 | 氨气的制备 氨的还原性 常见气体的制备与收集 物质性质的探究 | 实验探究题 |
| 22 | 0.65 | 化学键与化学反应中的能量关系 原电池原理理解 | 原理综合题 |
| 23 | 0.65 | 二氧化硫的弱氧化性 物质分离、提纯综合应用 | 工业流程题 |
| 三、填空题 | |||
| 24 | 0.65 | 化学反应的速率 浓度对化学反应速率的影响 化学平衡状态的判断方法 转化率的相关计算及判断 | |

 ,反应过程中正、逆反应速率v随时间t的变化情况正确的是
,反应过程中正、逆反应速率v随时间t的变化情况正确的是