名校
1 . 恒温恒容,4A(s)+3B(g) 2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是
2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是
 2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是
2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是| A.用A表示的反应速率是0.4mol•L-1•min-1 |
| B.气体的密度不再变化,则证明反应已经达到平衡状态 |
| C.2min末的反应速率v(B)=0.3mol•L-1•min-1 |
| D.分别用B、C表示反应的速率,其关系是:3v(B)=2v(C) |
您最近一年使用:0次
2023-04-22更新
|
278次组卷
|
2卷引用:四川省巴中市恩阳区2022-2023学年高二上学期1月期末化学试题
名校
解题方法
2 . 实验室利用下列方案探究影响化学反应速率的因素,实验时,分别量取 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定 溶液褪色时间来判断反应的快慢。请回答相关问题:
溶液褪色时间来判断反应的快慢。请回答相关问题:
(1)该反应的离子方程式为___________ 。
(2)实验①、②、③所加 溶液均要过量,理由是
溶液均要过量,理由是___________ 。
(3)实验①和实验②是探究___________ 对化学反应速率的影响。
(4)实验②测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=___________ 。
(5)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是___________ 。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的___________ (填字母)。
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定 溶液褪色时间来判断反应的快慢。请回答相关问题:
溶液褪色时间来判断反应的快慢。请回答相关问题:| 编号 | 温度/℃ |  溶液 溶液 | 酸性 溶液 溶液 | ||
浓度/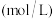 | 体积/ | 浓度/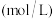 | 体积/ | ||
| ① | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| ② | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| ③ | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
(2)实验①、②、③所加
 溶液均要过量,理由是
溶液均要过量,理由是(3)实验①和实验②是探究
(4)实验②测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=
(5)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
您最近一年使用:0次
2023-10-07更新
|
28次组卷
|
2卷引用:四川省绵阳南山中学实验学校2023-2024学年高二上学期9月月考化学试题
解题方法
3 . 请根据要求回答相关问题:
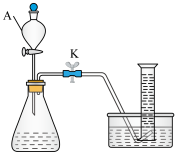
I.某小组用下图装置探究H2C2O₄溶液与酸性KMnO4溶液的反应(夹持装置略去)。
(1)仪器A的名称为___________ 。
(2)H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为___________ 。
(3)若以单位时间内生成的气体体积作为反应速率的观测指标,则量筒中最佳试剂为___________。
Ⅱ.某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(4)①T1=___________ ;V2=___________ 。
②若t1<8,则由此实验可以得出的结论是___________ 。
③忽略溶液体积的变化,利用实验②中数据计算,0~8s内,用KMnO4的浓度变化表示的反应速率v=___________ 。(保留3个有效数字)
④H2C2O4溶液与酸性KMnO4溶液生成的Mn2+对该反应有催化作用。请以实验1为对照组,设计实验方案证明Mn2+的催化作用___________ 。

I.某小组用下图装置探究H2C2O₄溶液与酸性KMnO4溶液的反应(夹持装置略去)。
(1)仪器A的名称为
(2)H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为
(3)若以单位时间内生成的气体体积作为反应速率的观测指标,则量筒中最佳试剂为___________。
| A.饱和NaHCO3溶液 | B.饱和NaCl溶液 |
| C.水 | D.饱和Na2CO3溶液 |
Ⅱ.某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
| 实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol/L | V/mL | c/mol/L | V/mL | |||
| ① | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| ② | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| ③ | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(4)①T1=
②若t1<8,则由此实验可以得出的结论是
③忽略溶液体积的变化,利用实验②中数据计算,0~8s内,用KMnO4的浓度变化表示的反应速率v=
④H2C2O4溶液与酸性KMnO4溶液生成的Mn2+对该反应有催化作用。请以实验1为对照组,设计实验方案证明Mn2+的催化作用
您最近一年使用:0次
2023高一下·浙江·期中
名校
4 . 某学习小组为了探究影响高锰酸钾酸性溶液与NaHSO3溶液反应速率的因素,该小组设计如表实验方案。
下列说法正确的是
| 实验 | V(NaHSO3)/mL c=0.1 mol/L | V(KMnO4)/mL c=0.6 mol/L | V(H2SO4)/mL c=0.1 mol/L | V(MnSO4)/mL c=0.1 mol/L | V(H2O)/mL | 褪色时间t/min |
| 1 | 3.0 | 2.0 | 1.0 | 0.0 | 2.0 | 8 |
| 2 | 3.0 | 2.0 | 2.0 | 0.0 | a | 6 |
| 3 | 4.0 | 2.0 | 2.0 | 0.0 | 0.0 | 4 |
| 4 | 4.0 | 2.0 | 1.0 | 0.5 | b | 3 |
A.该反应的离子方程式为:5 +2 +2 +6H+=2Mn2++5 +6H+=2Mn2++5 +3H2O +3H2O |
| B.a=1.0,b=0.5 |
C.实验3从反应开始到反应结束这段时间内反应速率v( )=0.025 mol/(L∙min) )=0.025 mol/(L∙min) |
D.实验证明 可能是该反应的催化剂 可能是该反应的催化剂 |
您最近一年使用:0次
2023-04-25更新
|
356次组卷
|
3卷引用:【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】
(已下线)【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题山东省东营市利津县高级中学2022-2023学年高一下学期5月月考化学试题
名校
解题方法
5 . 下列装置进行的相应实验,能达到实验目的的是
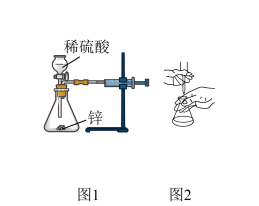



| A.图1装置可用于测定H2的生成速率(mL/s) |
| B.图2装置为用氢氧化钠标准溶液滴定未知浓度的盐酸溶液 |
| C.图3装置可证明元素的非金属性:Cl>C>Si |
| D.图4装置模拟“候氏制碱法”制取NaHCO3,应先从a通入NH3,后从b通入CO2,c中放蘸有稀硫酸的脱脂棉 |
您最近一年使用:0次
2023-06-26更新
|
133次组卷
|
2卷引用:河北省“五个一”名校联盟2022-2023学年高二下学期6月联考化学试题
解题方法
6 . 用 溶液氧化废水中的还原性污染物M,为研究降解效果。设计如下对比实验,探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示:
溶液氧化废水中的还原性污染物M,为研究降解效果。设计如下对比实验,探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示:

下列说法正确的是
 溶液氧化废水中的还原性污染物M,为研究降解效果。设计如下对比实验,探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示:
溶液氧化废水中的还原性污染物M,为研究降解效果。设计如下对比实验,探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示:| 实验编号 | 温度/℃ | pH |
| ① | 25 | 1 |
| ② | 45 | 1 |
| ③ | 25 | 7 |
| ④ | 25 | 1 |

下列说法正确的是
A.实验①在15min内M的降解速率为 |
| B.若其他条件相同,实验①②说明升高温度,M降解速率增大 |
| C.若其他条件相同,实验①③证明pH越小,越有利于M的降解 |
| D.实验②④说明M的浓度越小,降解的速率越慢 |
您最近一年使用:0次
名校
解题方法
7 . 实验小组探究 溶液与
溶液与 溶液的反应及其速率,实验过程和现象如表。已知:
溶液的反应及其速率,实验过程和现象如表。已知:
i、 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;
ii、淀粉检测 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝:
即可快速变蓝:
iii、可与 发生反应:
发生反应: 。
。
(1)实验1-1的目的是___________ 。
(2) 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
为了研究 与
与 反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
(3)实验2-1不能用于测定 与KI反应的速率,原因除变色时间过短外还有
与KI反应的速率,原因除变色时间过短外还有___________ 。
(4)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
猜想1: 先与
先与 反应,使
反应,使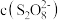 降低;
降低;
猜想2: 先与
先与 反应,___________。
反应,___________。
①甲同学提出猜想1的依据:由信息iii推测, 的还原性
的还原性___________ (填“强于”或“弱于”) 的。
的。
②乙同学根据现有数据证明猜想1不成立,理由是___________ 。
③补全猜想2:___________ 。
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算 内的平均反应速率
内的平均反应速率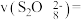
___________  (写出计算式)。
(写出计算式)。
 溶液与
溶液与 溶液的反应及其速率,实验过程和现象如表。已知:
溶液的反应及其速率,实验过程和现象如表。已知:i、
 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;ii、淀粉检测
 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝:
即可快速变蓝:iii、可与
 发生反应:
发生反应: 。
。| 编号 | 1-1 | 1-2 |
| 实验操作 | 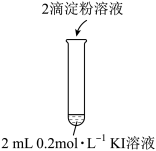 | 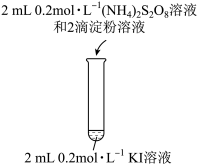 |
| 现象 | 无明显现象 | 溶液立即变蓝 |
(2)
 与
与 反应的离子方程式为
反应的离子方程式为为了研究
 与
与 反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。| 编号 | 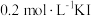 溶液 溶液 | 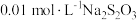 溶液 溶液 | 蒸馏水 | 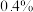 的淀粉溶液/滴 的淀粉溶液/滴 | 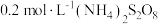 溶液 溶液 | 变色时间/s |
| 2-1 | 2 | 0 | 2.8 | 2 | 0.2 | 立即 |
| 2-2 | 2 | 0.8 | 0.2 | 2 | 0 | 30 |
 与KI反应的速率,原因除变色时间过短外还有
与KI反应的速率,原因除变色时间过短外还有(4)加入
 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。猜想1:
 先与
先与 反应,使
反应,使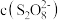 降低;
降低;猜想2:
 先与
先与 反应,___________。
反应,___________。①甲同学提出猜想1的依据:由信息iii推测,
 的还原性
的还原性 的。
的。②乙同学根据现有数据证明猜想1不成立,理由是
③补全猜想2:
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算
 内的平均反应速率
内的平均反应速率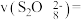
 (写出计算式)。
(写出计算式)。
您最近一年使用:0次
名校
8 . 温度为T1时,向1L的恒容反应器中充入2molCH4,只发生2CH4(g) C2H4(g)+2H2(g) ΔH>0,上述反应过程中0~15minCH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
C2H4(g)+2H2(g) ΔH>0,上述反应过程中0~15minCH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
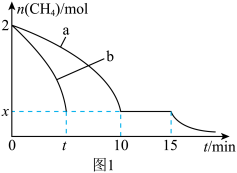
(1)0~10min内CH4表示的反应速率为___________ mol/(L·min)。
(2)下列叙述能证明该反应已经达到化学平衡状态的是(填序号)___________。
(3)若图1中曲线a、曲线b分别表示在温度T1时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(CH4)变化曲线,其中表示催化剂表面积较大的曲线是___________ (填“a”或“b”)。
(4)15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是___________
(5)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2)其中k正、k逆为速率常数仅与温度有关,T1温度时k正与k逆的比值为___________ (填数值)。若将温度由T1升高到T2,则反应速率增大的倍数v正___________ v逆(填“>”“=”或“<”),判断的理由是___________ 。
 C2H4(g)+2H2(g) ΔH>0,上述反应过程中0~15minCH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
C2H4(g)+2H2(g) ΔH>0,上述反应过程中0~15minCH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
(1)0~10min内CH4表示的反应速率为
(2)下列叙述能证明该反应已经达到化学平衡状态的是(填序号)___________。
| A.容器内混合气体密度不再变化 |
| B.容器内气体压强不再变化 |
| C.2v(CH4)正=v(C2H4)逆 |
| D.单位时间内消耗1molCH4同时消耗1molH2 |
(4)15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是___________
| A.升高温度 | B.改用高效催化剂 | C.扩大容器的体积 | D.增加CH4的浓度 |
您最近一年使用:0次
9 . 氨作为一种重要的化工原料,应用广泛。请回答下列有关问题:
(1)实验室中采用铵盐制备氨气的化学方程式为___________ ,常用___________ 检验氨气的存在。下列尾气处理装置可用于吸收氨气的是___________ (填字母)。
A. B.
B.  C.
C.
(2)某温度下,在一个2L的恒容密闭容器中进行氨的合成,氨气、氮气和氢气三种物质的物质的量随时间的变化曲线如图所示。

①0~2min内,用氢气表示的平均反应速率为___________ 。
②下列能证明某恒温恒容密闭容器中的合成氨反应已达到平衡状态的是___________ (填字母)。
A.容器中混合气体的总压强保持不变
B.容器中 的体积分数保持不变
的体积分数保持不变
C.容器中 、
、 和
和 的物质的量之比为1∶3∶2
的物质的量之比为1∶3∶2
D.容器中 的正反应速率和
的正反应速率和 的逆反应速率相等
的逆反应速率相等
(3)在催化剂和加热的条件下,将氨气氧化为一氧化氮是工业制硝酸的重要反应,该反应的化学方程式是___________ 。在催化剂和加热条件下,氨气与一氧化氮也会发生反应生成无污染氮气,其化学方程式为___________ 。
(1)实验室中采用铵盐制备氨气的化学方程式为
A.
 B.
B.  C.
C.
(2)某温度下,在一个2L的恒容密闭容器中进行氨的合成,氨气、氮气和氢气三种物质的物质的量随时间的变化曲线如图所示。

①0~2min内,用氢气表示的平均反应速率为
②下列能证明某恒温恒容密闭容器中的合成氨反应已达到平衡状态的是
A.容器中混合气体的总压强保持不变
B.容器中
 的体积分数保持不变
的体积分数保持不变C.容器中
 、
、 和
和 的物质的量之比为1∶3∶2
的物质的量之比为1∶3∶2D.容器中
 的正反应速率和
的正反应速率和 的逆反应速率相等
的逆反应速率相等(3)在催化剂和加热的条件下,将氨气氧化为一氧化氮是工业制硝酸的重要反应,该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
10 . 实验小组探究 溶液与KI溶液的反应及其速率,实验操作和现象如下。
溶液与KI溶液的反应及其速率,实验操作和现象如下。
已知:ⅰ. 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;
ⅱ.淀粉检测 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;
ⅲ. 可与
可与 发生反应:
发生反应: 。
。
(1)实验1-1的目的是_______ 。
(2) 与KI反应的离子方程式为
与KI反应的离子方程式为_______ 。
为了研究 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如下表。
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如下表。
(3)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:
溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:
猜想1: 先与
先与 反应,使
反应,使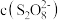 降低;
降低;
猜想2: 先与KI反应,_______。
先与KI反应,_______。
①甲同学提出猜想1的依据:由信息ⅲ推测, 的还原性
的还原性_______ (填“强于”或“弱于”)KI的。
②乙同学根据现有数据证明猜想1不成立,理由是_______ 。
③补全猜想2:_______ 。
(4)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率
_______  (写出计算式即可)。
(写出计算式即可)。
(5)实验2-2中,30s内未检测到 与
与 反应,可能的原因是
反应,可能的原因是_______ 。
 溶液与KI溶液的反应及其速率,实验操作和现象如下。
溶液与KI溶液的反应及其速率,实验操作和现象如下。已知:ⅰ.
 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;ⅱ.淀粉检测
 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;ⅲ.
 可与
可与 发生反应:
发生反应: 。
。| 编号 | 1-1 | 1-2 |
| 实验操作 | 2滴淀粉溶液 2mL  KI溶液 KI溶液 | 2mL   溶液和2滴淀粉溶液 溶液和2滴淀粉溶液 2mL  KI溶液 KI溶液 |
| 现象 | 无明显现象 | 溶液立即变蓝 |
(2)
 与KI反应的离子方程式为
与KI反应的离子方程式为为了研究
 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如下表。
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如下表。| 编号 |  KI溶液/mL KI溶液/mL |   溶液/mL 溶液/mL | 蒸馏水/mL | 淀粉溶液/滴 |   溶液/mL 溶液/mL | 变色时间/s |
| 2-1 | 2 | 0 | 2.8 | 2 | 0.2 | 立即 |
| 2-2 | 2 | 0.8 | 0.2 | 2 | 2 | 30 |
 溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:
溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:猜想1:
 先与
先与 反应,使
反应,使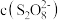 降低;
降低;猜想2:
 先与KI反应,_______。
先与KI反应,_______。①甲同学提出猜想1的依据:由信息ⅲ推测,
 的还原性
的还原性②乙同学根据现有数据证明猜想1不成立,理由是
③补全猜想2:
(4)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率

 (写出计算式即可)。
(写出计算式即可)。(5)实验2-2中,30s内未检测到
 与
与 反应,可能的原因是
反应,可能的原因是
您最近一年使用:0次



