1 . 下列有说法正确的是
| A.对反应A→B,1min内消耗4molA的反应速率一定比1min内消耗2molA的反应速率快 |
| B.糕点包装袋内放置抗氧化剂是为了减缓食物氧化速率 |
C.实验室用盐酸跟锌片反应制 ,用粗锌比纯锌速率快,主要目的是为了增大锌片和盐酸的接触面积从而加快反应速率 ,用粗锌比纯锌速率快,主要目的是为了增大锌片和盐酸的接触面积从而加快反应速率 |
| D.水结冰的过程不能自发进行的原因是熵减的过程,改变条件也不可能自发进行 |
您最近一年使用:0次
名校
解题方法
2 . 某实验小组探究NiO能否催化NO和CO反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②
 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是


 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
A.从理论上推断, 与 与 生成 生成 和 和 的反应,高温有利于自发进行 的反应,高温有利于自发进行 |
B.在空气中加热 可制备NiO 可制备NiO |
C.打开装置1中气球,通过观察气体是否变为红棕色判断是否生成 |
D.若以上实验证明 能够成功催化该反应,且固体A是 能够成功催化该反应,且固体A是 ,则装置2中的反应方程式为: ,则装置2中的反应方程式为: |
您最近一年使用:0次
2022-11-28更新
|
344次组卷
|
5卷引用:湖北省荆州中学2023-2024学年高三上学期10月半月考化学试题
湖北省荆州中学2023-2024学年高三上学期10月半月考化学试题重庆2023届拔尖强基联合11月定时检测化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)重庆市西南大学附属中学校2022-2023学年高三上学期11月拔尖强基联合定时检测化学试题四川外国语大学附属外国语学校2024届高三上学期10月月考化学试题
解题方法
3 . 二氧化碳甲烷化助力我国2060年前实现“碳中和”,其中涉及的主要反应如下:
反应Ⅰ:CO₂(g)+4H₂(g) CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹
CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹
反应Ⅱ:CO₂(g)+H₂(g) CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹
CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹
回答下列问题:
(1)由热化学方程式可知,反应Ⅰ属于反应_______(填写序号)
(2)动力学研究:在多个1L恒容密闭装置中,分别充入1molCO₂和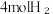 发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为
发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为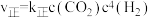 ,
,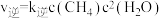 ,其中
,其中 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。

①图1中,至a点的H₂平均反应速率为_______  。
。
②图1中,v(a)逆_______ v(c)逆(填“>”、“=”或“<”)。
③图1中c点的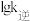 对应的是图2中的
对应的是图2中的_______ 点。
④图1中a点的v正,v逆与a点的K(平衡常数)、Q(浓度商)的关系是
______ 。
(3)热动力学研究:向10L的恒压密闭装置中充入5mol CO₂和20mol H₂,在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,得到平衡时各含碳物质的物质的量n(X)与温度T的关系如下图所示。

①当反应Ⅰ和反应Ⅱ均达到化学平衡状态时,维持温度不变,压缩装置体积,则反应Ⅱ的平衡移动方向是_______ (填序号)。
A.正向移动 B.逆向移动 C.不移动 D.无法确定
②曲线Z表示的是_______ (填写含碳元素物质的化学式)的物质的量与温度的关系,简述其在温度段500K~800K物质的量增大的原因_______ 。
③800K时,反应Ⅱ的平衡常数为_______ (计算结果保留两位有效数字)。
反应Ⅰ:CO₂(g)+4H₂(g)
 CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹
CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹反应Ⅱ:CO₂(g)+H₂(g)
 CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹
CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹回答下列问题:
(1)由热化学方程式可知,反应Ⅰ属于反应_______(填写序号)
| A.高温自发 | B.低温自发 | C.恒自发 | D.恒不自发 |
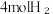 发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为
发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为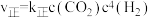 ,
,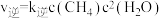 ,其中
,其中 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。
①图1中,至a点的H₂平均反应速率为
 。
。②图1中,v(a)逆
③图1中c点的
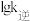 对应的是图2中的
对应的是图2中的④图1中a点的v正,v逆与a点的K(平衡常数)、Q(浓度商)的关系是

(3)热动力学研究:向10L的恒压密闭装置中充入5mol CO₂和20mol H₂,在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,得到平衡时各含碳物质的物质的量n(X)与温度T的关系如下图所示。

①当反应Ⅰ和反应Ⅱ均达到化学平衡状态时,维持温度不变,压缩装置体积,则反应Ⅱ的平衡移动方向是
A.正向移动 B.逆向移动 C.不移动 D.无法确定
②曲线Z表示的是
③800K时,反应Ⅱ的平衡常数为
您最近一年使用:0次
名校
4 . 某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数如下表所示。请回答下列问题:
(1)根据上述反应可推导出 、
、 与
与 之间的关系:
之间的关系:
_______ ;
(2)根据反应③判断熵变
_______ 0(填“>”“=”或“<”),依据反应自发进行的判据:ΔG=ΔH-TΔS<0时反应可自发进行,判断:在_______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)500℃下,测得反应③在某时刻时,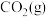 、
、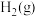 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,则此时v正
,则此时v正____ v逆(填“>”“=”或“<”)。
(4)提高反应③的反应速率且增大 的产率,可采取的措施_______。
的产率,可采取的措施_______。
(5) 捕获和转化可减少
捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应④完成之后,以
排放并实现资源利用,原理如图1所示。反应④完成之后,以 为载气,将恒定组成的
为载气,将恒定组成的 、
、 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
,在催化剂上有积碳。
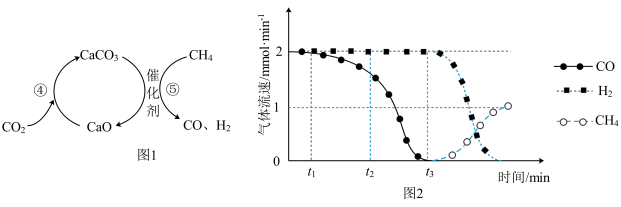
则反应⑤的化学方程式为_______ ,下列叙述正确的是_______ 。
A.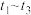 ,
, 比
比 多,且生成
多,且生成 速率不变,有可能是发生副反应
速率不变,有可能是发生副反应
B. 时刻,副反应生成
时刻,副反应生成 的速率大于反应⑤生成
的速率大于反应⑤生成 速率
速率
C. 之后,生成
之后,生成 的速率为0,是因为反应⑤不再发生
的速率为0,是因为反应⑤不再发生
| 化学反应 | 平衡常数 | |||
| 500℃ | 700℃ | 800℃ | ||
①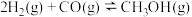  |  | 2.5 | 0.34 | 0.15 |
②  |  | 1.0 | 1.70 | 2.52 |
③  |  | |||
 、
、 与
与 之间的关系:
之间的关系:
(2)根据反应③判断熵变

(3)500℃下,测得反应③在某时刻时,
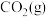 、
、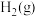 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,则此时v正
,则此时v正(4)提高反应③的反应速率且增大
 的产率,可采取的措施_______。
的产率,可采取的措施_______。| A.扩大反应容器的容积 | B.使用合适的催化剂 |
| C.缩小反应容器的容积 | D.从平衡体系中及时分离出 |
 捕获和转化可减少
捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应④完成之后,以
排放并实现资源利用,原理如图1所示。反应④完成之后,以 为载气,将恒定组成的
为载气,将恒定组成的 、
、 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
,在催化剂上有积碳。
则反应⑤的化学方程式为
A.
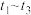 ,
, 比
比 多,且生成
多,且生成 速率不变,有可能是发生副反应
速率不变,有可能是发生副反应
B.
 时刻,副反应生成
时刻,副反应生成 的速率大于反应⑤生成
的速率大于反应⑤生成 速率
速率C.
 之后,生成
之后,生成 的速率为0,是因为反应⑤不再发生
的速率为0,是因为反应⑤不再发生
您最近一年使用:0次
5 . 已知: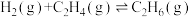
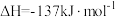 。请回答下列问题:
。请回答下列问题:
(1)该反应在_______ (填“低温”、“高温”或“任何温度”下能自发进行。
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
(3)若在10 L的密闭容器内2 mol H2(g)与a molC2H4(g)进行上述反应,测得 的平衡转化率与投料比X,
的平衡转化率与投料比X,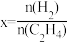 以及温度的关系如图所示。
以及温度的关系如图所示。
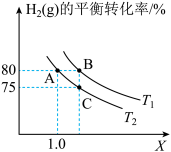
①反应从开始分别进行到A、B、C点时,_______ (填“吸收”或“放出”)的热量QA、QB、QC由大到小的顺序为_______ 。
②T1_______ (填“>”、“<”或“=”)T2。
③B点对应的体系中a=_______ 。A、B、C点对应体系的气体总压强pA、pB、pC由小到大的顺序为_______ 。
(4)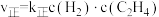 ,
,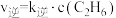 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
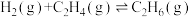
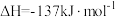 。请回答下列问题:
。请回答下列问题:(1)该反应在
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
| A.容器内混合气体的平均相对分子质量不变 | B.c正(H2)=c逆(C2H6) |
| C.容器内混合气体的压强不变 | D.容器内混合气体的密度不变 |
 的平衡转化率与投料比X,
的平衡转化率与投料比X,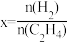 以及温度的关系如图所示。
以及温度的关系如图所示。
①反应从开始分别进行到A、B、C点时,
②T1
③B点对应的体系中a=
(4)
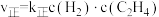 ,
,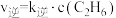 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。| A.k正增大的倍数大于k逆 | B.k正增大的倍数小于k逆 |
C.k正减小的倍数大于 | D.k正减小的倍数小于k逆 |
您最近一年使用:0次
2022-11-07更新
|
112次组卷
|
3卷引用:湖北省恩施州高中教育联盟2022-2023学年高二上学期期中考试化学试题
名校
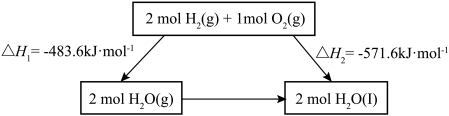
6 . 2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运的理念。已知:
下列说法不正确 的是

下列说法
| A.氢气既可以通过燃烧反应提供热能,也可以设计成燃料电池提供电能 |
B. 的过程中, 的过程中, , , |
C.断裂2mol 和1mol 和1mol 中化学键所需能量大于断裂2mol 中化学键所需能量大于断裂2mol 中化学键所需能量 中化学键所需能量 |
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关 ,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2022-11-04更新
|
620次组卷
|
9卷引用:湖北省襄阳市第五中学2022-2023学年高二下学期开学考试化学试题
7 . 汽车尾气中含有CO和NO等,可以用不同的方法净化处理,防止空气污染。回答下列问题:
(1)在汽车尾气系统中安装催化转化器可减少CO和NO的污染,其反应为2CO(g)+2NO(g) 2CO2(g)+N2(g) △H。
2CO2(g)+N2(g) △H。
①该反应在常温下能自发进行,则该反应的△H_______ 0(填“>”或“<”)。
②将CO和NO以一定流速通过两种不同的催化剂发生上述反应、相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率),结果如下图所示:
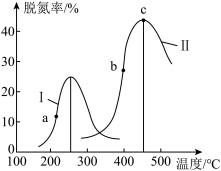
a点的v逆_______ b点的v正(填“>”“<”或“=”')。c点_______ (填“一定”或“不一定”)是平衡状态。
③对于反应2CO(g)+2NO(g) 2CO2(g)+N2(g),在实验中测得:v正= k正·c2(CO)·c2(NO)、v逆= k逆·c2(CO2)·c (N2),k正、k逆分别是正、逆反应速率常数,且只是温度的函数。
2CO2(g)+N2(g),在实验中测得:v正= k正·c2(CO)·c2(NO)、v逆= k逆·c2(CO2)·c (N2),k正、k逆分别是正、逆反应速率常数,且只是温度的函数。
T℃,将2 mol CO(g)和2 mol NO(g)通入体积为1 L的恒容密闭容器发生上述反应,反应平衡时,CO(g)的转化率为50%,则当CO(R)的转化率为25%时,v正:v逆=_______ 。
(2)二氧化铈(CeO2)在汽车尾气中CO的催化消除中有将广泛的应用,同时二氧化铈(CeO2)负载贵金属(Rh)和贵金属氧化物(Rh2O3)后催化活性的变化如下图所示。下列说法正确的是_______ (填标号)。
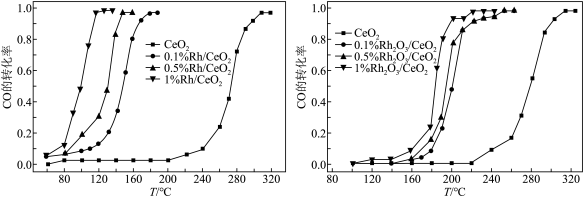
A.200℃时,复合催化剂比单一催化剂效率更高
B.在相同温度下,负载Rh2O3后催化剂的活性大于负载Rh的催化剂的活性
C.催化剂的活性随着负载Rh的增高而增大,促进了CO催化消除反应的平衡向正向移动
(3)用尿素水解生成的NH3催化还原NO,是柴油机车车辆尾气净化的主要方法。反应为4NH3(g)+O2(g)+4NO(g) 2N2(g)+6H2O(g)。实际应用中,加入尿素的量并不是越多越好,原因是
2N2(g)+6H2O(g)。实际应用中,加入尿素的量并不是越多越好,原因是__________ ,为了避免尿素过多造成的影响,可接一个氧化催化器,则氧化催化器中反应的化学方程式为_______ 。
(1)在汽车尾气系统中安装催化转化器可减少CO和NO的污染,其反应为2CO(g)+2NO(g)
 2CO2(g)+N2(g) △H。
2CO2(g)+N2(g) △H。①该反应在常温下能自发进行,则该反应的△H
②将CO和NO以一定流速通过两种不同的催化剂发生上述反应、相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率),结果如下图所示:

a点的v逆
③对于反应2CO(g)+2NO(g)
 2CO2(g)+N2(g),在实验中测得:v正= k正·c2(CO)·c2(NO)、v逆= k逆·c2(CO2)·c (N2),k正、k逆分别是正、逆反应速率常数,且只是温度的函数。
2CO2(g)+N2(g),在实验中测得:v正= k正·c2(CO)·c2(NO)、v逆= k逆·c2(CO2)·c (N2),k正、k逆分别是正、逆反应速率常数,且只是温度的函数。T℃,将2 mol CO(g)和2 mol NO(g)通入体积为1 L的恒容密闭容器发生上述反应,反应平衡时,CO(g)的转化率为50%,则当CO(R)的转化率为25%时,v正:v逆=
(2)二氧化铈(CeO2)在汽车尾气中CO的催化消除中有将广泛的应用,同时二氧化铈(CeO2)负载贵金属(Rh)和贵金属氧化物(Rh2O3)后催化活性的变化如下图所示。下列说法正确的是

A.200℃时,复合催化剂比单一催化剂效率更高
B.在相同温度下,负载Rh2O3后催化剂的活性大于负载Rh的催化剂的活性
C.催化剂的活性随着负载Rh的增高而增大,促进了CO催化消除反应的平衡向正向移动
(3)用尿素水解生成的NH3催化还原NO,是柴油机车车辆尾气净化的主要方法。反应为4NH3(g)+O2(g)+4NO(g)
 2N2(g)+6H2O(g)。实际应用中,加入尿素的量并不是越多越好,原因是
2N2(g)+6H2O(g)。实际应用中,加入尿素的量并不是越多越好,原因是
您最近一年使用:0次
8 . 工业生产中常用“古氏试砷法”检验微量砷,其反应原理如下:2AsH3(g)+12AgNO3(aq)+3H2O(1)=As2O3(s)+12HNO3(aq)+12Ag(s)。下列说法正确的是
| A.热稳定性AsH3强于NH3 | B.AsH3为平面三角形分子 |
| C.该制备反应是熵增过程 | D.实验中观察到有固体生成证明有砷元素存在 |
您最近一年使用:0次
9 . 硝酸盐是大气气溶胶中的一种重要无机组分,有文献报告气溶胶中会发生硝酸盐损耗,其反应原理为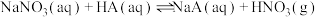 ,HA代表有机酸。若有机酸的酸性越强,则硝酸盐损耗进行的程度越大。下列说法错误的是
,HA代表有机酸。若有机酸的酸性越强,则硝酸盐损耗进行的程度越大。下列说法错误的是
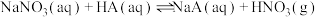 ,HA代表有机酸。若有机酸的酸性越强,则硝酸盐损耗进行的程度越大。下列说法错误的是
,HA代表有机酸。若有机酸的酸性越强,则硝酸盐损耗进行的程度越大。下列说法错误的是| A.该反应为熵增过程 |
| B.气溶胶可产生丁达尔效应 |
| C.硝酸盐损耗程度:甲酸<乙酸 |
D. 的空间结构为平面三角形 的空间结构为平面三角形 |
您最近一年使用:0次
名校
解题方法
10 . 由合成气(CO和H2)通过如下反应可制得甲醇:2H2(g)+CO(g) CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
 CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是| A.反应的ΔS>0 |
| B.当容器中气体密度不再发生变化时,反应达到平衡 |
| C.温度为400K时,反应的平衡常数K=2500 |
| D.其他条件不变,若起始时向容器中充入0.008molH2、0.004molCO和0.016molCH3OH,此时v(正)>v(逆) |
您最近一年使用:0次
2022-09-23更新
|
297次组卷
|
2卷引用:湖北省问津联合体2022-2023学年高二上学期10月质量检测化学试题



