解题方法
1 . 回答下列问题:
I.已知:①N2(g)+O2(g)=2NO(g) ΔH=+l80.5 kJ·mol-1
②C(S)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
③2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
(1)上述反应中属于放热反应的是_______ (填序号,下同),属于吸热反应的是_______ 。
(2)24 g固体碳粉完全燃烧生成CO2放出热量_______ kJ。
(3)已知NO和CO完全反应产生CO2和N2,请写出该反应的热化学方程式_______
Ⅱ.某温度时,在一个2 L的恒容密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。回答下列问题:
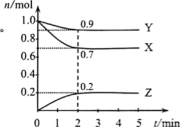
(4)化学方程式为_______ ,从反应开始到2 min,v(X)=_______ 。
(5)t为2 min时的压强是开始时压强的_______ 倍。
(6)下列说法中正确的是_______ (填选项)。
A.2v(X)=v(Z)
B.反应过程中,容器内压强先减小后不变
C.t=2 min时,X,Y的转化率相等
D.反应过程中,容器内混合气体的密度一直保持不变
I.已知:①N2(g)+O2(g)=2NO(g) ΔH=+l80.5 kJ·mol-1
②C(S)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
③2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
(1)上述反应中属于放热反应的是
(2)24 g固体碳粉完全燃烧生成CO2放出热量
(3)已知NO和CO完全反应产生CO2和N2,请写出该反应的热化学方程式
Ⅱ.某温度时,在一个2 L的恒容密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。回答下列问题:

(4)化学方程式为
(5)t为2 min时的压强是开始时压强的
(6)下列说法中正确的是
A.2v(X)=v(Z)
B.反应过程中,容器内压强先减小后不变
C.t=2 min时,X,Y的转化率相等
D.反应过程中,容器内混合气体的密度一直保持不变
您最近一年使用:0次
2 . 反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率最大的是
| A.v(A)=0.45mol/(L·min) | B.v(B)=0.6mol/(L·s) |
| C.v(C)=0.4mol/(L·s) | D.v(D)=0.45mol/(L·s) |
您最近一年使用:0次
2021-07-09更新
|
120次组卷
|
4卷引用:四川省南充市2020-2021学年高一下学期期末联考化学试题
解题方法
3 . 将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1mol/(L·min)。求:
(1)此时A的浓度c(A)=_______ mol/L
(2)前5min内用B表示的平均反应速率v(B)=_______ mol/(L·min);
(3)化学反应方程式中x的值为_______ 。
(1)此时A的浓度c(A)=
(2)前5min内用B表示的平均反应速率v(B)=
(3)化学反应方程式中x的值为
您最近一年使用:0次
4 . 氮氧化物是造成酸雨、臭氧空洞、光化学烟雾等环境问题的主要原因之一,如何消除大气污染物中氮氧化物已成为人们关注的主要问题之一。
I.NH3 -SCR法是工业上消除氮氧化物的常用方法。该法是利用氨的还原性,在一定条件下,将烟气中的NOx直接还原为N2.主要反应原理为:4NH3+4NO+O2 4N2+6H2O。
4N2+6H2O。
(1)已知有下列热化学方程式(a、b、c均大于0):
①4NH3(g) +4NO(g) + O2(g) 4N2(g)+6H2O(1) △H = —a kJ/mol
4N2(g)+6H2O(1) △H = —a kJ/mol
②N2(g)+O2(g) 2NO(g) △H = +b kJ/mol
2NO(g) △H = +b kJ/mol
③H2O(1) H2O(g) △H = +c kJ/mol
H2O(g) △H = +c kJ/mol
则氨气与氧气反应生成NO和气态水的热化学方程式为___________ 。
(2)其他条件相同,某2 L密闭容器中分别投入2 mol NH3、2 mol NO、1 mol O2,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图所示:

①甲、乙两种催化剂,催化效果较好的是___________ 。
②在催化剂甲作用下,高于210℃时,NO转化率降低的原因可能是___________ 。
Ⅱ.CH4可以消除氮氧化物的污染。主要反应原理为:CH4 (g) + 2 NO2 (g) CO2( g) + 2 H2O(g) + N2(g) △H =-868.7 kJ/mol
CO2( g) + 2 H2O(g) + N2(g) △H =-868.7 kJ/mol
(3)在3 L密闭容器中,通入0.1 mol CH4和0.2 mol NO2,在一定温度下进行上述反应,反应时间(t)与容器内CO2的物质的量(n)数据见下表:
①由表中数据,计算0~4min内:v(NO2)=___________ ,CH4的转化率为___________ 。
②该温度下的平衡常数K的值为___________ 。
Ⅲ. 研究发现,还可以采用原电池原理的方法消除氮氧化物的污染,其工作原理如图所示:

(4)该电池的正极为电极___________ (填“A”或“B”)。
(5)负极发生的电极反应式为:___________ 。
I.NH3 -SCR法是工业上消除氮氧化物的常用方法。该法是利用氨的还原性,在一定条件下,将烟气中的NOx直接还原为N2.主要反应原理为:4NH3+4NO+O2
 4N2+6H2O。
4N2+6H2O。(1)已知有下列热化学方程式(a、b、c均大于0):
①4NH3(g) +4NO(g) + O2(g)
 4N2(g)+6H2O(1) △H = —a kJ/mol
4N2(g)+6H2O(1) △H = —a kJ/mol②N2(g)+O2(g)
 2NO(g) △H = +b kJ/mol
2NO(g) △H = +b kJ/mol③H2O(1)
 H2O(g) △H = +c kJ/mol
H2O(g) △H = +c kJ/mol则氨气与氧气反应生成NO和气态水的热化学方程式为
(2)其他条件相同,某2 L密闭容器中分别投入2 mol NH3、2 mol NO、1 mol O2,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图所示:

①甲、乙两种催化剂,催化效果较好的是
②在催化剂甲作用下,高于210℃时,NO转化率降低的原因可能是
Ⅱ.CH4可以消除氮氧化物的污染。主要反应原理为:CH4 (g) + 2 NO2 (g)
 CO2( g) + 2 H2O(g) + N2(g) △H =-868.7 kJ/mol
CO2( g) + 2 H2O(g) + N2(g) △H =-868.7 kJ/mol(3)在3 L密闭容器中,通入0.1 mol CH4和0.2 mol NO2,在一定温度下进行上述反应,反应时间(t)与容器内CO2的物质的量(n)数据见下表:
| 反应时间t /min | 2 | 4 | 6 | 8 | 10 |
| CO2的物质的量n /mol | 0.04 | 0.06 | 0.07 | 0.075 | 0.075 |
①由表中数据,计算0~4min内:v(NO2)=
②该温度下的平衡常数K的值为
Ⅲ. 研究发现,还可以采用原电池原理的方法消除氮氧化物的污染,其工作原理如图所示:

(4)该电池的正极为电极
(5)负极发生的电极反应式为:
您最近一年使用:0次
名校
5 . 一定温度下,将1 mol A和2 mol B放入5 L的密闭容器中发生如下反应:A(s)+2B(g) C(g) + 2 D(g) △H<0,经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述正确的是
C(g) + 2 D(g) △H<0,经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述正确的是
 C(g) + 2 D(g) △H<0,经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述正确的是
C(g) + 2 D(g) △H<0,经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述正确的是 | A.加入少量A,反应速率加快 |
| B.在5 min内该反应用C的浓度改变量表示的反应速率为 0.02mol/(L·min) |
| C.保持体积不变,向容器充入一定量氦气,压强增大,反应速率加快 |
| D.升高温度,正反应速率减小,逆反应速率加快 |
您最近一年使用:0次
2021-05-21更新
|
870次组卷
|
10卷引用:四川省南充高级中学2020-2021学年高二下学期期中考试化学试题
四川省南充高级中学2020-2021学年高二下学期期中考试化学试题(已下线)第二章 第二节 影响化学反应速率的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)2.1.2 影响化学反应速率的因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第26练 化学反应速率-2023年高考化学一轮复习小题多维练(全国通用)山东省聊城市第二中学2022-2023学年高二上学期开学考试化学试题(已下线)第06讲 影响化学反应速率的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)黑龙江省大兴安岭呼玛县高级中学2021-2022学年高二上学期期末考试化学试题(已下线)2.3.1 化学反应速率的概念和测定-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)(已下线)2.3.3 化学反应速率综合分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)四川省内江市威远中学校2022-2023学年高二下学期期中考试化学试题
名校
解题方法
6 . 某温度下,浓度都是1mol·L-1的两种气体X2和Y2在密闭容器中反应,经过tmin后,测得物质的浓度分别为c(X2)=0.4mol·L-1、c(Y2)=0.8mol·L-1,则该反应的化学方程式可表示为
A.X2+2Y2 2XY2 2XY2 | B.2X2+Y2 2X2Y 2X2Y |
C.X2+3Y2 2XY3 2XY3 | D.3X2+Y2 2X3Y 2X3Y |
您最近一年使用:0次
2021-04-28更新
|
488次组卷
|
41卷引用:四川省南充市第一中学2021-2022学年高一下学期6月月考化学试题
四川省南充市第一中学2021-2022学年高一下学期6月月考化学试题(已下线)2010年上海市控江中学高一第二学期期末考试化学试卷(已下线)2010年江西省九江一中高二上学期第一次月考(化学)(已下线)2010-2011学年广东省中山市桂山中学高二下期中考试化学试卷(已下线)2011-2012年吉林省长春外国语学校高二上学期第一次月考化学试卷(已下线)2011-2012学年贵州省湄潭中学高二上学期期末考试化学试卷(已下线)2011-2012学年赤峰市第二实验中学高一下学期期末考试化学试卷(已下线)2011-2012学年海南省洋浦中学高二下学期期末考试化学试卷(已下线)2012-2013学年江西省赣南师院附中高二十月月考化学试卷(已下线)2012-2013学年江苏省淮安市楚州区范集中学高一下期期中考试化学卷(已下线)2012-2013学年福建省福州文博中学高一下学期期末考试化学试卷2015-2016学年山东省淄博市淄川一中高二上学期期中测试化学试卷2015-2016学年江苏省清江中学高一下期中化学试卷2015-2016学年江西省南昌市八一等五校高一5月联考化学试卷2016-2017学年山东省菏泽市高二上学期期中化学试卷江西省吉安县2016-2017学年高一下学期期中考试化学试题甘肃省嘉峪关市第一中学2016-2017学年高一下学期期末考试化学试题安徽省定远重点中学2018-2019学年高二上学期开学考试化学试题【校级联考】广东省肇庆联盟校2018-2019学年高二上学期期末考试化学试题江西省宜春市第九中学(外国语学校)2018-2019学年高一下学期期中考试化学试题江苏省沭阳县修远中学2018-2019学年高一下学期第二次月考(实验班)化学试题上海市金山中学2016-2017学年高一下学期期末考试化学试题陕西省咸阳百灵中学2019-2020学年高二上学期期中考试化学(理)试题广东省潮州市潮安区颜锡祺中学2019-2020学年高二上学期期中考试化学试题山西省晋中市平遥县第二中学2019-2020学年高二12月月考化学试题上海外国语大学附中2016-2017学年高一下学期期末考试化学试题河北省唐山市海港高级中学2019-2020学年高一下学期第五次校考化学试题河北省邯郸市肥乡区第一中学2019-2020学年高一下学期开学考试化学试题陕西省咸阳百灵学校2019-2020学年高一下学期第二次月考化学试题安徽省亳州市涡阳县第九中学2019-2020学年高一7月月考化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 章末综合检测卷安徽省定远县育才学校2020-2021学年高二上学期第一次月考化学试题安徽省安庆市宜秀区白泽湖中学2020-2021学年高二上学期第一次月考化学试题安徽省肥东县高级中学2020-2021学年高二上学期第二次月考化学试题(已下线)【浙江新东方】绍兴qw118广东省雷州市第二中学2020-2021学年高二上学期期中考试化学试题内蒙古自治区呼伦贝尔市鄂温克旗第三中学2020-2021学年高二上学期期中考试化学试题天津市耀华中学2020-2021学年高一下学期期中检测化学试题安徽省滁州市定远县育才学校2020-2021学年高一下学期期中考试化学试题福建省南安市柳城中学2020-2021学年高一下学期期中考试化学试题(已下线)第2章 化学反应速率与化学平衡(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
名校
解题方法
7 . NO2、NO、CO等是常见大气污染物,研究NO2、NO、CO等污染物的处理对建设美丽中国具有重要的意义。
(1)已知:①NO2(g)+CO(g)⇌CO2(g)+NO(g),断开1mol下列物质的所有化学键时所消耗能量分别为:
② N2(g)+
N2(g)+ O2(g)⇌NO(g)ΔH=+89.75kJ·mol-1
O2(g)⇌NO(g)ΔH=+89.75kJ·mol-1
③2NO(g)+O2(g)⇌2NO2(g)ΔH=-112.3kJ·mol-1
写出NO与CO反应生成无污染气体的热化学方程式:__ 。
(2)污染性气体NO2与CO在一定条件下的反应为2NO2(g)+4CO(g)⇌4CO2(g)+N2(g),某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1atm,5s时反应达到平衡,容器的压强变为原来的 ,则反应开始到平衡时CO的平均反应速率为ν(CO)=
,则反应开始到平衡时CO的平均反应速率为ν(CO)=_ ;若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol·L-1、0.4mol·L-1、0.1mol·L-1、1mol·L-1,要使反应向逆反应方向进行,a的取值范围为__ 。
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)ΔH<0.现在向体积为2L的恒容密闭容器(如图甲所示)中通入1molCO和2molH2:

测定不同时刻、不同温度(T/℃)下容器中CO的物质的量如下表:
请回答:
①T1__ (填“>”或“<”或“=”)T2,理由是__ 。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为___ ,该温度下的化学平衡常数为___ 。
②若将1molCO和2molH2通入原体积为2L的恒压密闭容器(如图乙所示)中,达平衡后再向容器中通入1molCH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量___ 。
(填“变大”、“变小”或“不变”)。
(1)已知:①NO2(g)+CO(g)⇌CO2(g)+NO(g),断开1mol下列物质的所有化学键时所消耗能量分别为:
| NO2 | CO | CO2 | NO |
| 812kJ | 1076kJ | 1490kJ | 632kJ |
 N2(g)+
N2(g)+ O2(g)⇌NO(g)ΔH=+89.75kJ·mol-1
O2(g)⇌NO(g)ΔH=+89.75kJ·mol-1③2NO(g)+O2(g)⇌2NO2(g)ΔH=-112.3kJ·mol-1
写出NO与CO反应生成无污染气体的热化学方程式:
(2)污染性气体NO2与CO在一定条件下的反应为2NO2(g)+4CO(g)⇌4CO2(g)+N2(g),某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1atm,5s时反应达到平衡,容器的压强变为原来的
 ,则反应开始到平衡时CO的平均反应速率为ν(CO)=
,则反应开始到平衡时CO的平均反应速率为ν(CO)=(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)ΔH<0.现在向体积为2L的恒容密闭容器(如图甲所示)中通入1molCO和2molH2:

测定不同时刻、不同温度(T/℃)下容器中CO的物质的量如下表:
| 温度 | 不同时刻容器中CO的物质的量 | ||||
| 0min | 10min | 20min | 30min | 40min | |
| T1 | 1mol | 0.8mol | 0.62mol | 0.4mol | 0.4mol |
| T2 | 1mol | 0.7mol | 0.5mol | a | a |
①T1
②若将1molCO和2molH2通入原体积为2L的恒压密闭容器(如图乙所示)中,达平衡后再向容器中通入1molCH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量
(填“变大”、“变小”或“不变”)。
您最近一年使用:0次
8 . 回答下列问题:
I.铅蓄电池是最常用的二次电池,电池总反应式为: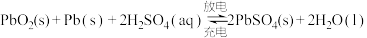
(1)放电时,铅蓄电池的负极反应式是_______ 。
(2)充电时,PbSO4(s)_______ (填序号)。
A.在阳极生成 B.在阴极生成 C.在两个电极上除去 D.在两个电极上生成
(3)用铅蓄电池作电源,以惰性电极电解浓的Na2SO4溶液制备烧碱和硫酸,装置如图所示,其中a、b为离子交换膜。
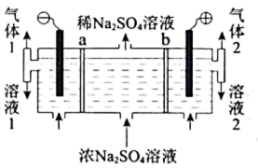
①a为_______ 离子交换膜(填“阴”或“阳”)。
②溶液1是_______ 。
③当铅蓄电池内消耗2 mol H2SO4时,理论上产生气体2的体积是_______ L(标准状况)。
II.一定温度下,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,发生反应: ,测得CO2和CH3OH的浓度随时间变化如下图。
,测得CO2和CH3OH的浓度随时间变化如下图。
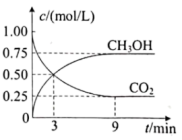
(4)反应从开始至达到平衡时,H2的平均反应速率是_______ 。
(5)平衡时CO2的转化率为_______ 。
(6)第9分钟时v逆(CH3OH)_______ (填“>”“<"或“=”)第3分钟时v正(CH3OH)。
(7)能说明上述反应达到平衡状态的是_______ (填编号)。
A.CO2与CH3OH的物质的量浓度相等
B.混合气体的密度不随时间的变化而变化
C.CO2在混合气体中的体积分数保持不变
D.单位时间内消耗3mol H2,同时生成1mol H2O
(8)为加快该反应速率,可采取的措施是_______ (填编号)。
A.恒容时充入Ne B.适当升高温度 C.增大容器的体积 D.选择高效催化剂
I.铅蓄电池是最常用的二次电池,电池总反应式为:
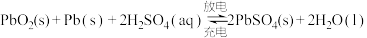
(1)放电时,铅蓄电池的负极反应式是
(2)充电时,PbSO4(s)
A.在阳极生成 B.在阴极生成 C.在两个电极上除去 D.在两个电极上生成
(3)用铅蓄电池作电源,以惰性电极电解浓的Na2SO4溶液制备烧碱和硫酸,装置如图所示,其中a、b为离子交换膜。

①a为
②溶液1是
③当铅蓄电池内消耗2 mol H2SO4时,理论上产生气体2的体积是
II.一定温度下,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,发生反应:
 ,测得CO2和CH3OH的浓度随时间变化如下图。
,测得CO2和CH3OH的浓度随时间变化如下图。
(4)反应从开始至达到平衡时,H2的平均反应速率是
(5)平衡时CO2的转化率为
(6)第9分钟时v逆(CH3OH)
(7)能说明上述反应达到平衡状态的是
A.CO2与CH3OH的物质的量浓度相等
B.混合气体的密度不随时间的变化而变化
C.CO2在混合气体中的体积分数保持不变
D.单位时间内消耗3mol H2,同时生成1mol H2O
(8)为加快该反应速率,可采取的措施是
A.恒容时充入Ne B.适当升高温度 C.增大容器的体积 D.选择高效催化剂
您最近一年使用:0次
名校
9 . (1)某温度时,在2L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:
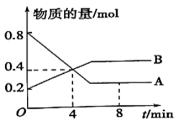
①该反应的化学方程式为___________ ;
②反应开始至4min时,B的平均反应速率为___________ ,A的转化率为___________ 。
③4min时,反应是否达到平衡状态?___________ (填“是”或“否”),8min时,v(正)___________ v(逆)(填“>”、“<”或“=”)。
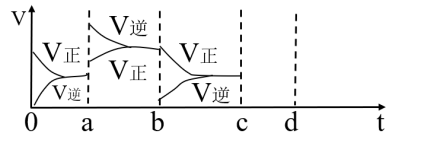
(2)下图表示在密闭容器中反应:2SO2(g)+O2(g) 2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时刻改变的条件可能是
2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时刻改变的条件可能是___________ ;b时改变的条件可能是___________ 。

①该反应的化学方程式为
②反应开始至4min时,B的平均反应速率为
③4min时,反应是否达到平衡状态?
(2)下图表示在密闭容器中反应:2SO2(g)+O2(g)
 2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时刻改变的条件可能是
2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时刻改变的条件可能是
您最近一年使用:0次
2020-12-06更新
|
169次组卷
|
3卷引用:四川省阆中东风中学校2020-2021学年高二上学期第三学月调研监测化学试题
名校
解题方法
10 . 以煤为原料可合成一系列燃料。
(1)已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
请写出甲醇燃烧生成H2O(g)的热化学方程式_________ ;
(2)向1 L密闭容器中加入2 mol CO、4 mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g) CH3OCH3(l)+H2O(l) ΔH=+71 kJ/mol
CH3OCH3(l)+H2O(l) ΔH=+71 kJ/mol
①该反应能否_________ 自发进行(填“能”、“不能”或“无法判断”)。
②下列叙述能说明此反应达到平衡状态的是_________ 。
a.混合气体的平均相对分子质量保持不变 b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变 d.混合气体的密度保持不变
e.1 mol CO生成的同时有1 mol O-H键断裂
(3)CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:
①0~10 min内,用H2O(g)表示的化学反应速率v(H2O)=_________ mol/(L·min)
②达到平衡时,该反应的平衡常数K=_________ (用分数表示)
③在其它条件不变的情况下,若30 min时改变温度为T2℃,此时H2的物质的量为3.2 mol,则T1_________ T2(填“>”、“<”或“=”),理由是_________ 。在其它条件不变的情况下,若30 min时向容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡_________ 移动(填“正向”、“逆向”或“不”)。
(1)已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
请写出甲醇燃烧生成H2O(g)的热化学方程式
(2)向1 L密闭容器中加入2 mol CO、4 mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g)
 CH3OCH3(l)+H2O(l) ΔH=+71 kJ/mol
CH3OCH3(l)+H2O(l) ΔH=+71 kJ/mol①该反应能否
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变 b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变 d.混合气体的密度保持不变
e.1 mol CO生成的同时有1 mol O-H键断裂
(3)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:| 反应条件 | 反应时间(min) | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 恒温恒容(T1℃、2 L) | 0 | 2 | 6 | 0 | 0 |
| 10 | 4.5 | ||||
| 20 | 1 | ||||
| 30 | 1 |
②达到平衡时,该反应的平衡常数K=
③在其它条件不变的情况下,若30 min时改变温度为T2℃,此时H2的物质的量为3.2 mol,则T1
您最近一年使用:0次



