名校
1 . 一定温度下,在一个 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: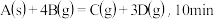 末,
末, 的物质的量减少
的物质的量减少 ,下列有关该反应的表述中正确的是
,下列有关该反应的表述中正确的是
 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: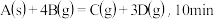 末,
末, 的物质的量减少
的物质的量减少 ,下列有关该反应的表述中正确的是
,下列有关该反应的表述中正确的是A.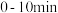 内,用 内,用 表示的平均反应速率是 表示的平均反应速率是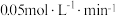 |
B.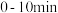 内,用 内,用 表示的平均反应速率是 表示的平均反应速率是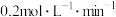 |
| C.反应速率:4V(B)=3V(D) |
| D.随着反应的进行,容器内气体压强始终保持不变 |
您最近一年使用:0次
2022-05-19更新
|
223次组卷
|
2卷引用:四川省南充市白塔中学2021-2022学年高一下学期第四次月考化学试题
名校
解题方法
2 . 在 个不同的容器中,不同的条件下进行合成氨反应。其中合成氨速率最快的是
个不同的容器中,不同的条件下进行合成氨反应。其中合成氨速率最快的是
 个不同的容器中,不同的条件下进行合成氨反应。其中合成氨速率最快的是
个不同的容器中,不同的条件下进行合成氨反应。其中合成氨速率最快的是A. | B.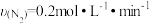 |
C. | D.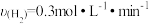 |
您最近一年使用:0次
2022-05-19更新
|
69次组卷
|
2卷引用:四川省南充市白塔中学2021-2022学年高一下学期第四次月考化学试题
名校
解题方法
3 . 在一定条件下,将3mol A和1mol B两种气体混合于容积为2L的恒容密闭容器中,发生如下反应: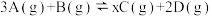 。2min末该反应达到平衡,测得生成0.4mol C和0.8mol D,下列判断不正确的是
。2min末该反应达到平衡,测得生成0.4mol C和0.8mol D,下列判断不正确的是
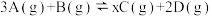 。2min末该反应达到平衡,测得生成0.4mol C和0.8mol D,下列判断不正确的是
。2min末该反应达到平衡,测得生成0.4mol C和0.8mol D,下列判断不正确的是A. |
| B.B的转化率为60% |
C.2min内A的平均反应速率为 |
D.2min时,A的浓度为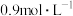 |
您最近一年使用:0次
2022-04-23更新
|
276次组卷
|
35卷引用:四川省西充中学 2021-2022 学年高二上学期期中考试化学试题
四川省西充中学 2021-2022 学年高二上学期期中考试化学试题北京市101中学2016-2017学年高一下学期期中考试化学试题黑龙江省大庆实验中学2016-2017学年高一6月月考化学试题湖南省衡阳市第八中学2016-2017学年高一下学期五科联赛(6月)理综化学试题吉林省辽源市第五中学2016-2017学年高二下学期期末考试化学试题【全国百强校】北京101中学2017-2018学年高一下学期期中考试化学试题山西省长治市沁县中学2018-2019学年高一下学期期中考试化学试题河南省周口扶沟县高级中学2018-2019学年高一下学期第二次月考化学试题黑龙江省大庆实验中学2018-2019学年高一下学期6月月考化学试题黑龙江省双鸭山市第一中学2018-2019学年高一下学期期末考试化学试题吉林省实验中学2019-2020学年高二上学期第一次月考化学试题四川省眉山市彭山区第一中学2019-2020学年高二上学期开学考试化学试题黑龙江省哈尔滨市双城区兆麟中学2019-2020学年度高一下学期期中考试化学试题黑龙江省大庆市肇州县第二中学2019-2020学年高一下学期期末考试化学试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第3节 化学反应的速率 课时1 化学反应速率高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第一节 化学反应速率 课时1 化学反应速率高一必修第二册(人教2019版)第六章 第二节 化学反应的速率与限度 综合训练(已下线)【全国百强校】黑龙江省大庆实验中学2018-2019学年高一6月月考试化学试题新疆吾尔自治区石河子第二中学2020-2021学年高二上学期第一次月考化学试题贵州省思南中学2020-2021学年高二上学期期中考试化学试题新疆新源县第二中学2019-2020学年高一下学期期末考试化学试题江苏省淮安市金湖、洪泽等六校2020-2021学年高一下学期联考期中考试(第六次学情调查)化学试题(已下线)专题06 化学反应速率和限度【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)甘肃省静宁县第一中学2020-2021学年高一下学期第三次月考化学(实验班)试题吉林省辽源市友好学校2020-2021学年高一下学期期末联考化学试题黑龙江省双鸭山市第一中学2019-2020学年高一下学期期末考试化学试卷湖北省十堰市2016-2017学年高一下学期期末调研考试化学试题江苏省盐城市伍佑中学2021-2022学年高一下学期学情调研(一)化学试题重庆市名校联盟2021-2022学年高一下学期第一次联合考试化学试题陕西省西安中学2021-2022学年高一下学期期中考试化学试题陕西省西安中学2021-2022学年高一下学期期中考试化学试题新疆呼图壁县第一中学2021-2022学年高二上学期期中考试化学试题浙江省金华市江南中学2021-2022学年高二上学期期中考试化学试题云南省昆明市第八中学2023-2024学年高二上学期特色部开学考化学试题江西省新余市第一中学2023-2024学年高二上学期开学考试化学试题
名校
4 . 某密闭容器(未特殊说明均为恒体积)中,某气相化学反应2A(g)⇌B(g)+D(g)在4种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如表:

根据上述数据,完成下列填空:
(1)在实验1,反应在10至30分钟时间内,A的平均反应速率为_______ mol·(L/min)。
(2)设实验1的反应速率为v1,实验2的反应速率为v2,则v2_______ v1(填“>”“=”“<”),并推测实验2隐含的条件是_______ 。
(3)设实验3在恒压条件中进行,其反应速率为v3,若向其中充入He(不参与反应),v3_______ (填“增大”“不变”“减小”),理由是_______ 。
(4)比较实验4和实验1可知v4>v1,原因是①_______ ,②_______ 。

根据上述数据,完成下列填空:
(1)在实验1,反应在10至30分钟时间内,A的平均反应速率为
(2)设实验1的反应速率为v1,实验2的反应速率为v2,则v2
(3)设实验3在恒压条件中进行,其反应速率为v3,若向其中充入He(不参与反应),v3
(4)比较实验4和实验1可知v4>v1,原因是①
您最近一年使用:0次
2022-04-12更新
|
142次组卷
|
2卷引用:四川省南充高级中学2020-2021学年高一下学期第二次月考化学试题
名校
5 . 按要求回答问题:
(1)以Fe和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①SO 向
向_______ 极移动(填“正”或“负”)。
②电子流动方向由_______ 极流向_______ 极(填“正”或“负”)。
③若有1mole-流过导线,则理论上正极析出标准状态下的气体_______ L。
④若将稀硫酸换成浓硝酸,一段时间后,正极电极方程式为_______ 。
(2)丙烷(C3H8)燃料电池是一种高效无污染的清洁电池,它用KOH做电解质。则负极反应方程式是_______ 。
(3)一定温度下,在容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
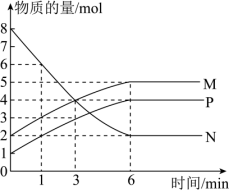
①反应化学方程式中各物质的系数比为a︰b︰c=_______ 。
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为_______ 。
(1)以Fe和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①SO
 向
向②电子流动方向由
③若有1mole-流过导线,则理论上正极析出标准状态下的气体
④若将稀硫酸换成浓硝酸,一段时间后,正极电极方程式为
(2)丙烷(C3H8)燃料电池是一种高效无污染的清洁电池,它用KOH做电解质。则负极反应方程式是
(3)一定温度下,在容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a︰b︰c=
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为
您最近一年使用:0次
名校
6 . 在某恒容密闭容器中发生反应 N2+3H2⇌2NH3 经过一段时间后,NH3 的浓度增加了0.4mol·L-1,该段时间内用 H2 表示的反应速率为 0.65 mol·L-1·s-1 则反应所经过的时间是
| A.0.44 s | B.0.92 s | C.1.33 s | D.2 s |
您最近一年使用:0次
2022-04-12更新
|
122次组卷
|
2卷引用:四川省南充高级中学2020-2021学年高一下学期第二次月考化学试题
名校
7 . 在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系3v(A)=2v(B),2v(A)=3v(C),则此反应可以表示为
| A.2A+3B=2C | B.A+3B=2C | C.6A+9B=4C | D.3A+B=2C |
您最近一年使用:0次
名校
8 . 煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中SO2的含量,已成为我国解决环境问题的主导技术之一。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
①2CaO(s)+2SO2(g)+O2(g)⇌2CaSO4(s) ∆H1=−1004.0kJ/mol
②CaSO4(s)+CO(g)⇌CaO(s)+SO2(g)+CO2(g) ∆H2=+219.0kJ/mol
(1)表示CO燃烧热的热化学方程式是___________ 。
(2)结合上述反应,从物质用量考虑,在煤燃烧过程中要提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),可采用的最适宜方法是___________ 。
(3)某温度下,在一个恒容密闭容器中加入CaSO4(s)和CO(g),若只发生反应②,测得如下数据:
0~20min内v(SO2)=___________ ,此条件下该反应的平衡常数为___________ mol·L−1。
(4)实际生产中常用石灰石代替生石灰,石灰石吸收热量分解为生石灰,即CaCO3(s)⇌CaO(s)+CO2(g) ∆H>0。800℃下,在一个密闭容器中加入一定量的CaCO3(s)进行该反应,CO2气体的浓度变化如下图所示,t1和与t2时分别改变一个条件,则改变的条件依次是________ 和________ 。

II.除去燃煤产生的废气中的SO2的过程如图所示。

(5)过程①是SO2的部分催化氧化反应,若参加反应的SO2和O2的体积比为4∶3,则反应①的化学方程式为___________ 。
(6)已知:NO2(g)+SO2(g)⇌NO(g)+SO3(g) ∆H<0。向密闭容器中充入等体积的NO2和SO2,测得平衡状态时压强对数lgp(NO2)和lgp(SO3)的关系如图所示。

则T1___________ T2(填“>”、“<”或“=”)。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
①2CaO(s)+2SO2(g)+O2(g)⇌2CaSO4(s) ∆H1=−1004.0kJ/mol
②CaSO4(s)+CO(g)⇌CaO(s)+SO2(g)+CO2(g) ∆H2=+219.0kJ/mol
(1)表示CO燃烧热的热化学方程式是
(2)结合上述反应,从物质用量考虑,在煤燃烧过程中要提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),可采用的最适宜方法是
(3)某温度下,在一个恒容密闭容器中加入CaSO4(s)和CO(g),若只发生反应②,测得如下数据:
| t/min | 0 | 10 | 20 | 30 | 40 |
| c(CO)/(mol·L−1) | 2 | 1.5 | 1.1 | 0.8 | 0.8 |
0~20min内v(SO2)=
(4)实际生产中常用石灰石代替生石灰,石灰石吸收热量分解为生石灰,即CaCO3(s)⇌CaO(s)+CO2(g) ∆H>0。800℃下,在一个密闭容器中加入一定量的CaCO3(s)进行该反应,CO2气体的浓度变化如下图所示,t1和与t2时分别改变一个条件,则改变的条件依次是

II.除去燃煤产生的废气中的SO2的过程如图所示。

(5)过程①是SO2的部分催化氧化反应,若参加反应的SO2和O2的体积比为4∶3,则反应①的化学方程式为
(6)已知:NO2(g)+SO2(g)⇌NO(g)+SO3(g) ∆H<0。向密闭容器中充入等体积的NO2和SO2,测得平衡状态时压强对数lgp(NO2)和lgp(SO3)的关系如图所示。

则T1
您最近一年使用:0次
2022-03-22更新
|
202次组卷
|
2卷引用:四川省南充高级中学2021-2022学年高三上学期第四次月考理综化学试题
名校
解题方法
9 . 草酸(H2C2O4)是一种重要的有机化工原料。为探究草酸的制取和性质,进行如下实验。
实验Ⅰ:探究草酸的制备
实验室用硝酸氧化淀粉水解液制草酸:C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O。装置如图所示:

(1)上图实验装置中仪器乙的名称为:_______ ,B装置的作用_______ 。
(2)检验淀粉是否完全水解所需要的试剂为:_______ 。
实验Ⅱ:探究草酸的不稳定性
已知:草酸晶体(H2C2O4·2H2O,M=126g/mol)无色,易溶于水,熔点为101℃,受热易脱水、升华,170℃以上分解产生H2O、CO和CO2。草酸的酸性比碳酸强,其钙盐难溶于水。

(3)请选取以上的装置证明草酸晶体分解的产物(可重复使用,加热装置和连接装置已略去)。仪器装置连接顺序为:C→_______ →_______ →_______ →_______ →D→A→F→E
(4)若实验结束后测得A管后面的F装置质量增加4.4g,则至少需分解草酸晶体的质量为_______ g。
实验Ⅲ:探究草酸与酸性高锰酸钾的反应
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快。为探究其原因,同学们做了如下对比实验;
写出高锰酸钾在酸性条件下氧化草酸的离子反应方程式:_______ 。由此你认为溶液褪色总是先慢后快的原因是_______ ,试求实验1中用KMnO4表示的平均化学反应速率为_______ (结果保留一位小数)。
实验Ⅰ:探究草酸的制备
实验室用硝酸氧化淀粉水解液制草酸:C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O。装置如图所示:

(1)上图实验装置中仪器乙的名称为:
(2)检验淀粉是否完全水解所需要的试剂为:
实验Ⅱ:探究草酸的不稳定性
已知:草酸晶体(H2C2O4·2H2O,M=126g/mol)无色,易溶于水,熔点为101℃,受热易脱水、升华,170℃以上分解产生H2O、CO和CO2。草酸的酸性比碳酸强,其钙盐难溶于水。

(3)请选取以上的装置证明草酸晶体分解的产物(可重复使用,加热装置和连接装置已略去)。仪器装置连接顺序为:C→
(4)若实验结束后测得A管后面的F装置质量增加4.4g,则至少需分解草酸晶体的质量为
实验Ⅲ:探究草酸与酸性高锰酸钾的反应
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快。为探究其原因,同学们做了如下对比实验;
| 实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(S) | 褪色时间(s) | ||
| c(mol·L-1) | V(mL) | c(mol·L-1) | V(mL) | |||
实验1 | 0.1 | 2 | 0.01 | 4 | 0 | 30 |
实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
您最近一年使用:0次
名校
解题方法
10 . 运用所学知识,回答下列问题:
(1)某温度下,在2L恒容密闭容器中充入一定量A,发生反应aA(g)⇌B(g)+cC(g)。反应达平衡时,测得c(B)=0.2mol·L-1,A、C的物质的量浓度随时间的变化如下图所示:
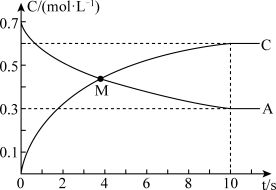
①a=_____ ,M点时,v正_____ v逆(填“>”“<”或“=”),10秒内用C表示的反应速率为_____ 。
②反应开始与达平衡时容器内的压强之比为______ 。
③可加快该反应速率的措施有_______ 。
A.增大容器的体积 B.恒容时充入Ne
C.适当升高温度 D.恒压时充入Ne
(2)某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。
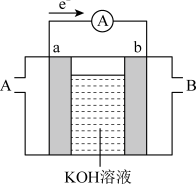
①空气从_____ (填“A”或“B”)口通入,溶液中OH-移向______ 极(填“a”或“b”)。
②若使用的燃料是甲烷,则负极的电极反应式为______ 。
(1)某温度下,在2L恒容密闭容器中充入一定量A,发生反应aA(g)⇌B(g)+cC(g)。反应达平衡时,测得c(B)=0.2mol·L-1,A、C的物质的量浓度随时间的变化如下图所示:

①a=
②反应开始与达平衡时容器内的压强之比为
③可加快该反应速率的措施有
A.增大容器的体积 B.恒容时充入Ne
C.适当升高温度 D.恒压时充入Ne
(2)某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。

①空气从
②若使用的燃料是甲烷,则负极的电极反应式为
您最近一年使用:0次
2022-03-09更新
|
321次组卷
|
2卷引用:四川省南充高级中学2021-2022学年高二上学期入学考试化学试题



