1 . 二氧化硫的催化氧化反应: 是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是
是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是
 是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是
是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是A.加入合适催化剂可以提高 的平衡产率 的平衡产率 |
| B.缩小容器容积可以增大活化分子百分含量 |
C.扩大容器容积可以提高 的平衡产率 的平衡产率 |
| D.缩小容器容积可以增大反应速率 |
您最近一年使用:0次
2 .  是重要的化工原料,可利用乙烯制备乙醇:
是重要的化工原料,可利用乙烯制备乙醇: 。向
。向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,测得
,测得 的平衡转化率与
的平衡转化率与 的关系如图所示,已知分压
的关系如图所示,已知分压 总压
总压 气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数(
气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数( ),下列说法错误的是
),下列说法错误的是

 是重要的化工原料,可利用乙烯制备乙醇:
是重要的化工原料,可利用乙烯制备乙醇: 。向
。向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,测得
,测得 的平衡转化率与
的平衡转化率与 的关系如图所示,已知分压
的关系如图所示,已知分压 总压
总压 气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数(
气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数( ),下列说法错误的是
),下列说法错误的是
| A.该反应为放热反应 |
| B.合适的催化剂能提高该反应的平衡转化率 |
C.若 点的压强为 点的压强为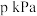 ,则该温度下的 ,则该温度下的 |
D.若反应从开始到b点用时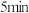 ,则 ,则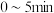 内, 内, |
您最近一年使用:0次
2022-12-15更新
|
370次组卷
|
3卷引用:河北省名校联考2022-2023学年高二上学期12月联考化学试题
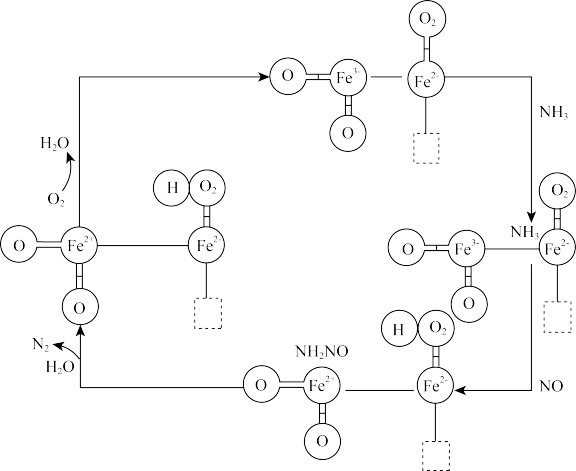
3 . 某科研团队利用缺陷工程(贫氧环境焙烧)制备了含有大量氧缺陷和表面羟基的 ,该
,该 参与如图所示的
参与如图所示的 还原。下列说法正确的是
还原。下列说法正确的是
 ,该
,该 参与如图所示的
参与如图所示的 还原。下列说法正确的是
还原。下列说法正确的是
A. 为该过程的氧化剂 为该过程的氧化剂 |
B.图中总反应可能为 |
| C.整个流程中含铁元素的物质中铁的化合价均相同 |
| D.该催化合成时,溶液的pH越小越好 |
您最近一年使用:0次
2022-12-11更新
|
236次组卷
|
5卷引用:河北省唐山市部分学校2022-2023学年高三上学期12月月考化学试题
河北省唐山市部分学校2022-2023学年高三上学期12月月考化学试题广东省江门市2022-2023学年高三上学期联考化学试题重庆市好教育联盟2023届高三12月调研考试化学试题吉林省部分学校2022-2023学年高三上学期12月联考化学试题(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题6-10)
4 . 课外实验小组以KI参与的某些反应来对反应过程和化学反应原理进行探究。
(1)KI中的 促进
促进 分解的反应机理如下
分解的反应机理如下
① (慢)
(慢)
② (快)
(快)
则此过程的决速步骤为______ (填序号),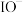 在此过程中的作用是
在此过程中的作用是____________ 。
(2)KI中的 在经酸化的溶液中易被空气氧化:
在经酸化的溶液中易被空气氧化:
实验小组探究外界条件对反应速率的影响,部分实验数据如下表。
①为确保A组实验在39℃下进行,应采用的控温方法为______ 。
②B组实验中V=______ ,C组是探究______ 对反应速率的影响,t的取值范围为______ 。
(3)若将C组实验反应后溶液充分放置一段时间,检验其吸收 的体积,可用
的体积,可用 标准溶液滴定吸收液(
标准溶液滴定吸收液( ),实验时应将
),实验时应将 标准溶液放在
标准溶液放在______ 滴定管中,滴定终点时实验现象为______ ,若消耗0.2mol/L 标准溶液为15.00mL,则吸收氧气在标准状况下的体积为
标准溶液为15.00mL,则吸收氧气在标准状况下的体积为______ 。
(1)KI中的
 促进
促进 分解的反应机理如下
分解的反应机理如下①
 (慢)
(慢)②
 (快)
(快)则此过程的决速步骤为
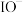 在此过程中的作用是
在此过程中的作用是(2)KI中的
 在经酸化的溶液中易被空气氧化:
在经酸化的溶液中易被空气氧化:
实验小组探究外界条件对反应速率的影响,部分实验数据如下表。
编号 | 温度/℃ |  硫酸体积/mL 硫酸体积/mL |  KI溶液体积/mL KI溶液体积/mL |  体积/mL 体积/mL | 淀粉溶液体积/mL | 出现蓝色的时间/s |
| A | 39 | 10.0 | 5.0 | 5.0 | 1.0 | 5 |
| B | 5 | 10.0 | 5.0 | V | 1.0 | 39 |
| C | 39 | 15.0 | 5.0 | 0.0 | 1.0 | t |
②B组实验中V=
(3)若将C组实验反应后溶液充分放置一段时间,检验其吸收
 的体积,可用
的体积,可用 标准溶液滴定吸收液(
标准溶液滴定吸收液( ),实验时应将
),实验时应将 标准溶液放在
标准溶液放在 标准溶液为15.00mL,则吸收氧气在标准状况下的体积为
标准溶液为15.00mL,则吸收氧气在标准状况下的体积为
您最近一年使用:0次
2022-11-24更新
|
305次组卷
|
4卷引用:河北省部分学校2022-2023学年高三上学期11月联考化学试题
名校
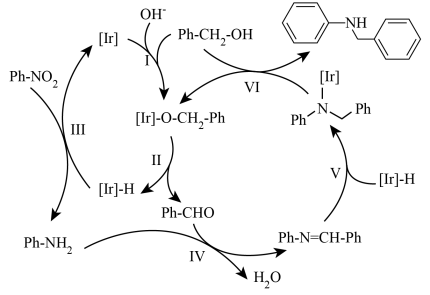
5 . 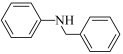 可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表
可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表 )下列说法
)下列说法不正确 的是
 可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表
可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表 )下列说法
)下列说法
| A.反应I过程中有水生成 |
| B.反应IV涉及加成反应和消去反应 |
| C.该过程反应原料为硝基苯和苯甲醇 |
D.用CH3CH2CH2OH替代上述过程中的同类物质参与反应,可以合成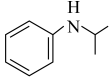 |
您最近一年使用:0次
2022-11-12更新
|
1736次组卷
|
9卷引用:河北省邯郸市第一中学2022-2023学年高三上学期一轮复习(四)化学试题
河北省邯郸市第一中学2022-2023学年高三上学期一轮复习(四)化学试题浙江省宁波市2022-2023学年高三上学期选考模拟考试化学试题(已下线)热点情景汇编-专题五 简单有机物中的化学(已下线)化学(浙江B卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)专题12 化学反应机理(测)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)【知识图鉴】单元讲练测选择性必修3第3单元03巩固练(已下线)仿真卷04-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)江西省赣州市兴国平川中学2022-2023学年高二下学期4月期中考试化学试题
6 . 已知 的能昼变化与反应进程的关系如图所示:
的能昼变化与反应进程的关系如图所示:
 的能昼变化与反应进程的关系如图所示:
的能昼变化与反应进程的关系如图所示:
A. (I) (I) (II) (II) (III) (III) | B.平衡时 的转化率: 的转化率: |
C.生成 的速率:III 的速率:III II II | D.X、Y分别参与了进程II、III的反应 |
您最近一年使用:0次
7 . 乙烯是一种重要的有机化工原料,广泛用于生产聚乙烯和氯乙烯。工业上利用乙烷为原料,通过如下反应Ⅰ或反应Ⅱ制得乙烯。回答下列问题:
反应Ⅰ:乙烷直接脱氢的原理:C2H6(g) C2H4(g)+H2(g) △H1
C2H4(g)+H2(g) △H1
(1)已知C2H6、C2H4、H2的燃烧热△H分别为-1560 kJ/mol、-1411 kJ/mol和-286 kJ/mol,则乙烯脱氢的反应△H1为_______ kJ/mol。
(2)科技工作者结合实验与计算机模拟结果,研究了乙烷在催化剂表面脱氢制乙烯的反应,其部分历程如下图1所示(吸附在催化剂表面的物种用*标注,TS表示过渡态):
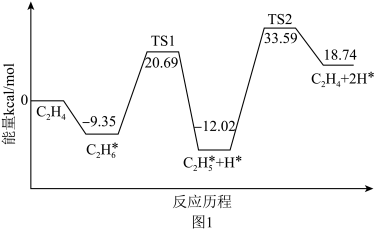
此部分历程中最大的活化能Ea=_______ kJ/mol,该步骤的反应方程式为_______ 。
(3)在压强恒为p的条件下,n(N2):n(C2H6)分别为a、b、c时,乙烷的平衡转化率与温度变化的关系如图2所示,则a、b、c的大小关系为_______ ;当n(N2):n(C2H6)=1,温度为973 K时,乙烷的转化率为50%,则反应的Kp=_______ 。
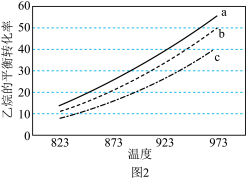
反应Ⅱ:CO2氧化乙烷制脱氢的原理C2H6(g)+CO2(g) C2H4(g)+CO(g)+H2O(g)
C2H4(g)+CO(g)+H2O(g)
(4)有研究表明CrO3催化CO2氧化乙烷制乙烯的机理可分为两步,其中第一步反应为3C2H6+2CrO3 3C2H4+Cr2O3+3H2O,则第二步反应为
3C2H4+Cr2O3+3H2O,则第二步反应为_______ 。
(5)已知CO2氧化乙烷脱氢容易发生副反应:C2H6(g)+2CO2(g) 4CO(g)+3H2O(g),当n(CO2):n(C2H6)=1:1投料,在923 K和保持总压恒定的条件下,研究催化剂X对“CO2氧化C2H6制C2H4”的影响,所得实验数据如下表:
4CO(g)+3H2O(g),当n(CO2):n(C2H6)=1:1投料,在923 K和保持总压恒定的条件下,研究催化剂X对“CO2氧化C2H6制C2H4”的影响,所得实验数据如下表:
结合具体反应分析,在催化剂X作用下,CO2氧化C2H6的主要产物是_______ 。若想提高C2H4的产率,应当_______ 。
反应Ⅰ:乙烷直接脱氢的原理:C2H6(g)
 C2H4(g)+H2(g) △H1
C2H4(g)+H2(g) △H1(1)已知C2H6、C2H4、H2的燃烧热△H分别为-1560 kJ/mol、-1411 kJ/mol和-286 kJ/mol,则乙烯脱氢的反应△H1为
(2)科技工作者结合实验与计算机模拟结果,研究了乙烷在催化剂表面脱氢制乙烯的反应,其部分历程如下图1所示(吸附在催化剂表面的物种用*标注,TS表示过渡态):

此部分历程中最大的活化能Ea=
(3)在压强恒为p的条件下,n(N2):n(C2H6)分别为a、b、c时,乙烷的平衡转化率与温度变化的关系如图2所示,则a、b、c的大小关系为

反应Ⅱ:CO2氧化乙烷制脱氢的原理C2H6(g)+CO2(g)
 C2H4(g)+CO(g)+H2O(g)
C2H4(g)+CO(g)+H2O(g)(4)有研究表明CrO3催化CO2氧化乙烷制乙烯的机理可分为两步,其中第一步反应为3C2H6+2CrO3
 3C2H4+Cr2O3+3H2O,则第二步反应为
3C2H4+Cr2O3+3H2O,则第二步反应为(5)已知CO2氧化乙烷脱氢容易发生副反应:C2H6(g)+2CO2(g)
 4CO(g)+3H2O(g),当n(CO2):n(C2H6)=1:1投料,在923 K和保持总压恒定的条件下,研究催化剂X对“CO2氧化C2H6制C2H4”的影响,所得实验数据如下表:
4CO(g)+3H2O(g),当n(CO2):n(C2H6)=1:1投料,在923 K和保持总压恒定的条件下,研究催化剂X对“CO2氧化C2H6制C2H4”的影响,所得实验数据如下表:| 催化剂 | C2H6的转化率 | CO2的转化率 | C2H4的转化率 |
| X | 19.0% | 37.6% | 3.3% |
您最近一年使用:0次
2022-10-20更新
|
245次组卷
|
2卷引用:河北昌黎第一中学2024届高三第六次调研考试化学试卷
解题方法
8 . 某小组探究Cu与硝酸的反应,过程如下图所示:
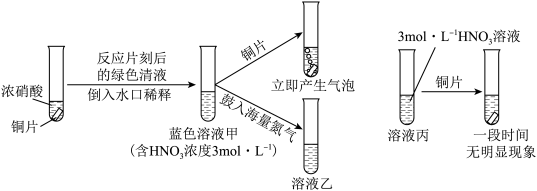
下列说法错误的是

下列说法错误的是
A.向溶液丙中加入少量硝酸铜,溶液呈浅蓝色,放入铜片,没有明显变化,说明 对该反应没有催化作用 对该反应没有催化作用 |
B.向放有铜片的溶液丙中通入足量 ,铜片表面立即产生气泡,说明 ,铜片表面立即产生气泡,说明 对该反应有催化作用 对该反应有催化作用 |
C.相同条件下,铜片与甲、乙、丙溶液的反应速率:v(甲)>v(乙)>v(丙),说明 对该反应有催化作用 对该反应有催化作用 |
D.向含有铜片的丙溶液中加入少量的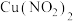 ,铜片上立即生成气泡,说明 ,铜片上立即生成气泡,说明 对该反应有催化作用 对该反应有催化作用 |
您最近一年使用:0次
2022-10-13更新
|
180次组卷
|
2卷引用:河北衡水市部分中学2022-2023学年高三上学期10月考试化学试题
名校
解题方法
9 . 如图表示使用不同催化剂(AuF和AuPF )催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是
)催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是

 )催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是
)催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是
| A.乙烯催化加氢是放热反应 |
| B.稳定性:过渡态1<过渡态2<乙烷 |
| C.催化剂不同,反应路径不同 |
| D.总能量:断键吸收>成键释放 |
您最近一年使用:0次
2022-10-12更新
|
486次组卷
|
9卷引用:河北省故城县高级中学2022-2023学年高二上学期第一次月考化学试题
河北省故城县高级中学2022-2023学年高二上学期第一次月考化学试题湖北省宜昌市协作体2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期第三次验收考试化学试题河南省鹤壁市高中2022-2023学年高二下学期第一次段考化学试题辽宁省朝阳市建平县实验中学2022-2023学年高一下学期7月期末化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期11月期中考试化学试题江西省赣州市兴国中学等六校2022-2023学年高三上学期12月月考化学试题江西省部分学校2023-2024学年高二上学期10月月考化学试题浙江省金华市东阳市外国语学校2023-2024学年高二上学期10月月考化学试题
名校
10 . 催化还原CO2是解决温室效应及能源问题的重要手段之一,研究表明CO2和H2可发生如下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H。向1L某刚性容器中通入1molCO2和3molH2,在相同时间内不同催化剂作用下CO2的转化率(催化剂A作用下CO2的转化率为A%,催化剂B作用下CO2的转化率为B%)与温度的关系如表所示:
CH3OH(g)+H2O(g) △H。向1L某刚性容器中通入1molCO2和3molH2,在相同时间内不同催化剂作用下CO2的转化率(催化剂A作用下CO2的转化率为A%,催化剂B作用下CO2的转化率为B%)与温度的关系如表所示:
回答下面问题:
(1)在CO2(g)+3H2(g) CH3OH(g)+H2O(g)反应中△S
CH3OH(g)+H2O(g)反应中△S____ 0(填“大于”“小于”“等于”或“不能确定”,下同),△H____ 0。
(2)温度在50℃以后,反应是否达到化学平衡状态?____ (填“是”或“否”)。温度在40℃以前,CO2的转化率随温度上升而增大的原因是____ 。
(3)在50℃时,CO2(g)+3H2(g) CH3OH(g)+H2O(g)的平衡常数K=
CH3OH(g)+H2O(g)的平衡常数K=____ (保留两位小数)。若向50℃、1L某刚性容器中通入1molCO2、3molH2、1molCH3OH(g)和1molH2O(g),此时v(正)____ v(逆)(填“大于”“小于”“等于”或“不能确定”)。
(4)图为反应在无催化剂、催化剂A和催化剂B的三种情况下“反应过程~能量”的示意图:

在图上标注“无催化剂”、“催化剂A”和“催化剂B”____ 。
(5)在相同条件下,催化剂A和催化剂B的催化效率与温度的关系如图所示:

实际应用中采取的条件是反应温度为T1,催化剂为A,分析原因是____ 。
 CH3OH(g)+H2O(g) △H。向1L某刚性容器中通入1molCO2和3molH2,在相同时间内不同催化剂作用下CO2的转化率(催化剂A作用下CO2的转化率为A%,催化剂B作用下CO2的转化率为B%)与温度的关系如表所示:
CH3OH(g)+H2O(g) △H。向1L某刚性容器中通入1molCO2和3molH2,在相同时间内不同催化剂作用下CO2的转化率(催化剂A作用下CO2的转化率为A%,催化剂B作用下CO2的转化率为B%)与温度的关系如表所示:| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| A% | 30% | 50% | 60% | 50% | 40% | 30% | 20% |
| B% | 10% | 30% | 50.5% | 50% | 40% | 30% | 20% |
回答下面问题:
(1)在CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)反应中△S
CH3OH(g)+H2O(g)反应中△S(2)温度在50℃以后,反应是否达到化学平衡状态?
(3)在50℃时,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)的平衡常数K=
CH3OH(g)+H2O(g)的平衡常数K=(4)图为反应在无催化剂、催化剂A和催化剂B的三种情况下“反应过程~能量”的示意图:

在图上标注“无催化剂”、“催化剂A”和“催化剂B”
(5)在相同条件下,催化剂A和催化剂B的催化效率与温度的关系如图所示:

实际应用中采取的条件是反应温度为T1,催化剂为A,分析原因是
您最近一年使用:0次
2022-10-12更新
|
88次组卷
|
2卷引用:河北省邢台市第二中学2022-2023学年高二上学期第一次月考化学试题



