解题方法
1 .  干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法
干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法错误 的是

 干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法
干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法
基元反应 |
|
| ||
|
|
|
| |
积碳: | 65.5 | 136.8 | 103.1 | 109.8 |
消碳: | 139.7 | 326.6 | 117.5 | 51.0 |
吸附在催化剂表面上的物种用*标注 | ||||
| A.一氧化碳歧化反应是放热反应 |
| B.甲烷裂解是镍基催化剂表面积碳的主要来源 |
C. 的焓变为 的焓变为 |
D.由上表判断,催化剂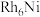 劣于 劣于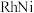 |
您最近一年使用:0次
解题方法
2 . 某化学实验小组设计了铝与相同浓度的不同铜盐溶液反应的实验方案,具体实验操作与现象如下。
下列说法错误的是
| 实验序号 | 实验操作 | 实验现象 |
| ① | 将铝片插入 溶液中 溶液中 | 长时间未观察到红色物质析出 |
| ② | 将铝片插入 溶液中 溶液中 | 15min后,铝片表面析出少量的红色物质,溶液颜色变化不明显 |
| ③ | Ⅰ.将铝片插入 溶液中 溶液中 | 反应迅速、剧烈,溶液呈酱油色样(含CuCl ) ) |
| Ⅱ.将酱油色样溶液倒入大量水中 | 产生白色沉淀(主要成分为CuCl) | |
| Ⅲ.取步骤Ⅱ反应后的上层清液,再插入铝 | 片产生大量无色气体,反应结束后生成大量红色海绵绒状物质,溶液变成无色 |
| A.可在实验①中加入NaCl固体,使铝片溶解 |
B.实验③的步骤Ⅰ中,溶液呈酱油色样的原因: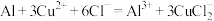 |
| C.实验③的步骤Ⅲ中,无色气体为H2,Cl-在实验Ⅲ中起催化与破坏保护膜的作用 |
D.相同条件下,Cu与等浓度的 溶液、 溶液、 溶液、 溶液、 溶液均不反应 溶液均不反应 |
您最近一年使用:0次
2024-03-15更新
|
173次组卷
|
2卷引用:江西省赣州市2024届高三下学期3月摸底考试化学试题
解题方法
3 . 铜镍硫化矿(主要成分NiS、CuS)有多种浸出方法:加压氨浸法、加压酸浸法、生物浸出法等。其中生物浸出法的原理如图所示。
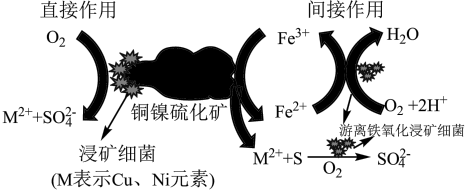
下列说法错误的是

下列说法错误的是
A.基态原子未成对电子数: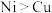 |
B. 在间接作用过程中起催化作用 在间接作用过程中起催化作用 |
| C.相比上述其他两种方法,生物浸出法具有操作简便、环境污染小等优点 |
D.浸出等质量的铜镍硫化矿,直接作用与间接作用所消耗的 的量不相等 的量不相等 |
您最近一年使用:0次
2024-03-15更新
|
127次组卷
|
2卷引用:江西省赣州市2024届高三下学期3月摸底考试化学试题
解题方法
4 . 反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)是我国科学家2021年发布的由CO2人工合成淀粉中的重要反应之一、CO2与H2制备甲醇在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的物种用*标注,TS为过渡态),下列说法不正确的是
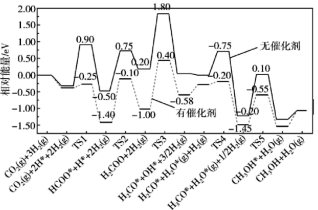

| A.升高温度,CO2与H2制备甲醇的反应v(逆)比v(正)增大的更多 |
| B.催化剂可使反应历程中决速步骤活化能降低0.20eV |
| C.加压、降温对制备甲醇有利,因此应该在高压、低温下进行上述反应 |
| D.CO2与H2制备甲醇反应往往伴随副反应,选择合适催化剂可提高甲醇反应的选择性 |
您最近一年使用:0次
解题方法
5 . 钴(Co)合金广泛应用于机械制造等领域。
(1)Co2+和Fe3+与KSCN溶液发生的反应相似。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为_____ 。
(2)推测Co+催化剂表面促进NH3还原NOx的反应历程如图所示。
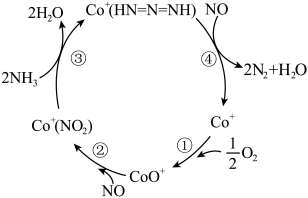
①在反应②中NO作_____ (填“氧化剂”或“还原剂”),与反应④中NO的作用_____ (填“是”或“不是”)一样的。
②写出步骤③对应的离子方程式:_____ 。
③整个历程中氧化剂与还原剂的物质的量之比为_____ 。
(3)现将35.7gCoCO3在空气中加热,可得24.1g钴的氧化物和另一种氧化物。试写出CoCO3在空气中受热时发生反应的化学方程式:_____ 。
(1)Co2+和Fe3+与KSCN溶液发生的反应相似。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为
(2)推测Co+催化剂表面促进NH3还原NOx的反应历程如图所示。

①在反应②中NO作
②写出步骤③对应的离子方程式:
③整个历程中氧化剂与还原剂的物质的量之比为
(3)现将35.7gCoCO3在空气中加热,可得24.1g钴的氧化物和另一种氧化物。试写出CoCO3在空气中受热时发生反应的化学方程式:
您最近一年使用:0次
解题方法
6 . 科学研究人员结合实验与计算机模拟结果,研究了CO2与H2在Pt/SiO2催化剂表面上生成CO和H2O的反应历程,其部分反应历程如图所示(吸附在Pt/SiO2催化剂表面上的物种用“·”标注,Ts表示过渡态)。
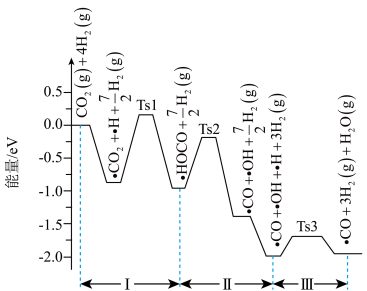
下列有关叙述正确的是

下列有关叙述正确的是
| A.升高温度总是能加快总反应速率 |
| B.上述条件下,上述反应释放能量小于无催化剂时释放能量 |
| C.上述反应历程中每一步均存在H-H键的断裂 |
| D.上述反应的速率由第I步反应决定 |
您最近一年使用:0次
7 . 18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为如下所示:
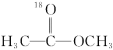 +OH-
+OH-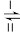
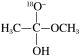
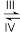
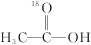 +CH3O-
+CH3O-
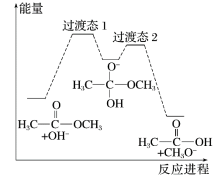
已知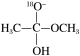

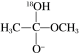 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是
| A.反应Ⅱ、Ⅲ为决速步 |
| B.反应结束后,溶液中存在18OH- |
| C.反应结束后,溶液中存在CH318OH |
| D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变 |
您最近一年使用:0次
名校
8 . 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述不正确的是

| A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.若图甲所示实验中反应速率:①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 |
| C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间 |
| D.为检查图乙所示装置的气密性,可关闭A处旋塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2024-03-12更新
|
989次组卷
|
5卷引用:河南省濮阳市南乐县第一高级中学2023-2024学年高一下学期模拟预测化学试题
名校
9 . 研究 资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。已知:
资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。已知:
I.
II.
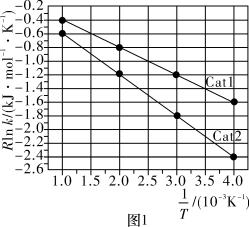
(1)一定条件下,速率常数与活化能、温度的关系式为 (R、C为常数,k为速率常数,
(R、C为常数,k为速率常数, 为活化能,T为温度)。一定温度下,反应Ⅰ的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图1所示。
为活化能,T为温度)。一定温度下,反应Ⅰ的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图1所示。
在Cat2作用下,该反应的活化能 为
为___________  ;催化效果更好的是
;催化效果更好的是___________ (填“Cat1”或“Cat2”)。
(2) 在
在 催化下,同时发生反应I、II;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的
催化下,同时发生反应I、II;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的 及
及 ;起始及达到平衡时(tmin时恰好达到平衡),容器内各气体物质的量及总压强如下表:
;起始及达到平衡时(tmin时恰好达到平衡),容器内各气体物质的量及总压强如下表:
若反应I、II均达到平衡时, ;则表中
;则表中
___________ ;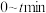 内,
内, 的分压变化率为
的分压变化率为___________  ;反应I的平衡常数
;反应I的平衡常数
___________ 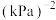 。
。
(3) 催化加氢制甲烷涉及的反应主要有:
催化加氢制甲烷涉及的反应主要有:
主反应:
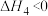
副反应:

若将 和
和 按体积比为
按体积比为 混合(
混合(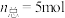 ),匀速通入装有催化剂的反应容器中,发生上述反应(包括主反应和副反应)。反应相同时间,
),匀速通入装有催化剂的反应容器中,发生上述反应(包括主反应和副反应)。反应相同时间, 转化率、
转化率、 和CO选择性随温度变化的曲线分别如图所示。
和CO选择性随温度变化的曲线分别如图所示。
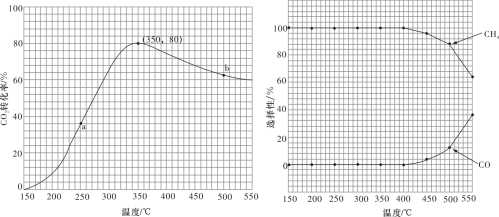
①a点的正反应速率和逆反应速率的大小关系为
___________ (填“>”“=”或“<”) 。
。
②催化剂在较低温度时主要选择___________ (填“主反应”或“副反应”)。
③350~400℃时; 转化率呈现减小的变化趋势,其原因是
转化率呈现减小的变化趋势,其原因是___________ 。
 资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。已知:
资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。已知:I.

II.

(1)一定条件下,速率常数与活化能、温度的关系式为
 (R、C为常数,k为速率常数,
(R、C为常数,k为速率常数, 为活化能,T为温度)。一定温度下,反应Ⅰ的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图1所示。
为活化能,T为温度)。一定温度下,反应Ⅰ的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图1所示。在Cat2作用下,该反应的活化能
 为
为 ;催化效果更好的是
;催化效果更好的是
(2)
 在
在 催化下,同时发生反应I、II;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的
催化下,同时发生反应I、II;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的 及
及 ;起始及达到平衡时(tmin时恰好达到平衡),容器内各气体物质的量及总压强如下表:
;起始及达到平衡时(tmin时恰好达到平衡),容器内各气体物质的量及总压强如下表:| 物质的量/mol | 总压强/kPa | |||||
 |  |  | CO |  | ||
| 起始 | 0.5 | 0.9 | 0 | 0 | 0 |  |
| 平衡 | n | 0.3 | p | |||
 ;则表中
;则表中
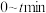 内,
内, 的分压变化率为
的分压变化率为 ;反应I的平衡常数
;反应I的平衡常数
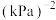 。
。(3)
 催化加氢制甲烷涉及的反应主要有:
催化加氢制甲烷涉及的反应主要有:主反应:

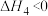
副反应:


若将
 和
和 按体积比为
按体积比为 混合(
混合(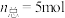 ),匀速通入装有催化剂的反应容器中,发生上述反应(包括主反应和副反应)。反应相同时间,
),匀速通入装有催化剂的反应容器中,发生上述反应(包括主反应和副反应)。反应相同时间, 转化率、
转化率、 和CO选择性随温度变化的曲线分别如图所示。
和CO选择性随温度变化的曲线分别如图所示。
①a点的正反应速率和逆反应速率的大小关系为

 。
。②催化剂在较低温度时主要选择
③350~400℃时;
 转化率呈现减小的变化趋势,其原因是
转化率呈现减小的变化趋势,其原因是
您最近一年使用:0次
名校
10 . 实验是化学研究的一种重要手段,请完成以下实验的探究与分析。
I.化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式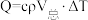 计算获得。
计算获得。
(1)配制0.50 NaOH溶液。
NaOH溶液。
①若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体___________ g。
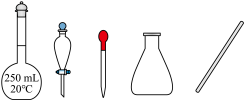
②实验中所需的玻璃仪器有烧杯、量筒和___________ 。(从下图中选择,写出名称)
(2)测定热量:将浓度为 的酸溶液和
的酸溶液和 的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和
的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和 分别取
分别取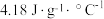 和
和 ,下同)。
,下同)。
①温度:b___________ c(填“>”“<”或“=”),理由是___________ 。
②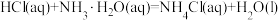 的
的
___________ 。
Ⅱ.碘及其化合物在人类活动中占有重要地位。“大象牙膏”实验中,将H2O2、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
第一步:H2O2+I-=H2O+IO-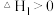 慢反应
慢反应
第二步:H2O2+IO-=O2+I-+H2O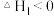 快反应
快反应
(3)该反应的决速步骤为___________ ,总反应方程式为___________ 。
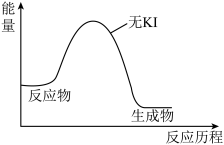
(4)在答题卡的图中画出有KI参与的两步反应的能量历程图___________ 。
I.化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式
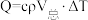 计算获得。
计算获得。(1)配制0.50
 NaOH溶液。
NaOH溶液。①若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体
②实验中所需的玻璃仪器有烧杯、量筒和

(2)测定热量:将浓度为
 的酸溶液和
的酸溶液和 的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和
的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和 分别取
分别取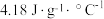 和
和 ,下同)。
,下同)。| 序号 | 体系温度/℃ | ||
| 反应试剂 | 反应前 | 反应后 | |
| i | HCl+NaOH | a | b |
| ii | HCl+NH₃·H₂O | a | c |
②
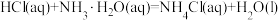 的
的
Ⅱ.碘及其化合物在人类活动中占有重要地位。“大象牙膏”实验中,将H2O2、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
第一步:H2O2+I-=H2O+IO-
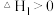 慢反应
慢反应第二步:H2O2+IO-=O2+I-+H2O
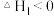 快反应
快反应(3)该反应的决速步骤为
(4)在答题卡的图中画出有KI参与的两步反应的能量历程图

您最近一年使用:0次







