名校
解题方法
1 . 氢气作为一种清洁能源,一直是能源研究的热点,水煤气变换反应可用于大规模制 ,反应原理如下:
,反应原理如下:
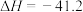 kJ⋅mol
kJ⋅mol
(1)根据下表中提供的数据,计算

 。
。化学键 |
|
|
|
|
键能/kJ·mol | 803 | x | 463 | 436 |
(2)某温度下,在一恒容密闭容器中充入CO和
 ,加入催化剂使其发生上述反应(忽略其他副反应),测得该反应中初始压强为
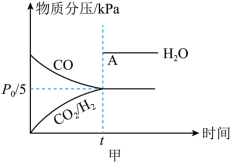
,加入催化剂使其发生上述反应(忽略其他副反应),测得该反应中初始压强为 ,分压如图甲所示(t时刻前,
,分压如图甲所示(t时刻前, 的分压未给出),则A点坐标为(t,
的分压未给出),则A点坐标为(t,
(3)反应
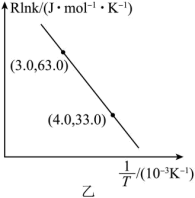
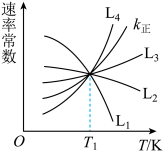
 的Arrhenius经验公式的实验数据如图乙中曲线所示,已知经验公式为
的Arrhenius经验公式的实验数据如图乙中曲线所示,已知经验公式为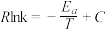 (其中
(其中 为活化能,k为速率常数,R和C为常数)。该反应的活化能
为活化能,k为速率常数,R和C为常数)。该反应的活化能
当使用更高效催化剂时,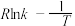
您最近一年使用:0次
2 . 合成氨时采用400-500℃左右的温度进行,主要是因为在该温度时
| A.合成氨的化学反应限度最大 | B.N2的转化率最高 |
| C.催化剂的活性最大 | D.NH3在平衡混合气体中的体积分数最大 |
您最近一年使用:0次
名校
3 . 在一定条件下探究二甲醚的制备反应为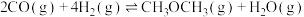
 ,测定结果如图所示。下列判断错误的是
,测定结果如图所示。下列判断错误的是
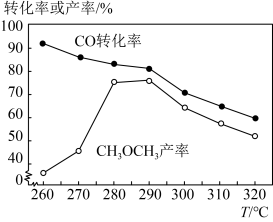
A.该反应的 | B.该反应伴随着副反应的发生 |
| C.加入催化剂可以提高CH3OCH3的产率 | D.工业上选择的较适宜温度为280~290℃ |
您最近一年使用:0次
名校
4 . 资源化利用二氧化硫,一方面能保护环境,另一方面能提高经济效益,具有深远意义。钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)常温下进行“钠碱法”的模拟实验。用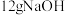 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________ L(折算成标准状况)。若实验时只吸收了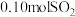 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为___________ 。
(2)当钠碱法的吸收液 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是___________ (填写化学式)。
(3)将 通入
通入 溶液时,得到一组
溶液时,得到一组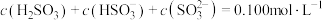 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
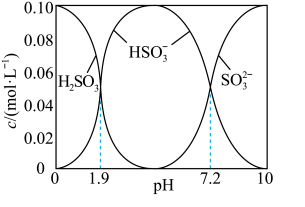
若溶液的 ,溶液中
,溶液中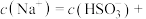
___________ 此时溶液中
___________  。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)
(4)亚硫酸为二元弱酸, 时,其电离常数
时,其电离常数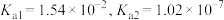 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。___________ 。
(5)工业中可用含 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了___________ (选填编号)。
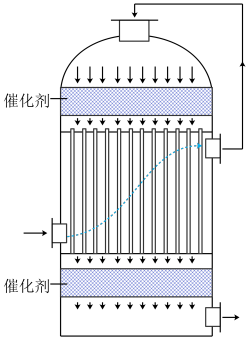
a.充分利用热能 b.防止形成酸雾 c.加速转化 d.获取纯净
d.获取纯净
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)常温下进行“钠碱法”的模拟实验。用
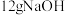 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为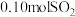 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为(2)当钠碱法的吸收液
 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是(3)将
 通入
通入 溶液时,得到一组
溶液时,得到一组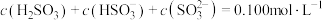 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
若溶液的
 ,溶液中
,溶液中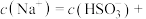

 。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)(4)亚硫酸为二元弱酸,
 时,其电离常数
时,其电离常数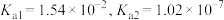 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。(5)工业中可用含
 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了
a.充分利用热能 b.防止形成酸雾 c.加速转化
 d.获取纯净
d.获取纯净
您最近一年使用:0次
名校
5 . 在催化剂表面,丙烷催化氧化脱氢反应历程如下图.下列说法正确的是
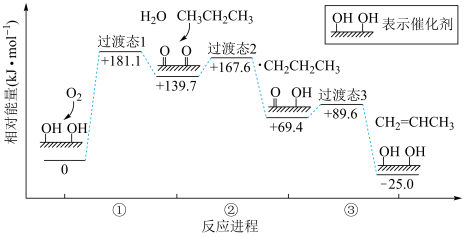
A.催化剂改变了丙烷氧化脱氢的焓变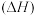 | B.①中,催化剂发生氧化反应 |
| C.过渡态物质的稳定性:过渡态2小于过渡态1 | D.总反应的速率由③决定 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.升高温度,速率加快,说明升高温度反应的活化能降低 |
| B.有些反应在磁场下反应速率加快,说明活化分子数增大 |
| C.氢气在氯气中燃烧时,释放的化学能等于产生的热能 |
| D.化学反应的焓变是决定化学反应方向的唯一因素 |
您最近一年使用:0次
7 .  的资源化利用是实现碳中和的重要途径。
的资源化利用是实现碳中和的重要途径。
Ⅰ.热化学法处理 。
。 加氢制
加氢制 的反应为:
的反应为:
(1)该反应能自发进行的主要原因是___________ 。
(2)该反应的正逆反应速率可分别表示为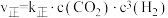 ,
,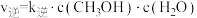 ,其中
,其中 、
、 为速率常数。如图所示能够代表
为速率常数。如图所示能够代表 的曲线为
的曲线为___________ (填“ ”“
”“ ”“
”“ ”或“
”或“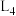 ”);若该反应的化学平衡常数
”);若该反应的化学平衡常数 ,那么发生该反应的温度
,那么发生该反应的温度___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)在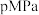 下,将
下,将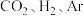 按物质的量之比为
按物质的量之比为 充入密闭容器,
充入密闭容器, 的平衡转化率为
的平衡转化率为 ,此时平衡常数
,此时平衡常数
___________  。
。
(4)实际合成反应时,也会有 等生成。在恒压条件下
等生成。在恒压条件下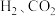 的体积比为
的体积比为 反应时,在催化剂作用下反应相同时间所测得的
反应时,在催化剂作用下反应相同时间所测得的 选择性和产率随温度的变化如图所示:
选择性和产率随温度的变化如图所示:

①合成 最适宜的温度为
最适宜的温度为___________
②在 范围内随着温度的升高,
范围内随着温度的升高, 的产率迅速升高的原因是
的产率迅速升高的原因是___________ 。
Ⅱ.回收利用工业废气中的 和
和 ,实验原理示意图如下。
,实验原理示意图如下。
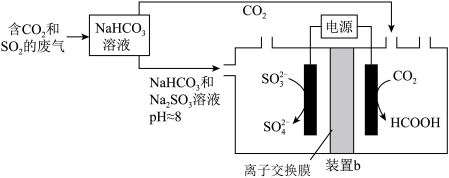
(5)反应后装置b中溶液
___________ (填“增大”、“减小”或“不变”),装置b中的总反应的离子方程式为___________ 。
 的资源化利用是实现碳中和的重要途径。
的资源化利用是实现碳中和的重要途径。Ⅰ.热化学法处理
 。
。 加氢制
加氢制 的反应为:
的反应为:
(1)该反应能自发进行的主要原因是
(2)该反应的正逆反应速率可分别表示为
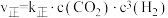 ,
,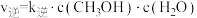 ,其中
,其中 、
、 为速率常数。如图所示能够代表
为速率常数。如图所示能够代表 的曲线为
的曲线为 ”“
”“ ”“
”“ ”或“
”或“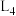 ”);若该反应的化学平衡常数
”);若该反应的化学平衡常数 ,那么发生该反应的温度
,那么发生该反应的温度 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)在
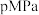 下,将
下,将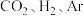 按物质的量之比为
按物质的量之比为 充入密闭容器,
充入密闭容器, 的平衡转化率为
的平衡转化率为 ,此时平衡常数
,此时平衡常数
 。
。(4)实际合成反应时,也会有
 等生成。在恒压条件下
等生成。在恒压条件下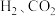 的体积比为
的体积比为 反应时,在催化剂作用下反应相同时间所测得的
反应时,在催化剂作用下反应相同时间所测得的 选择性和产率随温度的变化如图所示:
选择性和产率随温度的变化如图所示:
①合成
 最适宜的温度为
最适宜的温度为②在
 范围内随着温度的升高,
范围内随着温度的升高, 的产率迅速升高的原因是
的产率迅速升高的原因是Ⅱ.回收利用工业废气中的
 和
和 ,实验原理示意图如下。
,实验原理示意图如下。
(5)反应后装置b中溶液

您最近一年使用:0次
名校
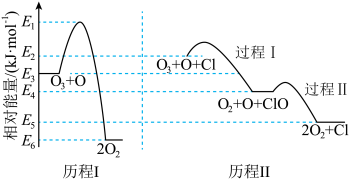
8 . 标准状况下,气态反应物和生成物的相对能量与反应历程示意图如下,已知: 和
和 的相对能量为0。下列说法错误的是
的相对能量为0。下列说法错误的是
 和
和 的相对能量为0。下列说法错误的是
的相对能量为0。下列说法错误的是
A.相同条件下, 的平衡转化率:历程Ⅰ=历程Ⅱ 的平衡转化率:历程Ⅰ=历程Ⅱ |
B.可计算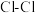 键能为 键能为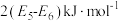 |
C.由图可知 |
| D.历程Ⅱ反应的快慢取决于过程Ⅰ反应的快慢 |
您最近一年使用:0次
解题方法
9 . 在酸性条件下,黄铁矿( ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
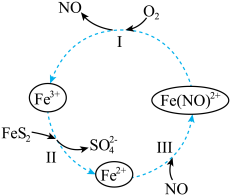
总反应:
(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:_______ 。
②反应Ⅱ:_______ 。
(2)NO在总反应中的作用是_______ 。
 ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
总反应:

(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:
②反应Ⅱ:
(2)NO在总反应中的作用是
您最近一年使用:0次
名校
10 . 常温常压下利用Cu/ZnO/ZrO催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注):
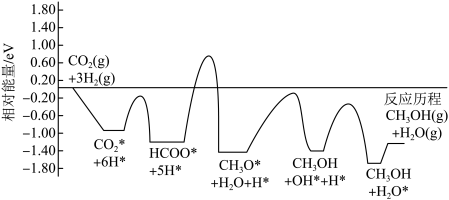
A.转化历程有四个基元反应,决速步为: |
| B.若无Cu/ZnO/ZrO催化剂,二氧化碳加氢制甲醇不能自发进行 |
| C.反应过程中断裂与形成的共价键类型相同 |
D.寻找高效催化剂,有利于 的回收利用,使该反应原子利用率达到100% 的回收利用,使该反应原子利用率达到100% |
您最近一年使用:0次
2024-03-17更新
|
486次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题
江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题湖北省七市州教科研协作体2024届高三下学期二模化学试题(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题04?化学反应机理、历程、能垒图分析(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)







