名校
解题方法
1 . 研究表明, 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是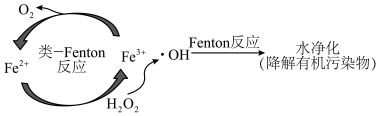
A.0.1mol羟基自由基(·OH)所含电子的数目为 |
B. 可以改变反应历程,降低 可以改变反应历程,降低 分解反应的反应热 分解反应的反应热 |
C. 与 与 反应产生羟基自由基的反应为 反应产生羟基自由基的反应为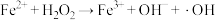 |
| D.去除废水中难降解的有机污染物,主要利用了羟基自由基的还原性 |
您最近一年使用:0次
2024-04-05更新
|
153次组卷
|
3卷引用:河北省石家庄市河北正定中学2023-2024学年高三下学期第一次月考化学试题
名校
解题方法
2 . 某同学对甲苯与高锰酸钾水溶液反应速率做了如下两个探究实验:
实验Ⅰ: 取一定量的甲苯与一定体积,一定浓度的高锰酸钾水溶液混合,振荡 缓慢褪色。
缓慢褪色。
实验Ⅱ: 在实验Ⅰ的试剂取量基础上,再加入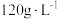 的冠醚(18—冠—6),振荡,
的冠醚(18—冠—6),振荡,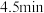 褪色。
褪色。
实验Ⅰ: 取一定量的甲苯与一定体积,一定浓度的高锰酸钾水溶液混合,振荡
 缓慢褪色。
缓慢褪色。实验Ⅱ: 在实验Ⅰ的试剂取量基础上,再加入
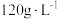 的冠醚(18—冠—6),振荡,
的冠醚(18—冠—6),振荡,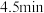 褪色。
褪色。
| A.冠醚是该反应的催化剂 |
B. 与冠醚形成的超分子可溶于甲苯 与冠醚形成的超分子可溶于甲苯 |
C.冠醚与 之间以弱配位键作用实现对 之间以弱配位键作用实现对 的识别 的识别 |
D.实验Ⅰ反应速率小的原因是高锰酸钾不溶于甲苯,氧化剂 与还原剂甲苯接触不充分 与还原剂甲苯接触不充分 |
您最近一年使用:0次
名校
3 . 某学习小组利用5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O来探究“外界条件对化学反应速率的影响”。实验时,先分别量取KMnO4酸性溶液、H2C2O4(一种弱酸)溶液,然后倒入大试管中迅速振荡,通过测定褪色所需时间来判断反应的快慢。
(1)下列因素能加快该反应速率的是___________。
(2)为了观察到紫色褪去,如果H2C2O4与KMnO4溶液的体积相同,则它们初始物质的量浓度需要满足的关系为:c(H2C2O4):c(KMnO4)___________ 。
(3)甲同学设计了如下实验
①探究温度对化学反应速率影响的组合实验编号是___________ 。
②已知b实验生成CO2体积随时间的变化曲线如图,请在图中画出a实验生成CO2体积随时间的变化曲线。___________

③实验b测得混合后溶液褪色的时间为30s,忽略混合前后体积的微小变化,则这段时间平均反应速率v(H2C2O4)=___________ (保留3位有效数字)。
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①乙同学据此提出以下假设:
假设1:___________ 。
假设2:生成Mn2+对反应有催化作用
假设3:生成CO2对反应有催化作用
假设4:反应生成的K+或 该反应有催化作用
该反应有催化作用
丙同学认为假设4不合理,其理由是___________ 。
②丁同学用如下实验证明假设2成立:在A和B二试管中分别加入4mL0.2mol·L-1草酸溶液,再在A试管中加入lmL0.1mol·L-1MnSO4溶液、B试管中加入___________ mL蒸馏水,然后在两支试管中同时分别加入1mL0.1mol·L-1KMnO4酸性溶液。预期的实验现象是___________ 。在B试管中加入蒸馏水的目的是___________ 。同学们认为不宜用MnCl2溶液代替MnSO4溶液对该反应进行催化探究,其原因是(用离子方程式表示)___________ 。
(1)下列因素能加快该反应速率的是___________。
| A.加入少量K2SO4固体 | B.加入少量NaCl固体 |
| C.增大压强 | D.加入少量Na2C2O4固体 |
(2)为了观察到紫色褪去,如果H2C2O4与KMnO4溶液的体积相同,则它们初始物质的量浓度需要满足的关系为:c(H2C2O4):c(KMnO4)
(3)甲同学设计了如下实验
| 实验 编号 | H2C2O4溶液 | KMnO4溶液 | 温度/℃ | 褪色时间/s | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | |||
| a | 0.10 | 2.0 | 0.010 | 4.0 | 25 | t1 |
| b | 0.20 | 2.0 | 0.010 | 4.0 | 25 | t2 |
| c | 0.20 | 2.0 | 0.010 | 4.0 | 50 | t3 |
②已知b实验生成CO2体积随时间的变化曲线如图,请在图中画出a实验生成CO2体积随时间的变化曲线。

③实验b测得混合后溶液褪色的时间为30s,忽略混合前后体积的微小变化,则这段时间平均反应速率v(H2C2O4)=
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①乙同学据此提出以下假设:
假设1:
假设2:生成Mn2+对反应有催化作用
假设3:生成CO2对反应有催化作用
假设4:反应生成的K+或
 该反应有催化作用
该反应有催化作用丙同学认为假设4不合理,其理由是
②丁同学用如下实验证明假设2成立:在A和B二试管中分别加入4mL0.2mol·L-1草酸溶液,再在A试管中加入lmL0.1mol·L-1MnSO4溶液、B试管中加入
您最近一年使用:0次
名校
解题方法
4 . 据文献显示: 催化合成DMC的一种反应机理如图所示。下列叙述正确的是
催化合成DMC的一种反应机理如图所示。下列叙述正确的是
 催化合成DMC的一种反应机理如图所示。下列叙述正确的是
催化合成DMC的一种反应机理如图所示。下列叙述正确的是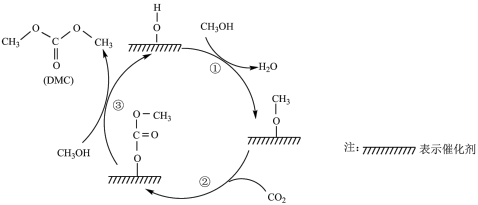
A. 是反应中间体 是反应中间体 |
B.①②③中均有 的断裂 的断裂 |
C. 可有效提高DMC的产率 可有效提高DMC的产率 |
D.合成DMC的反应为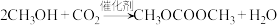 |
您最近一年使用:0次
2024-04-03更新
|
83次组卷
|
2卷引用:云南省大理市下关第一中学2023-2024学年高二下学期3月月考化学试题
5 . 中国科学家在实验室内实现了从二氧化碳到糖的精准全合成,合成过程如图所示。下列说法错误的是
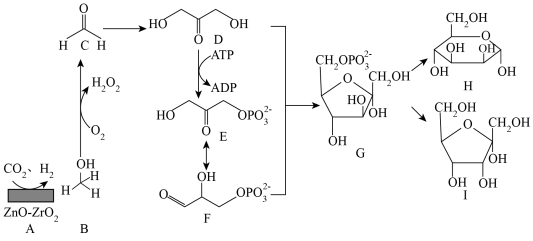
| A.化合物B生成化合物C的反应为氧化反应 |
| B.化合物D中所有原子可能共平面 |
| C.化合物E和F均能使酸性高锰酸钾溶液褪色 |
| D.化合物H、I互为同分异构体 |
您最近一年使用:0次
2024-04-02更新
|
72次组卷
|
2卷引用:河北省石家庄市第十七中学2023-202424学年高三下学期3月月考化学试题
名校
解题方法
6 . 氮及其化合物的转化过程如图所示。下列分析不合理的是
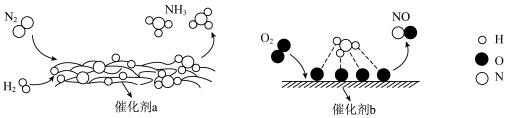
| A.催化剂a表面发生了极性共价键的断裂和形成 |
B. 与 与 反应生成 反应生成 的原子利用率(期望产物的总质量与生成物的总质量之比)为100% 的原子利用率(期望产物的总质量与生成物的总质量之比)为100% |
| C.在催化剂b表面形成氮氧键时,涉及电子转移 |
| D.使用催化剂a、b均可以提高单位时间内生成物的产量 |
您最近一年使用:0次
2024-04-02更新
|
230次组卷
|
3卷引用:四川省成都市树德中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
7 . 氧化铟基纳米催化剂 可用于
可用于 选择性加氢制备
选择性加氢制备 ,其反应机理如图所示。下列说法
,其反应机理如图所示。下列说法不正确 的是
 可用于
可用于 选择性加氢制备
选择性加氢制备 ,其反应机理如图所示。下列说法
,其反应机理如图所示。下列说法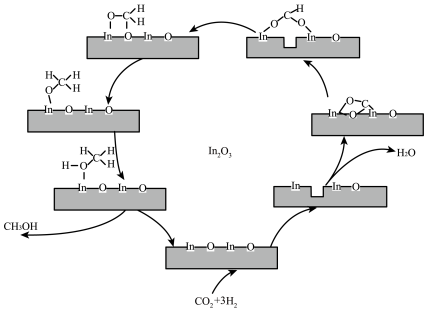
A.该反应每生成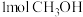 ,转移 ,转移 电子 电子 |
B. 与 与 中,碳原子的杂化方式分别是 中,碳原子的杂化方式分别是 与 与 杂化 杂化 |
C.该反应过程中 只有 只有 键断裂,没有 键断裂,没有 键断裂,但有新 键断裂,但有新 键形成 键形成 |
D.催化剂 ,参与反应生成了过渡态物质,降低了反应的活化能,加快了化学反应速率 ,参与反应生成了过渡态物质,降低了反应的活化能,加快了化学反应速率 |
您最近一年使用:0次
2024-04-02更新
|
93次组卷
|
2卷引用:浙江省精诚联盟2023-2024学年高二下学期3月月考化学试题
解题方法
8 . 2023 年杭州亚运会主火炬创新使用了绿色“零碳甲醇”作为燃料,这不仅在亚运史上是第一次,在全球大型体育赛事上也是首次实现了废碳的再生利用。“零碳甲醇”是符合“碳中和”属性的绿色能源。
请回答下列问题:
(1)工业上主要利用以下反应合成甲醇: CO2(g)+3H2(g) CH3OH(g)+H2O(g)。已知在一定条件下该反应的
CH3OH(g)+H2O(g)。已知在一定条件下该反应的 = -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围
= -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围 ___________ K(用含a、b的代数式表示)。
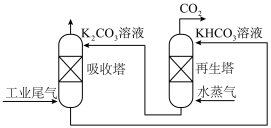
(2)目前有多种用于工业捕集CO2的方法,主要分为吸收(物理吸收、化学吸收、生物吸收)、吸附、深冷分离和膜分离等,也有将不同捕集方法相结合的方法。一种模拟脱除工业尾气中CO2的示意图如图所示: 后,
后, 则该溶液的pOH=
则该溶液的pOH=___________ (该温度下H2CO3的Ka1=4.6×10-7,Ka2=5.0×10-11 Kw=1×10-a,用含a的代数式表示)。
(3)CO2合成甲醇的工艺主要分为两类,一类称为直接法:CO2直接加H2合成甲醇;一类称为间接法:CO2和H2通过逆水煤气反应,先合成CO后,CO和H2再合成甲醇。
I.CO2 (g)+3H2 (g) CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
Ⅲ.CO(g)+2H2(g) 3CH3OH(g) ΔH3=-90kJ⋅mol-1
3CH3OH(g) ΔH3=-90kJ⋅mol-1
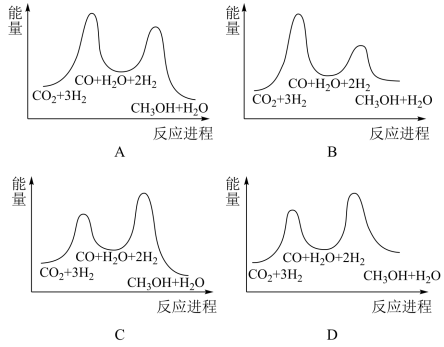
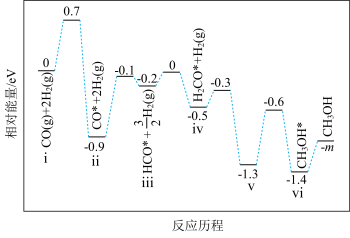
①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是___________ (填字母)。___________ 。
③工业生产中测定体系的压强具有实际意义。一定温度下,仅利用反应Ⅰ直接合成甲醇,将体积分数为a% CO2、3a% H2 的进料气(含杂质气体),以 Cu/Zn/Al/Zr纳米纤维为催化剂,控制压强为50 bar(1 bar=100 kPa)发生反应I,进料气中杂质气体不反应,达到平衡时二氧化碳的转化率为90%,达到平衡时, p(H2) =___________ bar,反应I的平衡常数Kp= ___________ bar-2(Kp为用分压表示的平衡常数,分压=总压×物质的量分数,用含a的代数式表示)。
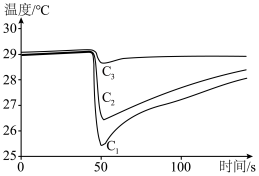
(4)甲醇便于运输,是一种具有前景的液体燃料,利用手持技术,通过测定甲醇、乙醇、正丙醇等三种物质在温度传感器尖头处蒸发时的温度变化曲线,根据曲线下降的幅度和速率的快慢,可以比较它们之间的分子间作用力的大小。请判断表示甲醇的曲线是___________ ,理由是___________ 。
请回答下列问题:
(1)工业上主要利用以下反应合成甲醇: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。已知在一定条件下该反应的
CH3OH(g)+H2O(g)。已知在一定条件下该反应的 = -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围
= -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围 (2)目前有多种用于工业捕集CO2的方法,主要分为吸收(物理吸收、化学吸收、生物吸收)、吸附、深冷分离和膜分离等,也有将不同捕集方法相结合的方法。一种模拟脱除工业尾气中CO2的示意图如图所示:
 后,
后, 则该溶液的pOH=
则该溶液的pOH=(3)CO2合成甲醇的工艺主要分为两类,一类称为直接法:CO2直接加H2合成甲醇;一类称为间接法:CO2和H2通过逆水煤气反应,先合成CO后,CO和H2再合成甲醇。
I.CO2 (g)+3H2 (g)
 CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1Ⅲ.CO(g)+2H2(g)
 3CH3OH(g) ΔH3=-90kJ⋅mol-1
3CH3OH(g) ΔH3=-90kJ⋅mol-1①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是
③工业生产中测定体系的压强具有实际意义。一定温度下,仅利用反应Ⅰ直接合成甲醇,将体积分数为a% CO2、3a% H2 的进料气(含杂质气体),以 Cu/Zn/Al/Zr纳米纤维为催化剂,控制压强为50 bar(1 bar=100 kPa)发生反应I,进料气中杂质气体不反应,达到平衡时二氧化碳的转化率为90%,达到平衡时, p(H2) =
(4)甲醇便于运输,是一种具有前景的液体燃料,利用手持技术,通过测定甲醇、乙醇、正丙醇等三种物质在温度传感器尖头处蒸发时的温度变化曲线,根据曲线下降的幅度和速率的快慢,可以比较它们之间的分子间作用力的大小。请判断表示甲醇的曲线是
您最近一年使用:0次
2024-04-02更新
|
171次组卷
|
2卷引用:安徽省部分学校2023-2024学年高三下学期3月联考化学试题
名校
解题方法
9 . N2H4是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某Ru(Ⅱ)催化剂用[L-Ru-NH3]+表示|能高效电催化氧化NH3合成N2H4,其反应机理如图所示(图中L为原子团)。下列说法错误的是
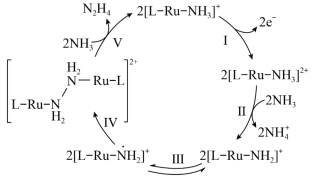
| A.[L-Ru-NH3]2+中Ru的化合价为+3 |
| B.反应Ⅳ中有非极性键的断裂与形成 |
| C.电催化氧化NH3合成N2H4发生在电解池阳极区 |
| D.N2H4与NH3中 N 原子的 VSEPR 模型均为四面体形 |
您最近一年使用:0次
2024-04-02更新
|
576次组卷
|
6卷引用:安徽省部分学校2023-2024学年高三下学期3月联考化学试题
安徽省部分学校2023-2024学年高三下学期3月联考化学试题广西省钦州市第四中学2023-2024学年高三下学期第八周考试化学试卷安徽省示范高中皖北协作区2024届高三联考化学试题江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 (已下线)通关练07 原子、分子、晶体结构再归纳-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)河南省郑州市宇华实验学校2024届高三下学期第三次模拟考试化学试题
名校
10 . 镍基材料作为甲醇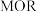 反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出
反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出 和
和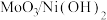 均能催化甲醇
均能催化甲醇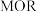 反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
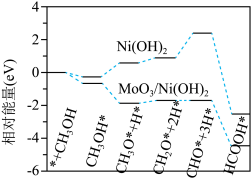
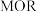 反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出
反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出 和
和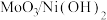 均能催化甲醇
均能催化甲醇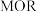 反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
A.文献中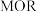 反应指的是还原反应 反应指的是还原反应 |
B.吸附甲醇的效果: 劣于 劣于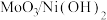 |
C. 催化下,消耗 催化下,消耗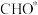 的步骤为决速步 的步骤为决速步 |
D.上述历程中碳原子的杂化类型由 转化为 转化为 |
您最近一年使用:0次



