1 .  的一种制备方法如图所示,下列说法不正确的是
的一种制备方法如图所示,下列说法不正确的是
 的一种制备方法如图所示,下列说法不正确的是
的一种制备方法如图所示,下列说法不正确的是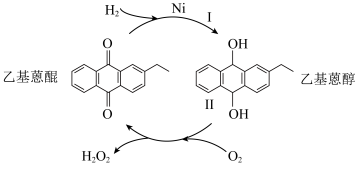
| A.反应Ⅰ中乙基蒽醌被氧化为乙基蒽醇 |
| B.催化剂镍改变了反应速率,未改变反应焓变 |
C.制备原理是 |
| D.乙基蒽醌是总反应的催化剂 |
您最近半年使用:0次
2 . 近日,广州大学韩冬雪、牛利团队报告了一种氧空位浓度可调的物质 ,直接用于温和条件下
,直接用于温和条件下 、
、 的协同光催化反应合成尿素。反应过程中的能量变化及机理如下:
的协同光催化反应合成尿素。反应过程中的能量变化及机理如下:
 ,直接用于温和条件下
,直接用于温和条件下 、
、 的协同光催化反应合成尿素。反应过程中的能量变化及机理如下:
的协同光催化反应合成尿素。反应过程中的能量变化及机理如下: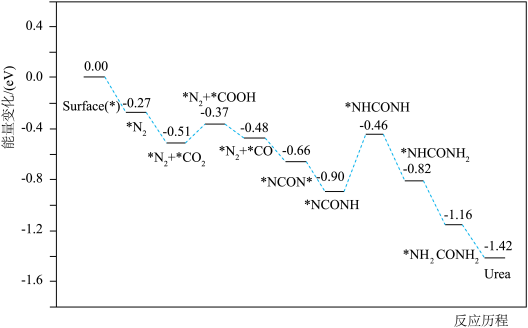
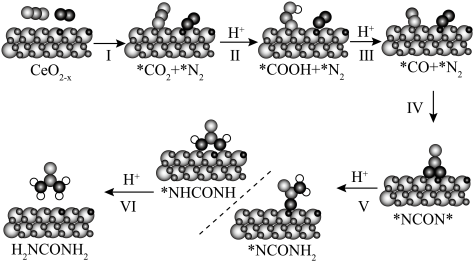
A. 是该尿素合成机理中的催化剂 是该尿素合成机理中的催化剂 |
B. 、 、 在 在 表面上的吸附是吸热反应 表面上的吸附是吸热反应 |
| C.步骤Ⅴ是该反应机理的决速步骤 |
D.该反应机理的氧化电极反应: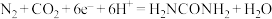 |
您最近半年使用:0次
名校
解题方法
3 . 氮氧化物( )都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:
)都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:
(1)NO在空气中发生氧化反应:
 ,该反应分两步完成,其反应历程如图所示。
,该反应分两步完成,其反应历程如图所示。_______ ;决定: 反应速率的是
反应速率的是_______ (填“反应I”或“反应Ⅱ”)。
(2)T℃,在密闭容器中尝试利用表面催化工艺分解NO,若用 分别表示
分别表示 ,NO,
,NO, 和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示:
和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示:
(3)厌氧氨化法(Anammox)是一种新型的氨氮去除技术,反应模型如图。 )是
)是_______ (填“极性”或“非极性”)分子。羟胺( )可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为
)可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为_______ ;
②该过程的总反应的方程式为_______ 。
(4)在恒温条件下,向初始压强为PMPa的恒容密闭容器中加入等物质的量CO和NO发生反应: ,反应达到平衡时,
,反应达到平衡时, 的体积分数为20%,则NO的转化率为
的体积分数为20%,则NO的转化率为_______ (保留一位小数)。该条件下反应平衡常数
_______ MPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 )都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:
)都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:(1)NO在空气中发生氧化反应:

 ,该反应分两步完成,其反应历程如图所示。
,该反应分两步完成,其反应历程如图所示。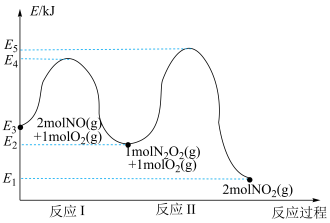
 反应速率的是
反应速率的是(2)T℃,在密闭容器中尝试利用表面催化工艺分解NO,若用
 分别表示
分别表示 ,NO,
,NO, 和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示:
和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示: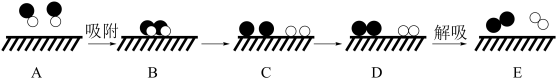
| A.b到c吸热,c到d放热 |
| B.当体系压强恒定时,反应达到平衡状态 |
C.除去体系中 可提高NO的平衡转化率 可提高NO的平衡转化率 |
| D.固体催化剂起到反应载体的作用,不改变反应的活化能和焓变 |
(3)厌氧氨化法(Anammox)是一种新型的氨氮去除技术,反应模型如图。
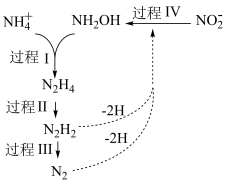
 )是
)是 )可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为
)可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为②该过程的总反应的方程式为
(4)在恒温条件下,向初始压强为PMPa的恒容密闭容器中加入等物质的量CO和NO发生反应:
 ,反应达到平衡时,
,反应达到平衡时, 的体积分数为20%,则NO的转化率为
的体积分数为20%,则NO的转化率为
您最近半年使用:0次
名校
解题方法
4 . 甲烷是一种清洁燃料,与水制氢和天然气脱硫具有重要的现实意义。回答下列问题:
Ⅰ.一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
①
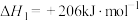
②
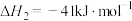
恒定压强为100kPa时,将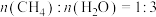 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。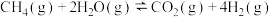

______  ,反应在
,反应在______ 条件下能自发进行。
(2)600℃时, 的平衡分压为
的平衡分压为______ kPa,反应②的物质的量分数的平衡常数
______ (用物质的量分数代替平衡浓度计算,保留2位有效数字)。
(3)系统中q的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:______ 。
Ⅱ.与 重整,不但可以消除污染,还可以制氢。主要反应如下:
重整,不但可以消除污染,还可以制氢。主要反应如下: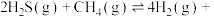
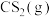
 。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。
。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。
(4)图(a)为800℃、 催化剂条件下投入等量
催化剂条件下投入等量 ,不同投料比分别达到平衡时
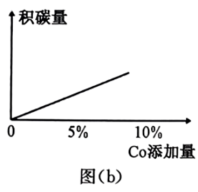
,不同投料比分别达到平衡时 转化率、平均反应速率图。C组图像中平均速率最低的原因可能是
转化率、平均反应速率图。C组图像中平均速率最低的原因可能是______ ;相同质量的同种催化剂,在载体上的分散度越高,催化作用越强,原因是______ 。______ 反应(填化学方程式)。
Ⅰ.一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
①

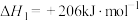
②

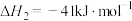
恒定压强为100kPa时,将
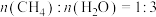 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。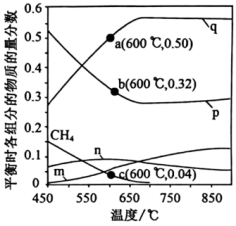
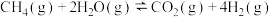

 ,反应在
,反应在(2)600℃时,
 的平衡分压为
的平衡分压为
(3)系统中q的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
Ⅱ.与
 重整,不但可以消除污染,还可以制氢。主要反应如下:
重整,不但可以消除污染,还可以制氢。主要反应如下: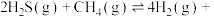
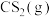
 。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。
。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。(4)图(a)为800℃、
 催化剂条件下投入等量
催化剂条件下投入等量 ,不同投料比分别达到平衡时
,不同投料比分别达到平衡时 转化率、平均反应速率图。C组图像中平均速率最低的原因可能是
转化率、平均反应速率图。C组图像中平均速率最低的原因可能是
您最近半年使用:0次
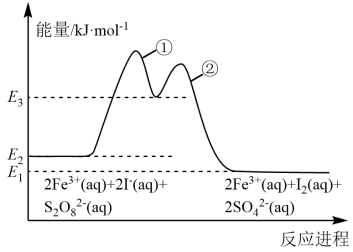
5 . 已知 催化反应
催化反应 历程如下图所示,催化历程中有
历程如下图所示,催化历程中有 参与。下列有关该反应的说法正确的是
参与。下列有关该反应的说法正确的是
 催化反应
催化反应 历程如下图所示,催化历程中有
历程如下图所示,催化历程中有 参与。下列有关该反应的说法正确的是
参与。下列有关该反应的说法正确的是
| A.步骤①的速率常数大于步骤② |
| B.反应历程中存在非极性键的断裂和形成 |
| C.催化历程中,仅氧元素的化合价未发生变化 |
D.步骤②的热化学方程为:  |
您最近半年使用:0次
名校
6 . PTC(可表示为Q+X-)的作用是使一种反应物由一相转移到另一相中参加反应,促使一个可以溶于有机溶剂的底物和一个不溶于此溶剂的离子型试剂两者之间发生反应。下列说法错误的是
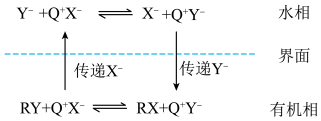
A.总反应为: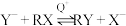 |
| B.Q+易溶于水相而难溶于有机相 |
| C.PTC是相转移催化剂,且化学性质应稳定且易回收 |
| D.不使用昂贵的特殊溶剂,且不要求无水操作,简化了工艺 |
您最近半年使用:0次
7 . 在酸性环境中,纳米Fe/Ni复合材料去除污染水体的N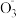 的反应过程(Ni不参与反应)如图所示,下列说法正确的是
的反应过程(Ni不参与反应)如图所示,下列说法正确的是
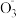 的反应过程(Ni不参与反应)如图所示,下列说法正确的是
的反应过程(Ni不参与反应)如图所示,下列说法正确的是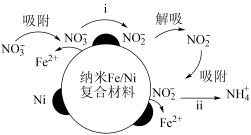
| A.反应步骤i中产生了气体 | B.反应步骤ⅱ不需要H+的参与 |
C.去除N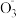 后的水体pH增大 后的水体pH增大 | D.处理过程中Fe/Ni复合材料作催化剂 |
您最近半年使用:0次
8 . 45℃时,碱性条件下,用负载在Al2O3表面的纳米Ag作催化剂可将甲醛转化为H2,反应的机理如图所示。下列说法不正确的是
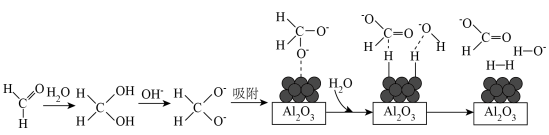
| A.图中第一步为加成反应 |
B.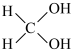 只有一种结构 只有一种结构 |
| C.若将甲醛中的氢用D原子标记为DCDO,得到的氢气产物为D2 |
| D.制得高纯度的氢气,同时可处理有毒的甲醛是甲醛制氢的优点之一 |
您最近半年使用:0次
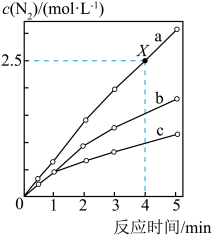
9 . 相同条件下,在固定容积的密闭容器中选用不同的催化剂(a、b、c)发生反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
| A.催化剂的催化效率:a>b>c |
| B.X点时,NH3的化学反应速率为0.5 mol·L-1·min-1 |
| C.使用催化剂a、b、c达到平衡时NO的转化率相等 |
| D.若在恒容绝热的密闭容器中发生该反应,当K值不变时,说明反应已经达到平衡 |
您最近半年使用:0次
10 .  的捕集和利用具有重要意义。
的捕集和利用具有重要意义。
 .
. 的催化氧化
的催化氧化
(1) 在
在 表面催化氧化的过程始于
表面催化氧化的过程始于 与
与 形成的酸性位点(如图所示),并生成金属硫酸盐(
形成的酸性位点(如图所示),并生成金属硫酸盐(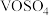 )中间体。
)中间体。___________ 。
②写出中间体受热分解产生 、
、 的化学方程式:
的化学方程式:___________ 。
(2)一定温度下,恒压密闭容器中发生反应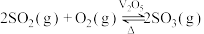
 ,
, 平衡转化率与反应温度和压强的关系如图所示。
平衡转化率与反应温度和压强的关系如图所示。
___________ (填“=0”或“>0”或“<0”)。
②实际生产中选择图中C点的反应条件,不选择A、B点的理由分别是___________ 。
 .
. 的催化还原
的催化还原
(3) 催化剂能催化CO还原
催化剂能催化CO还原 ,反应为
,反应为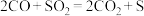 。将
。将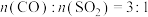 的混合气体(载气为
的混合气体(载气为 )匀速通过装有
)匀速通过装有 催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。
催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。___________ (填化学式)。
②谱峰4在活化前后也发生了一定变化,即部分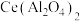 转变为
转变为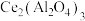 ,写出对应的化学反应方程式:
,写出对应的化学反应方程式:___________ 。
③实验中反应物的配比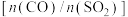 设定为3∶1而不是2∶1的可能原因是
设定为3∶1而不是2∶1的可能原因是___________ 。
 的捕集和利用具有重要意义。
的捕集和利用具有重要意义。 .
. 的催化氧化
的催化氧化(1)
 在
在 表面催化氧化的过程始于
表面催化氧化的过程始于 与
与 形成的酸性位点(如图所示),并生成金属硫酸盐(
形成的酸性位点(如图所示),并生成金属硫酸盐(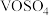 )中间体。
)中间体。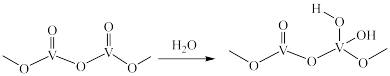
②写出中间体受热分解产生
 、
、 的化学方程式:
的化学方程式:(2)一定温度下,恒压密闭容器中发生反应
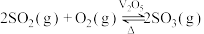
 ,
, 平衡转化率与反应温度和压强的关系如图所示。
平衡转化率与反应温度和压强的关系如图所示。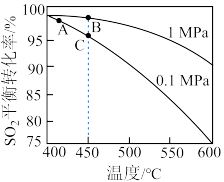

②实际生产中选择图中C点的反应条件,不选择A、B点的理由分别是
 .
. 的催化还原
的催化还原(3)
 催化剂能催化CO还原
催化剂能催化CO还原 ,反应为
,反应为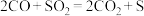 。将
。将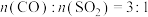 的混合气体(载气为
的混合气体(载气为 )匀速通过装有
)匀速通过装有 催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。
催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。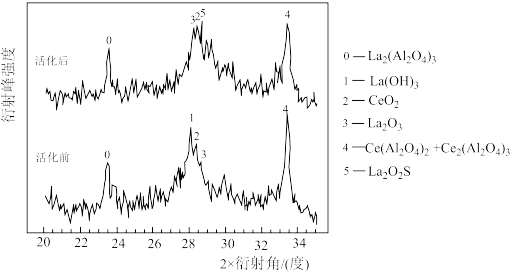
②谱峰4在活化前后也发生了一定变化,即部分
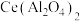 转变为
转变为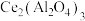 ,写出对应的化学反应方程式:
,写出对应的化学反应方程式:③实验中反应物的配比
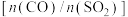 设定为3∶1而不是2∶1的可能原因是
设定为3∶1而不是2∶1的可能原因是
您最近半年使用:0次



