名校
解题方法
1 . 汽车尾气中含有CO、NO2等有毒气体,对汽车家装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
已知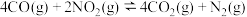
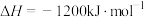
(1)该反应在___________ (填“高温、低温或任何温度”)下能自发进行。
(2)对于该反应,改变某一反应条件(温度 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。
(3)某实验小组模拟上述净化过程,一定温度下,在 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: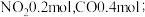 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。
① 的平衡体积分数:甲
的平衡体积分数:甲___________ 乙(填“>、=、<或不确定”,下同)。
② 的平衡浓度:甲
的平衡浓度:甲___________ 乙。
③甲中 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为___________ 。
已知
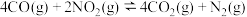
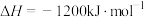
(1)该反应在
(2)对于该反应,改变某一反应条件(温度
 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。A.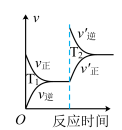 | B.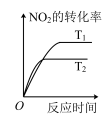 | C.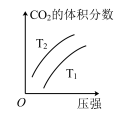 | D.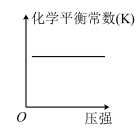 |
(3)某实验小组模拟上述净化过程,一定温度下,在
 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: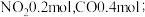 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。①
 的平衡体积分数:甲
的平衡体积分数:甲②
 的平衡浓度:甲
的平衡浓度:甲③甲中
 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为
您最近一年使用:0次
2 . 为了缓解温室效应与能源供应之间的冲突,从空气中捕集CO2并将其转化为燃料或增值化学品成为了新的研究热点,如甲醇的制备。回答下列问题:
I.制备合成气:反应 在工业上有重要应用。
在工业上有重要应用。
(1)该反应在不同温度下的平衡常数如表所示。
①反应的
___________ 0(填“>”“<”或“=”)。
②反应常在较高温度下进行,该措施的优缺点是___________ 。
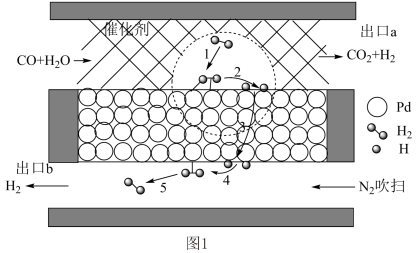
(2)该反应常在Pd膜反应器中进行,其工作原理如图1所示。___________ 。
Ⅱ.合成甲醇:在体积不变的密闭容器中投入 和
和 ,不同条件下发生反应:
,不同条件下发生反应: 。实验测得平衡时
。实验测得平衡时 的转化率随温度、压强的变化如图2所示。
的转化率随温度、压强的变化如图2所示。___________ (填“温度”或“压强”)。若图2中M点对应的容器体积为5L,则N点的平衡常数K为___________ 。
(4)图3中正确表示该反应的平衡常数的负对数 与X的关系的曲线
与X的关系的曲线___________ (填“AC”或“AB”)。 。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到
。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到 时刻达到平衡状态的是
时刻达到平衡状态的是___________ (填标号)。
I.制备合成气:反应
 在工业上有重要应用。
在工业上有重要应用。(1)该反应在不同温度下的平衡常数如表所示。
| 温度/℃ | 700 | 800 | 830 | 1000 |
| 平衡常数 | 1.67 | 1.11 | 1.00 | 0.59 |

②反应常在较高温度下进行,该措施的优缺点是
(2)该反应常在Pd膜反应器中进行,其工作原理如图1所示。
Ⅱ.合成甲醇:在体积不变的密闭容器中投入
 和
和 ,不同条件下发生反应:
,不同条件下发生反应: 。实验测得平衡时
。实验测得平衡时 的转化率随温度、压强的变化如图2所示。
的转化率随温度、压强的变化如图2所示。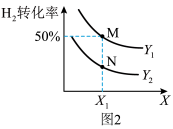
(4)图3中正确表示该反应的平衡常数的负对数
 与X的关系的曲线
与X的关系的曲线
 。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到
。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到 时刻达到平衡状态的是
时刻达到平衡状态的是a.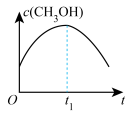 b.
b.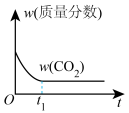 c.
c. 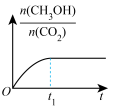 d.
d.
您最近一年使用:0次
3 . 回答下列问题。
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为
2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为___________ %。
(2)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g) 2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:
2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:
①写出化学平衡常数K的表达式___________ 。
②试比较K1、K2的大小,K1___________ K2(填“>”、“<”或“=”);
③400℃时,当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正___________ v(N2)逆(填“>”、“<”或“=”)。
(3)平衡后,若提高H2的转化率,可以采取的措施有___________。
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为
2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为(2)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)
 2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:
2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②试比较K1、K2的大小,K1
③400℃时,当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正
(3)平衡后,若提高H2的转化率,可以采取的措施有___________。
| A.加了催化剂 | B.增大容器体积 | C.降低反应体系的温度 | D.加入一定量N2 |
您最近一年使用:0次
名校
解题方法
4 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。___________ 。
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)=___________ 。
(3)2min反应达到平衡时体系内的压强比起始时的压强___________ (填增大、减小或无变化);平衡时混合气体密度和起始时相比___________ (填增大、减小或无变化)。
(4)下列说法正确的是___________。

(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)=
(3)2min反应达到平衡时体系内的压强比起始时的压强
(4)下列说法正确的是___________。
| A.使用催化剂不可以使化学平衡发生移动。 |
| B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢 |
| C.增大Y的浓度,正反应速率加快,逆反应速率减慢 |
| D.化学反应的限度是不可能改变的 |
您最近一年使用:0次
名校
5 . 已知反应:2NO2(g) N2O4(g),把NO2、N2O4的混合气体盛装在两个连通的烧瓶里,然后用夹子夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示。与常温时烧瓶内气体的颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅。下列说法错误的是
N2O4(g),把NO2、N2O4的混合气体盛装在两个连通的烧瓶里,然后用夹子夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示。与常温时烧瓶内气体的颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅。下列说法错误的是
 N2O4(g),把NO2、N2O4的混合气体盛装在两个连通的烧瓶里,然后用夹子夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示。与常温时烧瓶内气体的颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅。下列说法错误的是
N2O4(g),把NO2、N2O4的混合气体盛装在两个连通的烧瓶里,然后用夹子夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示。与常温时烧瓶内气体的颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅。下列说法错误的是
A.反应2NO2(g) N2O4(g)的正反应为吸热反应 N2O4(g)的正反应为吸热反应 |
| B.上述过程中,A烧瓶内正、逆反应速率均加快 |
| C.上述过程中,B烧瓶内c(NO2)减小,c(N2O4)增大 |
| D.上述过程中,A,B烧瓶内气体密度均保持不变 |
您最近一年使用:0次
名校
6 .  还原
还原 制
制 的反应体系中,主要发生反应的热化学方程式为
的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ

反应Ⅱ

在恒容密闭容器中,起始投入一定物质的量的 和
和 发生反应,平衡时
发生反应,平衡时 的转化率、产物
的转化率、产物 或CO其中之一的选择性[
或CO其中之一的选择性[ ]随温度变化如下图所示。下列说法正确的是
]随温度变化如下图所示。下列说法正确的是

 还原
还原 制
制 的反应体系中,主要发生反应的热化学方程式为
的反应体系中,主要发生反应的热化学方程式为反应Ⅰ


反应Ⅱ


在恒容密闭容器中,起始投入一定物质的量的
 和
和 发生反应,平衡时
发生反应,平衡时 的转化率、产物
的转化率、产物 或CO其中之一的选择性[
或CO其中之一的选择性[ ]随温度变化如下图所示。下列说法正确的是
]随温度变化如下图所示。下列说法正确的是
| A.图中曲线a表示CO的选择性 |
B.200~600℃时,温度越高,平衡时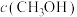 的浓度越小 的浓度越小 |
C.研究和使用在低温区高效的催化剂可提高制取 的产率 的产率 |
| D.高于600℃,反应Ⅱ的速率加快,反应Ⅰ的速率减慢 |
您最近一年使用:0次
名校
7 . 室温下,下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将两只装有NO2的玻璃球分别置于冷水和热水中 | 温度对化学平衡产生影响 |
| B | 向盛有淀粉、KI的溶液中滴加HNO3酸化的 溶液,振荡 溶液,振荡 | 比较Fe3+和I2的氧化性 |
| C | 用pH计分别测量等体积HCOOH和CH3COOH溶液的pH | 推电子基团对羧基酸性影响的比较 |
| D | 向溴水中滴加少量乙醇,振荡 | 比较Br2在水中和乙醇中溶解度的大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 在体积为1 L的恒温密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应: CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ,测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
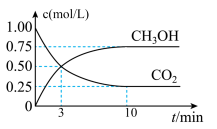
| A.该化学反应在3 min时达到平衡状态 |
| B.保持其他条件不变,降低温度,平衡时c(CH3OH)=0.85 mol·L-1,则该反应的ΔH >0 |
| C.相同温度下,起始时向上述容器中充入0.5 mol CO2、1.5 mol H2,平衡时CO2的转化率为75% |
| D.12 min时,向上述容器中再充入0.25 mol CO2、0.25 mol H2O(g),此时反应将向正反应方向进行 |
您最近一年使用:0次
2023-12-23更新
|
126次组卷
|
3卷引用:江苏省徐州市第七中学2023-2024学年高二下学期3月考试化学试题
名校
9 . 下列事实不能 用勒夏特列原理解释的是
| A.高压比常压更有利于合成氨反应 |
| B.红棕色的NO2气体,加压后颜色先变深后变浅,但比原来要深 |
| C.氯水在光照条件下颜色变浅,最终变为无色 |
| D.压缩H2和I2(g)反应的平衡混合气体,气体颜色变深 |
您最近一年使用:0次
2023-12-23更新
|
164次组卷
|
2卷引用:江苏省徐州市第七中学2023-2024学年高二下学期3月考试化学试题
名校
解题方法
10 . 在不同温度下,向 两个恒温、体积为
两个恒温、体积为 的恒容密闭容器中均通入
的恒容密闭容器中均通入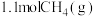 和
和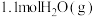 ,发生反应
,发生反应 。测得容器
。测得容器 中
中 物质的量、容器
物质的量、容器 中
中 物质的量随时间的变化曲线如图所示。下列说法正确的是
物质的量随时间的变化曲线如图所示。下列说法正确的是

 两个恒温、体积为
两个恒温、体积为 的恒容密闭容器中均通入
的恒容密闭容器中均通入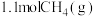 和
和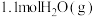 ,发生反应
,发生反应 。测得容器
。测得容器 中
中 物质的量、容器
物质的量、容器 中
中 物质的量随时间的变化曲线如图所示。下列说法正确的是
物质的量随时间的变化曲线如图所示。下列说法正确的是
A.反应 的 的 |
B. 容器前 容器前 用 用 表示的平均反应速率为 表示的平均反应速率为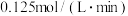 |
C.a容器达到平衡后,再充入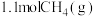 和 和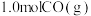 ,此时 ,此时 |
| D.两容器达到平衡时,b容器压强大于a容器压强 |
您最近一年使用:0次
2023-12-19更新
|
204次组卷
|
2卷引用: 江苏省徐州市第七中学2023-2024学年高三上学期1月月考化学试题



