1 . 某小组以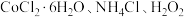 、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
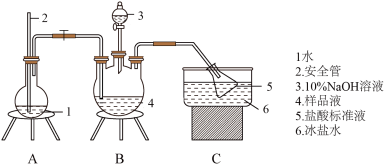
①氨的测定:准确称取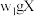 ,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量
,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量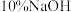 溶液,通入水蒸气,将样品液中的氨全部蒸出,用
溶液,通入水蒸气,将样品液中的氨全部蒸出,用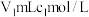 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用
的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用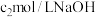 标准溶液滴定过剩的
标准溶液滴定过剩的 ,到终点时消耗
,到终点时消耗 溶液。
溶液。
②氯的测定:准确称取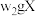 ,配成溶液后移取
,配成溶液后移取 于锥形瓶中,调
于锥形瓶中,调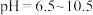 ,滴加指示剂
,滴加指示剂 溶液。在不断摇动下,用
溶液。在不断摇动下,用 标准溶液滴定至终点。(
标准溶液滴定至终点。( 为砖红色)
为砖红色)
回答下列问题:
(1)下列说法不正确 的是___________。
(2)滴定前,有关滴定管的正确操作为___________ (选出正确操作并按序排列)。
检漏→蒸馏水洗涤 开始滴定。
开始滴定。
A.烘干
B.装入滴定液至“0”刻度以上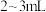 处
处
C.调整滴定液液面至“0”刻度或“0”刻度以下
D.用洗耳球吹出润洗液
E.排除气泡
F.用滴定液润洗2至3次
G.记录起始读数
(3)氯的测定过程中,滴定终点的现象是___________ 。当溶液中的 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中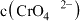 为
为___________  (保留两位有效数字)。已知
(保留两位有效数字)。已知 时,
时, 。
。
(4)测定 过程中,溶液
过程中,溶液 过低会使
过低会使 浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释
浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释 过低使
过低使 浓度降低的原因
浓度降低的原因___________ 。
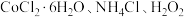 、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
①氨的测定:准确称取
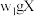 ,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量
,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量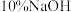 溶液,通入水蒸气,将样品液中的氨全部蒸出,用
溶液,通入水蒸气,将样品液中的氨全部蒸出,用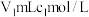 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用
的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用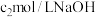 标准溶液滴定过剩的
标准溶液滴定过剩的 ,到终点时消耗
,到终点时消耗 溶液。
溶液。②氯的测定:准确称取
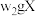 ,配成溶液后移取
,配成溶液后移取 于锥形瓶中,调
于锥形瓶中,调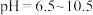 ,滴加指示剂
,滴加指示剂 溶液。在不断摇动下,用
溶液。在不断摇动下,用 标准溶液滴定至终点。(
标准溶液滴定至终点。( 为砖红色)
为砖红色)回答下列问题:
(1)下列说法
| A.安全管的作用是:当A中压力过大时,安全管中液面上升,使A瓶中压力稳定 |
| B.氨的测定过程中,滴定终点时仰视读数,氨的测定含量将偏高 |
| C.氨的测定接近终点时的“半滴操作”是:轻轻挤压玻璃珠下方的橡皮管,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁 |
| D.氯的测定过程中,使用棕色滴定管的原因是防止硝酸银见光分解 |
(2)滴定前,有关滴定管的正确操作为
检漏→蒸馏水洗涤
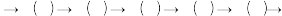 开始滴定。
开始滴定。A.烘干
B.装入滴定液至“0”刻度以上
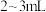 处
处C.调整滴定液液面至“0”刻度或“0”刻度以下
D.用洗耳球吹出润洗液
E.排除气泡
F.用滴定液润洗2至3次
G.记录起始读数
(3)氯的测定过程中,滴定终点的现象是
 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中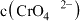 为
为 (保留两位有效数字)。已知
(保留两位有效数字)。已知 时,
时, 。
。(4)测定
 过程中,溶液
过程中,溶液 过低会使
过低会使 浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释
浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释 过低使
过低使 浓度降低的原因
浓度降低的原因
您最近一年使用:0次
2 . 关节炎首次发作一般在寒冷的季节,原因是关节滑液中形成了尿酸钠晶体( ),易诱发关节疼痛,其化学机理:①
),易诱发关节疼痛,其化学机理:①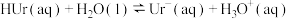 ;②
;②
 。下列叙述正确的是
。下列叙述正确的是
 ),易诱发关节疼痛,其化学机理:①
),易诱发关节疼痛,其化学机理:①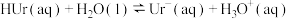 ;②
;②
 。下列叙述正确的是
。下列叙述正确的是| A.反应①是尿酸的水解方程式 |
B.反应②的 |
C.增大关节滑液中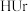 和 和 含量是治疗关节疼痛的方法之一 含量是治疗关节疼痛的方法之一 |
| D.关节保暖可以缓解疼痛,原理是平衡②逆向移动 |
您最近一年使用:0次
名校
3 . 实验室以二氧化铈( )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:
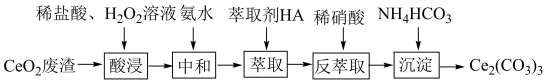
(1)“酸浸”时 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为___________
(2)pH约为7的 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,同时放出
沉淀,同时放出 ,该沉淀中
,该沉淀中 含量与加料方式有关。
含量与加料方式有关。
①得到含 量较少的
量较少的 的加料方式为
的加料方式为___________ (填序号)。
A.将 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中
② 溶液与
溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:___________
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是___________ 。
②反萃取的目的是将有机层 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有___________ 。
(4)实验中需要测定溶液中 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的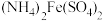 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取25.00 mL
。请补充完整实验方案:①准确量取25.00 mL  溶液[
溶液[ 约为
约为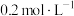 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将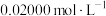
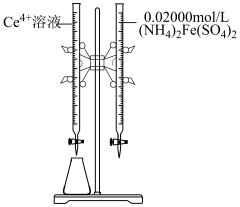
 和待测
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③___________
 )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:
(1)“酸浸”时
 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为(2)pH约为7的
 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,同时放出
沉淀,同时放出 ,该沉淀中
,该沉淀中 含量与加料方式有关。
含量与加料方式有关。①得到含
 量较少的
量较少的 的加料方式为
的加料方式为A.将
 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中②
 溶液与
溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:(3)通过中和、萃取、反萃取、沉淀等过程,可制备
 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是
②反萃取的目的是将有机层
 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有(4)实验中需要测定溶液中
 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的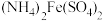 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取25.00 mL
。请补充完整实验方案:①准确量取25.00 mL  溶液[
溶液[ 约为
约为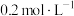 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将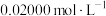
 和待测
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③
您最近一年使用:0次
4 . 一定温度时,恒容密闭容器中发生反应:2HI(g)⇌H2(g)+I2(g),达平衡充入HI(g)。下列说法错误的是
| A.平衡向正反应方向移动 | B.HI的分解率不变 |
| C.HI的百分含量不变 | D.气体颜色深浅不变 |
您最近一年使用:0次
名校
5 . 已知
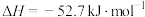 ,常温下N2O4为无色气体。
,常温下N2O4为无色气体。
(1)某课外活动小组为了探究压强对化学平衡的影响,设计了相关实验,请根据所学知识预测实验结果:在容积为30cm3针筒中抽入10cm3的NO2气体,将针筒前端封闭,静置一段时间至气体颜色不变。将针筒活塞拉至20cm3处,此时气体的颜色___________ (填“变深”、“变浅”或“不变”),一段时间后气体颜色___________ (填“变深”、“变浅”或“不变”),但仍比拉动活塞之前针筒内气体的颜色___________ (填“深”或“浅”)。在此过程中,该反应的化学平衡常数___________ (填“增大”、“减小”或“不变”),混合气体中NO2的百分含量___________ (填“增大”、“减小”或“不变”)。
(2)利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

①有关该过程说法正确的是___________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
②反应至B点时NO2的转化率为___________ 。
③图像中C、E两点气体平均摩尔质量较大的点为___________ (填代号)。
(3)某温度下,在体积恒为1 L的密闭容器内,起始时只加入1 mol NO2,达到平衡时其转化率为75%,则该温度下反应 的平衡常数
的平衡常数
___________ L⋅mol-1。

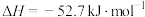 ,常温下N2O4为无色气体。
,常温下N2O4为无色气体。(1)某课外活动小组为了探究压强对化学平衡的影响,设计了相关实验,请根据所学知识预测实验结果:在容积为30cm3针筒中抽入10cm3的NO2气体,将针筒前端封闭,静置一段时间至气体颜色不变。将针筒活塞拉至20cm3处,此时气体的颜色
(2)利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

①有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
②反应至B点时NO2的转化率为
③图像中C、E两点气体平均摩尔质量较大的点为
(3)某温度下,在体积恒为1 L的密闭容器内,起始时只加入1 mol NO2,达到平衡时其转化率为75%,则该温度下反应
 的平衡常数
的平衡常数
您最近一年使用:0次
解题方法
6 . 一定条件下,利用R(g)制备M(g),反应为① ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示。下列说法正确的是
两个副反应,反应历程如图所示。下列说法正确的是
 ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示。下列说法正确的是
两个副反应,反应历程如图所示。下列说法正确的是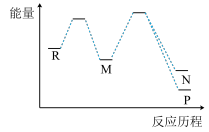
| A.反应③比反应①更快达到平衡 |
| B.温度越高,产物中M的纯度越高 |
| C.一定时间内,使用合适的催化剂可减少体系中P的含量 |
D.增大R的浓度,反应①②③的 增大, 增大, 减小 减小 |
您最近一年使用:0次
2023-12-02更新
|
431次组卷
|
4卷引用:广东省2024届普通高中毕业班高三上学期第二次调研考试化学试题
广东省2024届普通高中毕业班高三上学期第二次调研考试化学试题2024届广东省茂名市化州市高三上学期第二次调研考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)化学(广东卷01)-2024年高考押题预测卷
7 . 由 -羟基丁酸
-羟基丁酸 生成
生成 -丁内酯的反应如下:
-丁内酯的反应如下: 时,水溶液中
时,水溶液中 -羟基丁酸的初始浓度为
-羟基丁酸的初始浓度为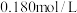 ,随着反应的进行,测得
,随着反应的进行,测得 -丁内酯的浓度随时间的变化如下表所示:
-丁内酯的浓度随时间的变化如下表所示:
下列说法不正确的是
 -羟基丁酸
-羟基丁酸 生成
生成 -丁内酯的反应如下:
-丁内酯的反应如下: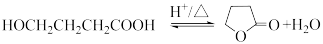
 时,水溶液中
时,水溶液中 -羟基丁酸的初始浓度为
-羟基丁酸的初始浓度为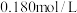 ,随着反应的进行,测得
,随着反应的进行,测得 -丁内酯的浓度随时间的变化如下表所示:
-丁内酯的浓度随时间的变化如下表所示: | 21 | 50 | 80 | 100 | 120 | 160 | 220 |  |
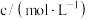 | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
A.在50~80 内,以 内,以 -丁内酯的浓度变化表示的反应速率为 -丁内酯的浓度变化表示的反应速率为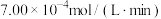 |
B.在 时,该反应的平衡常数 时,该反应的平衡常数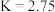 |
C.若将 -羟基丁酸的初始浓度降低,体系中水含量增多,平衡逆向移动, -羟基丁酸的初始浓度降低,体系中水含量增多,平衡逆向移动, -羟基丁酸的平衡转化率减小 -羟基丁酸的平衡转化率减小 |
D.将反应溶剂更换为非水溶剂并通过共沸回流的方式移除体系中的水分,有助于提高 -丁内酯的平衡产率 -丁内酯的平衡产率 |
您最近一年使用:0次
名校
8 . 在一恒容密闭容器中,反应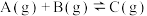 达到平衡,若增大A的浓度,使平衡右移,并达到新的平衡,下列说法正确的是
达到平衡,若增大A的浓度,使平衡右移,并达到新的平衡,下列说法正确的是
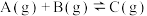 达到平衡,若增大A的浓度,使平衡右移,并达到新的平衡,下列说法正确的是
达到平衡,若增大A的浓度,使平衡右移,并达到新的平衡,下列说法正确的是| A.A的浓度一定比原平衡大 |
| B.A的转化率增大 |
| C.C的百分含量一定大于原平衡C的百分含量 |
D.该反应的 增大 增大 |
您最近一年使用:0次
9 . 反应 ,反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
,反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是

 ,反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
,反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
| A.达到平衡后,若降温,平衡向右移动 |
| B.达到平衡后,加入催化剂,B%减小 |
| C.达到平衡后,加入物质C,平衡向左移,C%减小 |
| D.达到平衡后,加入物质A,正反应速率增大,逆反应速率减小 |
您最近一年使用:0次
名校
10 . (NH4)2Cr2O7用于有机合成催化剂,媒染剂,显影液等。某化学兴趣小组对(NH4)2Cr2O7的部分性质及含氮量进行探究。已知: (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+,回答下列问题:
(黄色)+2H+,回答下列问题:
(1)在试管中加入少量固体(NH4)2Cr2O7,滴加足量浓KOH溶液,振荡、微热,观察到的主要现象是固体溶解、有刺激性气味气体放出、___________ 。
(2)实验室常用甲醛法测定含(NH4)2Cr2O7的样品中氮的质量分数,其反应原理为:2Ba2++ +H2O=2BaCrO4↓+2H+;4
+H2O=2BaCrO4↓+2H+;4 +6HCHO=3H++6H2O+(CH2)6N4H+;(CH2)6N4H+
+6HCHO=3H++6H2O+(CH2)6N4H+;(CH2)6N4H+ (CH2)6N4+H+,K=7×10-6,然后用NaOH标准溶液滴定反应生成的酸和酸性物质。
(CH2)6N4+H+,K=7×10-6,然后用NaOH标准溶液滴定反应生成的酸和酸性物质。
实验步骤:
ⅰ.称取样品mg,配成250mL溶液。
ⅱ.量取25.00mL样品溶液,用氯化钡溶液使 完全沉淀后,加入10mL20%的中性甲醛溶液,摇匀、静置5min。
完全沉淀后,加入10mL20%的中性甲醛溶液,摇匀、静置5min。
ⅲ.以酚酞作指示剂,用cmol·L-1标准NaOH溶液滴定,记录数据。
ⅳ.重复步骤ⅱ、ⅲ 2-3次,处理数据。
①滴定终点的现象是___________ 。
②滴定操作使用的玻璃仪器主要有___________ 。
③滴定时边滴边摇动锥形瓶,眼睛应观察___________ 。
④步骤ⅲ发生反应的离子方程式是H++OH-= H2O和___________ 。
⑤若实验平均消耗NaOH溶液的体积为vmL,该样品中氮的质量分数的计算式为___________ 。(用含m、c、v式子表示,需要化简)
⑥下列情况会导致测定结果偏低的是___________ 。(填序号)
a. 若步骤ⅰ中定容时俯视溶液液面
b. 若实验中使用的甲醛常混有微量甲酸
c. 若步骤ⅱ没有静置5min
d. 若实验时装NaOH标准液的滴定管只用蒸馏水洗涤而未用标准液润洗
 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+,回答下列问题:
(黄色)+2H+,回答下列问题:(1)在试管中加入少量固体(NH4)2Cr2O7,滴加足量浓KOH溶液,振荡、微热,观察到的主要现象是固体溶解、有刺激性气味气体放出、
(2)实验室常用甲醛法测定含(NH4)2Cr2O7的样品中氮的质量分数,其反应原理为:2Ba2++
 +H2O=2BaCrO4↓+2H+;4
+H2O=2BaCrO4↓+2H+;4 +6HCHO=3H++6H2O+(CH2)6N4H+;(CH2)6N4H+
+6HCHO=3H++6H2O+(CH2)6N4H+;(CH2)6N4H+ (CH2)6N4+H+,K=7×10-6,然后用NaOH标准溶液滴定反应生成的酸和酸性物质。
(CH2)6N4+H+,K=7×10-6,然后用NaOH标准溶液滴定反应生成的酸和酸性物质。实验步骤:
ⅰ.称取样品mg,配成250mL溶液。
ⅱ.量取25.00mL样品溶液,用氯化钡溶液使
 完全沉淀后,加入10mL20%的中性甲醛溶液,摇匀、静置5min。
完全沉淀后,加入10mL20%的中性甲醛溶液,摇匀、静置5min。ⅲ.以酚酞作指示剂,用cmol·L-1标准NaOH溶液滴定,记录数据。
ⅳ.重复步骤ⅱ、ⅲ 2-3次,处理数据。
①滴定终点的现象是
②滴定操作使用的玻璃仪器主要有
③滴定时边滴边摇动锥形瓶,眼睛应观察
④步骤ⅲ发生反应的离子方程式是H++OH-= H2O和
⑤若实验平均消耗NaOH溶液的体积为vmL,该样品中氮的质量分数的计算式为
⑥下列情况会导致测定结果偏低的是
a. 若步骤ⅰ中定容时俯视溶液液面
b. 若实验中使用的甲醛常混有微量甲酸
c. 若步骤ⅱ没有静置5min
d. 若实验时装NaOH标准液的滴定管只用蒸馏水洗涤而未用标准液润洗
您最近一年使用:0次



