解题方法
1 . 回答下列问题。
(1)工业合成氨的反应: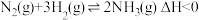 ,分别在
,分别在 、
、 温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
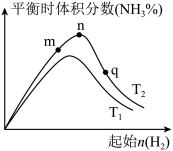
①比较在m、n、q三点所处的平衡状态中,反应物 的转化率最高的是
的转化率最高的是___________ 点。
② 条件下,在
条件下,在 的密闭容器中,充入
的密闭容器中,充入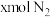 和
和 时,
时, 达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):
达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):
___________ ;该反应的平衡常数的值
___________ 。
③图像中
___________  (填“高于”、“低于”、“等于”或“无法确定”)。
(填“高于”、“低于”、“等于”或“无法确定”)。
(2)一定温度下,在密闭容器中将等物质的量的 和
和 混合,采用适当的催化剂进行反应
混合,采用适当的催化剂进行反应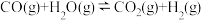 ,已知此温度下,该反应的平衡常数
,已知此温度下,该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数为
的物质的量分数为___________  。
。
(1)工业合成氨的反应:
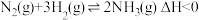 ,分别在
,分别在 、
、 温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
①比较在m、n、q三点所处的平衡状态中,反应物
 的转化率最高的是
的转化率最高的是②
 条件下,在
条件下,在 的密闭容器中,充入
的密闭容器中,充入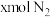 和
和 时,
时, 达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):
达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):

③图像中

 (填“高于”、“低于”、“等于”或“无法确定”)。
(填“高于”、“低于”、“等于”或“无法确定”)。(2)一定温度下,在密闭容器中将等物质的量的
 和
和 混合,采用适当的催化剂进行反应
混合,采用适当的催化剂进行反应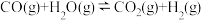 ,已知此温度下,该反应的平衡常数
,已知此温度下,该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数为
的物质的量分数为 。
。
您最近半年使用:0次
2 . 下列事实不能 用勒夏特列原理来解释的是
| A.实验室中常用排饱和食盐水的方法收集Cl2 |
| B.鼓入过量空气有利于SO2转化为SO3 |
| C.开启啤酒瓶后,压强变小,瓶中立刻泛起大量泡沫 |
| D.煅烧硫铁矿时先将矿石粉碎 |
您最近半年使用:0次
3 . 下列过程中的颜色变化不能用勒夏特列原理解释的是
A.向5mL0.1mol•L-1重铬酸钾溶液中(存在平衡: (橙色)+H2O⇌2 (橙色)+H2O⇌2 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 |
| B.对2NO2(g)⇌N2O4(g)平衡体系增大压强(缩小体积)的瞬间,气体的颜色变深 |
| C.将NO2球浸泡在热水中,红棕色变深 |
| D.溴水中有平衡:Br2+H2O⇌HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅 |
您最近半年使用:0次
名校
解题方法
4 . 下列说法不正确的是
A.向 溶液中加入稀硫酸,溶液颜色由橙色变为黄色 溶液中加入稀硫酸,溶液颜色由橙色变为黄色 |
| B.中和滴定实验中,锥形瓶用水洗涤后,不能用待测液润洗 |
| C.中和反应反应热测定实验中,一组完整实验数据需要测温度3次 |
D.配制 溶液时,应将 溶液时,应将 固体溶于较浓的盐酸中,再加水稀释到所需浓度 固体溶于较浓的盐酸中,再加水稀释到所需浓度 |
您最近半年使用:0次
名校
5 . 下列事实能用勒夏特列原理解释的是
A.氯水中存在平衡: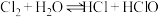 ,当加入 ,当加入 溶液后,溶液颜色变浅 溶液后,溶液颜色变浅 |
B.对 反应,减小体积使压强增大混合气体颜色变深 反应,减小体积使压强增大混合气体颜色变深 |
| C.合成氨中用铁触媒作催化剂提高氨的单位时间产量 |
| D.升高温度有利于合成氨 |
您最近半年使用:0次
解题方法
6 . K2Cr2O7溶液中存在平衡: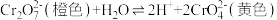 。
。
(1)向2mL0.1mol/LK2Cr2O7溶液中滴加5滴6mol/LNaOH溶液。可观察到的现象是_______ ;得出的结论是:_______ 。
(2)向上述溶液中再滴加10滴6mol/LH2SO4溶液。可观察到的现象是_______ ;得出的结论是_______ 。
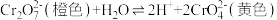 。
。(1)向2mL0.1mol/LK2Cr2O7溶液中滴加5滴6mol/LNaOH溶液。可观察到的现象是
(2)向上述溶液中再滴加10滴6mol/LH2SO4溶液。可观察到的现象是
您最近半年使用:0次
7 . 用尿素水解生成的NH3催化还原NO,是柴油机车辆尾气净化的主要方法。反应为 ,达到平衡后,再通入一定量O2,达到新平衡时,下列说法不正确的是
,达到平衡后,再通入一定量O2,达到新平衡时,下列说法不正确的是
 ,达到平衡后,再通入一定量O2,达到新平衡时,下列说法不正确的是
,达到平衡后,再通入一定量O2,达到新平衡时,下列说法不正确的是| A.N2的平衡浓度增大 | B.NO的转化率增大 |
| C.正向反应速率增大 | D.反应平衡常数增大 |
您最近半年使用:0次
名校
8 . 下述反应可制备特种陶瓷的原料MgO:MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
 MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是| A.恒温时,增大压强平衡逆向移动,平衡常数减小 |
| B.容积不变时,升高温度,混合气体的平均相对分子质量减小 |
| C.恒温恒容时,分离出部分CO2气体可提高MgSO4的转化率 |
D.恒温恒容时,冲入CO气体,达到新平衡时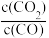 增大 增大 |
您最近半年使用:0次
9 . 探究外界因素对化学平衡的影响
Ⅰ. 利用“[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O ΔH > 0”探究温度和浓度对化学平衡的影响。
[CuCl4]2-(黄色)+4H2O ΔH > 0”探究温度和浓度对化学平衡的影响。
实验过程:常温下,将CuCl2溶于水中得到CuCl2浓溶液,获得黄绿色溶液。并平均分为5份置于5个试管中并标记为a、b、c、d、e号试管
(1)b号试管的实验现象为________ ,c号试管相对于a号试管来说,c的溶液由黄绿色变为________ (填“蓝”或“黄”)色。对比a、b、c三支试管颜色变化,得到的结论是________________ 。
(2)对比a、d、e三支试管颜色变化,得到的结论是________ 。
Ⅱ.利用2N2O5(g) 4NO2(g) +O2(g)探究压强对化学平衡的影响。(已知:N2O5是一种无色气体)
4NO2(g) +O2(g)探究压强对化学平衡的影响。(已知:N2O5是一种无色气体)
在初始体积为V 的、无色透明的、带有活塞的石英玻璃容器中充入一定量N2O5,将温度升到一定温度并保持不变使其充分反应,如下图所示。
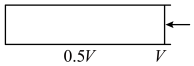
(3)待反应充分反应后,将容器的容积压缩为0.5V,可以观察到“混合气体颜色先快速变深,然后缓慢变浅”,说明该反应的平衡________ (填“正向”、“逆向”或“不”)移动;再将容积扩大到V,可以观察到“混合气体颜色先快速变浅,然后缓慢加深”,说明该反应的平衡________ (填“正向”、“逆向”或“不”)移动;
(4)通过上述实验,压强对化学平衡的影响是:________ 。
Ⅰ. 利用“[Cu(H2O)4]2+(蓝色)+4Cl-
 [CuCl4]2-(黄色)+4H2O ΔH > 0”探究温度和浓度对化学平衡的影响。
[CuCl4]2-(黄色)+4H2O ΔH > 0”探究温度和浓度对化学平衡的影响。实验过程:常温下,将CuCl2溶于水中得到CuCl2浓溶液,获得黄绿色溶液。并平均分为5份置于5个试管中并标记为a、b、c、d、e号试管
| 试管编号 | 处理方式 |
| a | 加入1ml 的水 |
| b | 加入1mL 0.1mol·L-1 AgNO3溶液(足量)充分反应 |
| c | 加入1ml 0.1mol·L-1 NaCl溶液(足量)充分反应 |
| d | 加入1mL 的水 并置于50℃的热水浴中充分反应 |
| e | 加入1mL 的水 并置于冰水浴中充分反应 |
(1)b号试管的实验现象为
(2)对比a、d、e三支试管颜色变化,得到的结论是
Ⅱ.利用2N2O5(g)
 4NO2(g) +O2(g)探究压强对化学平衡的影响。(已知:N2O5是一种无色气体)
4NO2(g) +O2(g)探究压强对化学平衡的影响。(已知:N2O5是一种无色气体)在初始体积为V 的、无色透明的、带有活塞的石英玻璃容器中充入一定量N2O5,将温度升到一定温度并保持不变使其充分反应,如下图所示。

(3)待反应充分反应后,将容器的容积压缩为0.5V,可以观察到“混合气体颜色先快速变深,然后缓慢变浅”,说明该反应的平衡
(4)通过上述实验,压强对化学平衡的影响是:
您最近半年使用:0次
10 .  溶液中存在平衡:
溶液中存在平衡: ,加入下列物质能够使溶液橙色明显加深的是
,加入下列物质能够使溶液橙色明显加深的是
 溶液中存在平衡:
溶液中存在平衡: ,加入下列物质能够使溶液橙色明显加深的是
,加入下列物质能够使溶液橙色明显加深的是| A.3~5滴浓硫酸 | B.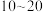 滴浓 滴浓 溶液 溶液 |
| C.1mLC2H5OH | D.1mLH2O |
您最近半年使用:0次



