名校
解题方法
1 . 如图所示为工业合成氨的流程图。下列说法错误的是


| A.步骤①中“净化”可以防止催化剂中毒 |
| B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率 |
| C.步骤③、④、⑤均有利于提高原料平衡的转化率 |
| D.为保持足够高的原料转化率,应在反应达到一定时间时将氨从混合气中分离出去 |
您最近半年使用:0次
2021-10-12更新
|
374次组卷
|
10卷引用:山东省菏泽市2020-2021学年高二上学期期中考试化学试题(A)
山东省菏泽市2020-2021学年高二上学期期中考试化学试题(A)黑龙江省大庆中学2021-2022学年高二上学期第一次月考化学试题重庆市育才中学校2021-2022学年高二上学期第一次月考化学试题重庆市永川景圣中学校2021-2022学年高二上学期第一次月考化学试题天津市第二十一中学2021-2022学年高二上学期期中检测化学试题天津市咸水沽第二中学2021-2022学年高二上学期期中化学试题安徽省滁州市定远县育才学校2021-2022学年高二(实验班)上学期第三次月考化学试题陕西省渭南市临渭区华州区2021-2022学年高二上学期期末考试化学试题陕西省汉中市乡县第一中学2023-2024学年高二上学期10月月考化学试题新疆乌鲁木齐市第八中学2023-2024学年高二上学期期中考试化学试题
2 . 已知反应C(s)+H2O(g) CO(g)+H2(g) ΔH>0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
CO(g)+H2(g) ΔH>0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
 CO(g)+H2(g) ΔH>0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
CO(g)+H2(g) ΔH>0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是| A.升高温度,平衡向逆反应方向移动 |
| B.增大H2的浓度,平衡向逆向移动 |
| C.更换高效催化剂,CO平衡转化率增大 |
| D.减小压强,c(CO)减小 |
您最近半年使用:0次
2021-10-09更新
|
107次组卷
|
2卷引用:云南省楚雄师范学院附属中学2020-2021学年高二上学期期中考试化学试题
3 . 锶(Sr)位于元素周期表的第5周期IIA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。完成下列填空:
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是______ 。非金属性最强的是______ 。
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式______ ,该分子为______ (选填“极性”、“非极性”)分子。
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号______ 。写出锶原子的最外层电子排布式______ 。下列关于锶及其化合物的叙述中,错误的是______ 。
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(4)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因______ 。
钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO 3Ba↑+BaO+Al2O3。
3Ba↑+BaO+Al2O3。
(5)常温下Al的金属性比Ba的金属性______ (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是______ 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(4)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因
钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO
 3Ba↑+BaO+Al2O3。
3Ba↑+BaO+Al2O3。(5)常温下Al的金属性比Ba的金属性
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
您最近半年使用:0次
名校
4 . 反应mA(s)+nB(g)⇌pC(g)+qD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示,下列叙述正确的是


| A.达到平衡后,加入催化剂,C%增大 |
| B.达到平衡后,若升温,平衡向左移动 |
| C.化学方程式中n<p+q |
| D.达到平衡后,增加A的量有利于平衡向右移动 |
您最近半年使用:0次
2021-09-30更新
|
566次组卷
|
8卷引用:陕西省千阳中学2020-2021学年高二上学期期中化学(理科)试题
陕西省千阳中学2020-2021学年高二上学期期中化学(理科)试题重庆市暨华中学校2021-2022学年高二上学期第一次月考化学试题天津市武清区崔黄口中学2021-2022学年高二上学期第一次练习化学试题湖北省武汉市江夏实验高级中学2021-2022学年高二上学期10月考试化学试题广西贺州市昭平县昭平中学2021-2022学年高二上学期第二次月考化学试题青海省西宁市大通回族土族自治县2021-2022学年高二上学期期末考试化学试题(已下线)第13讲 第二章《化学反应速率与化学平衡》单元测试(基础巩固)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)专题05 影响化学平衡的因素【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
名校
解题方法
5 . 硫酸铜在工农业生产中有着广泛的应用,用某种氧化铜矿制备硫酸铜的工艺流程如图:

(1)浸出时所用硫酸的质量浓度(单位体积的溶液所含溶质的质量)为29.4g·L-1,溶液密度约为1.2g/cm3,则溶液中溶质的质量分数为______ 。(请保留一位小数)
(2)萃取“相比”是表示萃取效果的参数之一,指的是有机相(O)与水相(A)的体积比。采用一定浓度的铜萃取剂萃取硫酸浸出液中的铜离子,测得当萃取时间为120s时,“相比”(O/A)对铜萃取率的影响如图所示。在实际操作中“相比”应选择______ 。(填序号)
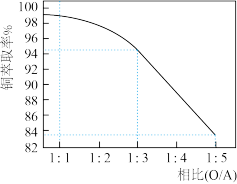
A.1:1 B.1:3 C.1:5
(3)已知铜萃取剂可用HR(O)表示,萃取过程可表示为:Cu2++2HR(O)⇌CuR2(O)+2H+,反萃取加入400 g·L-1硫酸的理由是______ 。
(4)游泳场馆常用硫酸铜作杀菌剂,这是利用了CuSO4的_______ 性质。

(1)浸出时所用硫酸的质量浓度(单位体积的溶液所含溶质的质量)为29.4g·L-1,溶液密度约为1.2g/cm3,则溶液中溶质的质量分数为
(2)萃取“相比”是表示萃取效果的参数之一,指的是有机相(O)与水相(A)的体积比。采用一定浓度的铜萃取剂萃取硫酸浸出液中的铜离子,测得当萃取时间为120s时,“相比”(O/A)对铜萃取率的影响如图所示。在实际操作中“相比”应选择

A.1:1 B.1:3 C.1:5
(3)已知铜萃取剂可用HR(O)表示,萃取过程可表示为:Cu2++2HR(O)⇌CuR2(O)+2H+,反萃取加入400 g·L-1硫酸的理由是
(4)游泳场馆常用硫酸铜作杀菌剂,这是利用了CuSO4的
您最近半年使用:0次
名校
解题方法
6 . 下列说法不正确的是
| A.NH3的熔、沸点比ⅤA族其他元素氢化物的都高 |
| B.向碘的四氯化碳溶液中加入浓的KI溶液,溶液紫色会变浅 |
| C.尿素(CO(NH2)2)的熔、沸点比醋酸的高 |
| D.含1 mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生2 mol白色沉淀 |
您最近半年使用:0次
2021-09-26更新
|
158次组卷
|
3卷引用:四川省内江市第六中学2020-2021学年高二上学期期中考试化学试题
11-12高二上·海南·期末
7 . 如图是关于反应A2(g)+3B2(g)⇌2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是


| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
您最近半年使用:0次
2021-09-02更新
|
868次组卷
|
52卷引用:2010—2011学年海南省洋浦中学高二上学期期末考试化学试卷
(已下线)2010—2011学年海南省洋浦中学高二上学期期末考试化学试卷(已下线)2011-2012年吉林省长春外国语学校高二上学期第一次月考化学试卷(已下线)2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷(已下线)2011-2012学年贵州省凯里一中高二上学期期中考试化学试卷(已下线)2011-2012学年云南蒙自高中高二上学期期中考试化学试卷(已下线)2012-2013学年安徽省舒城晓天中学高二上学期第一次月考化学试卷(已下线)2012-2013学年浙江省宁海县正学中学高二下学期第一次阶段性测试化学试卷(已下线)2012-2013学年山东省临沭一中高二10月学情调查化学试卷(已下线)2014年高二化学人教版选修四 8化学平衡移动练习卷(已下线)2013-2014四川省雅安中学下学期期中考试高二化学试卷(已下线)2011-2012贵州省凯里一中第一学期期末考试高二化学试卷(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2014-2015学年湖北省部分重点中学高二上学期期中考试化学试卷(已下线)2014秋河北省唐山一中高二上学期期中化学试卷(已下线)2014-2015学年辽宁师范大学附中高二10月模考化学试卷2015届吉林省东北师大附中高三上学期第三次摸底化学试卷2014-2015学年山东省微山一中高二下学期期末考试化学试卷2015-2016学年河北省成安一中高二上学期10月月考化学试卷2015-2016学年江苏省海安实验中学高二上学期期中选修化学试卷2015-2016学年四川省成都市六校高二上学期期中联考化学试卷2015-2016学年山东省泰安市高二上学期期末考试化学试卷2016-2017学年贵州省安顺平坝第一高级中学高二上期中化学卷2016-2017学年浙江省余姚中学高二上期中化学试卷安徽省六安市第一中学2017-2018学年高二上学期开学考试化学试题河北省定州中学2017-2018学年高二上学期开学考试化学试题河南省林州市第一中学分校(林虑中学)2017-2018学年高二上学期开学检测化学试题河北省深州中学2016-2017学年高二下学期期末考试化学试题云南省姚安县第一中学2017-2018学年高二10月月考化学试题河北省故城县高级中学2018届高三12月月考化学试题甘肃省武威市第十八中2018-2019学年高二上学期第一次月考化学试题【区级联考】山东省济南市莱芜区2019届高三第一学期期末质量检测化学试题步步为赢 高二化学寒假作业:作业五 化学平衡的图像分析2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷黑龙江桦南二中2019-2020学年高二上学期期中考试化学试题天津市和平区2018-2019高二期末考试化学试题黑龙江省海林市朝鲜族中学2020-2021学年高二上学期第一次月考化学试题江苏省宿迁市沭阳县潼阳中学2020-2021学年高二下学期第一次月考化学试题山西省运城市稷山中学2022届高三上学期月考(一)化学试题(已下线)第19讲 化学平衡 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省长沙市周南中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)考向22 化学平衡状态 化学平衡的移动-备战2022年高考化学一轮复习考点微专题(已下线)章末培优2 专题2 化学反应速率与化学平衡-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)湖南省怀化市第五中学2021-2022学年高二上学期期中考试化学试题云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题(已下线)第6章 化学反应速率和化学平衡复习-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)上海市嘉定区第一中学2021-2022学年高一下学期期期末考试化学试题(已下线)第19讲 化学平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省武威市凉州区2020-2021学年高二上学期期末考试化学试题浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题新疆乌鲁木齐八一中学2023-2024学年高二上学期11月期中化学试题
8 . 某密闭容器中放入一定量的NO2,发生反应2NO2(g)⇌N2O4(g)+Q,在达平衡后,若分别单独改变下列条件,重新达到平衡后,能使平衡混合气体平均相对分子质量减小的是
| A.通入N2 | B.通入NO2 | C.通入N2O4 | D.降低温度 |
您最近半年使用:0次
名校
9 . 一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2molSO2、1molO2 | 4molSO3 | 2molSO2、1molO2 |
| 平衡v正(SO2)/mol/(L·s) | v1 | v2 | v3 |
| 平衡c(SO3)mol/L | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率/α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c2<2c1 | B.K1>K3,p2>2p3 |
| C.v1>v3,α1(SO2)>α3(SO2) | D.c2>2c3,α2(SO3)+α3(SO2)<1 |
您最近半年使用:0次
2021-08-14更新
|
1544次组卷
|
25卷引用:天津市静海区第一中学2020届高三下学期第六周周末训练化学试题
天津市静海区第一中学2020届高三下学期第六周周末训练化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 高考帮人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 过高考 3年真题强化闯关浙江省诸暨市2019-2020学年高二上学期期末考试化学试题宁夏银川一中2020-2021学年高二上学期期末考试化学试题浙江省宁波市九校2020-2021学年高二上学期期末联考化学试题(已下线)【绍兴新东方】绍兴高中化学00008(已下线)【浙江新东方】高中化学20210304-010(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)四川省蓬安中学校2019-2020学年高二上学期开学考试化学试题(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题广西浦北中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2.3.2 压强变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)吉林省长春市第二中学2021-2022学年高二上学期第一次月考化学试题江西省吉安一中2021-2022学年高二上学期第一次段考化学试题江西省九江市第一中学2021-2022学年高二上学期期中考试化学试题江西省宜春市八校2022-2023学年高二上学期12月联考化学试题河北省部分学校2023-2024学年高二上学期10月联考化学试题安徽省当涂第一中学2023-2024学年高二上学期10月月考化学试题
10 . 常温下,在饱和氯水中,化学反应为:Cl2+H2O⇌HCl+HClO。下列说法正确的是
| A.当溶液pH不变时,该反应一定达到平衡状态 |
| B.向该溶液中加水,平衡向正反应移动,K一定增大 |
| C.向该溶液中通入Cl2,平衡一定向正反应方向移动 |
| D.光照条件下HCl浓度增大,平衡一定向逆反应方向移动 |
您最近半年使用:0次



