1 . 向两个体积可变的密闭容器中均充入1mol的A和2mol的B,发生反应:A2(g)+2B2(g)⇌2AB2(g)ΔH.维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2的体积分数随温度的变化如图所示。
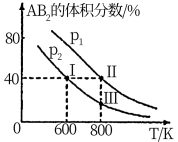
已知:①图中I、II、III点均处于曲线上;②点II时容器的体积为0.1L。下列叙述正确的是

已知:①图中I、II、III点均处于曲线上;②点II时容器的体积为0.1L。下列叙述正确的是
| A.由图象可知:p1<p2 ΔH<0 |
| B.点I时A2的平衡转化率为40% |
| C.点III所对应的反应平衡常数K=0.2 |
| D.将点II所对应的容器冷却到600K,不可能变成点I |
您最近一年使用:0次
名校
解题方法
2 . 苯乙烯是石油化学工业的重要原料之一。世界上90%以上的苯乙烯是采用乙苯催化脱氢法制得。具体反应为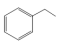 (g)
(g)
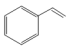 (g)+H2(g) ∆H=+124kJ/mol。
(g)+H2(g) ∆H=+124kJ/mol。
(1)相关物质的相对能量如表所示:
则苯乙烯(g)的相对能量为___ kJ•mol-1。
(2)工业上通常在乙苯蒸气中掺入水蒸气(物质的量之比为1:9),控制反应温度625℃,在等压(p)下进行上述反应,达到平衡时乙苯的转化率为α。
①掺入水蒸气能提高乙苯的平衡转化率,其原因是___ 。
②该温度下,反应的平衡常数Kp=__ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)乙苯催化脱氢制备苯乙烯时,通常会伴随着副反应发生,其中一个反应为 (g)+H2(g)
(g)+H2(g)
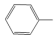 +CH4(g)。该反应的速率方程为r=k×c乙苯×c氢气,其中r为瞬时速率,k为反应速率常数,c乙苯和c氢气分别为乙苯和氢气的物质的量浓度。某温度下,向恒容密闭容器中充入等物质的量的乙苯和氢气,发生上述反应。
+CH4(g)。该反应的速率方程为r=k×c乙苯×c氢气,其中r为瞬时速率,k为反应速率常数,c乙苯和c氢气分别为乙苯和氢气的物质的量浓度。某温度下,向恒容密闭容器中充入等物质的量的乙苯和氢气,发生上述反应。
①对于该反应,下列说法正确的是____ 。
A.降低乙苯的浓度时,r减小
B.降低甲苯的浓度时,r减小
C.升高反应温度,k增大
D.达到平衡前,甲烷的生成速率逐渐增大
②设反应开始时的反应速率为r0,达到平衡之前,乙苯的转化率为α时的反应速率为r1,则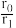 =
=___ 。
(4)含苯乙烯的废水排放会对环境造成严重污染,目前常采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水,pH=6.2)。已知:•OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。.
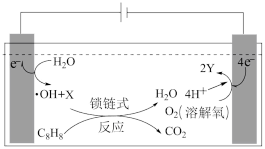
阴极反应式为____ ,X微粒的化学式为____ 。
 (g)
(g)
 (g)+H2(g) ∆H=+124kJ/mol。
(g)+H2(g) ∆H=+124kJ/mol。(1)相关物质的相对能量如表所示:
| 物质 | 乙苯(g) | H2(g) |
| 相对能量/(kJ•mol-1) | a | 0 |
(2)工业上通常在乙苯蒸气中掺入水蒸气(物质的量之比为1:9),控制反应温度625℃,在等压(p)下进行上述反应,达到平衡时乙苯的转化率为α。
①掺入水蒸气能提高乙苯的平衡转化率,其原因是
②该温度下,反应的平衡常数Kp=
(3)乙苯催化脱氢制备苯乙烯时,通常会伴随着副反应发生,其中一个反应为
 (g)+H2(g)
(g)+H2(g)
 +CH4(g)。该反应的速率方程为r=k×c乙苯×c氢气,其中r为瞬时速率,k为反应速率常数,c乙苯和c氢气分别为乙苯和氢气的物质的量浓度。某温度下,向恒容密闭容器中充入等物质的量的乙苯和氢气,发生上述反应。
+CH4(g)。该反应的速率方程为r=k×c乙苯×c氢气,其中r为瞬时速率,k为反应速率常数,c乙苯和c氢气分别为乙苯和氢气的物质的量浓度。某温度下,向恒容密闭容器中充入等物质的量的乙苯和氢气,发生上述反应。①对于该反应,下列说法正确的是
A.降低乙苯的浓度时,r减小
B.降低甲苯的浓度时,r减小
C.升高反应温度,k增大
D.达到平衡前,甲烷的生成速率逐渐增大
②设反应开始时的反应速率为r0,达到平衡之前,乙苯的转化率为α时的反应速率为r1,则
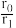 =
=(4)含苯乙烯的废水排放会对环境造成严重污染,目前常采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水,pH=6.2)。已知:•OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。.

阴极反应式为
您最近一年使用:0次
解题方法
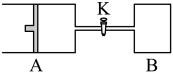
3 . 如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和催化剂的条件下,两容器中各自发生下列反应
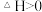 ;达到平衡时,VA=1.2aL,则下列说法不正确的是
;达到平衡时,VA=1.2aL,则下列说法不正确的是

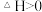 ;达到平衡时,VA=1.2aL,则下列说法不正确的是
;达到平衡时,VA=1.2aL,则下列说法不正确的是
| A.反应开始时,B容器中化学反应速率快 |
| B.A容器中X的转化率为40%,且比B容器中X的转化率大 |
| C.打开K一段时间达平衡时,A的体积为2.4aL(连通管中气体体积不计) |
| D.打开K达新平衡后,升高B容器温度,A容器体积会增大 |
您最近一年使用:0次
2021-02-07更新
|
315次组卷
|
5卷引用:【浙江新东方】高中化学20210304-010
(已下线)【浙江新东方】高中化学20210304-010浙江省宁波市九校2020-2021学年高二上学期期末联考化学试题(已下线)【绍兴新东方】绍兴高中化学00008(已下线)期中考试模拟试题(一)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)四川省成都金苹果锦城第一中学2023-2024学年高二上学期期中考试化学试题
4 . 为减少碳氧化物的排放,工业上可回收 和
和 合成甲醇(
合成甲醇( )。
)。
(1)利用 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:
反应Ⅰ
反应Ⅱ
控制 和
和 初始投料比为
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
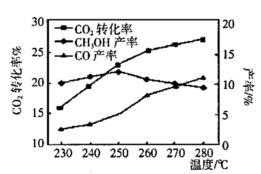
①反应Ⅰ能自发的反应条件:______ 。(填“低温”、“高温”、“任何温度”)
②由图可知温度升高 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是______ 。
③由图可知获取 最适宜的温度是
最适宜的温度是______ 。
④控制 和
和 初始投料比为
初始投料比为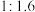 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为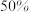 ,甲醇选择性为
,甲醇选择性为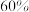 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是______ 。(甲醇的选择性:转化的 中生成甲醇的百分比)
中生成甲醇的百分比)
(2)利用 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:
反应Ⅲ
其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是______ 。
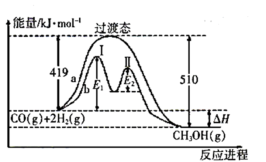
A. 上述反应的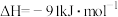
B. 反应正反应的活化能为
反应正反应的活化能为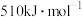
C. 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D. 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E. 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入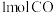 和
和 ,向乙中加入
,向乙中加入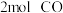 和
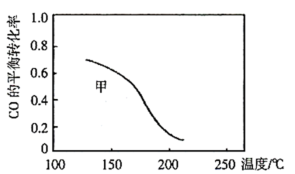
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线______ 。
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式______ 。
 和
和 合成甲醇(
合成甲醇( )。
)。(1)利用
 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:反应Ⅰ

反应Ⅱ

控制
 和
和 初始投料比为
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
①反应Ⅰ能自发的反应条件:
②由图可知温度升高
 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是③由图可知获取
 最适宜的温度是
最适宜的温度是④控制
 和
和 初始投料比为
初始投料比为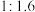 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为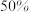 ,甲醇选择性为
,甲醇选择性为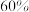 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是 中生成甲醇的百分比)
中生成甲醇的百分比)(2)利用
 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:反应Ⅲ

其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是

A. 上述反应的
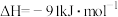
B.
 反应正反应的活化能为
反应正反应的活化能为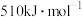
C.
 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应D.
 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E.
 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入
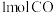 和
和 ,向乙中加入
,向乙中加入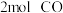 和
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式
您最近一年使用:0次
名校
解题方法
5 . 利用辉钼矿冶炼组的原理为
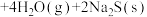
 。在压强为
。在压强为 的条件下,测得达到平衡时的有关气体体积分数的变化如图中实线所示:
的条件下,测得达到平衡时的有关气体体积分数的变化如图中实线所示:

下列判断正确的是

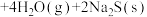
 。在压强为
。在压强为 的条件下,测得达到平衡时的有关气体体积分数的变化如图中实线所示:
的条件下,测得达到平衡时的有关气体体积分数的变化如图中实线所示:
下列判断正确的是
A.通过图象曲线变化规律无法判断 正负 正负 |
| B.a为CO变化曲线,b为水蒸气变化曲线 |
C.压强为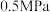 时,虚线Ⅱ可能为 时,虚线Ⅱ可能为 的变化曲线 的变化曲线 |
D.M点 的转化率为75% 的转化率为75% |
您最近一年使用:0次
2021-01-26更新
|
660次组卷
|
8卷引用:重庆市缙云教育联盟2021-2022学年高三9月月度质量检测化学试题
重庆市缙云教育联盟2021-2022学年高三9月月度质量检测化学试题吉林省长春市十一高中2022届高三上学期第一学程考试化学试题湖南省攸县长鸿实验中学2022-2023学年高三第四次月考化学试题(已下线)解密09 化学反应速率与平衡(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)课时38 化学平衡常规图像-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第4讲 化学反应速率及平衡图像山西省运城市2020-2021学年高二上学期期末考试化学试题
名校
6 . 一定温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl5 (g)  PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是
 PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是| 容器编号 | 物质的起始浓度/(mol·L-1) | 物质的平衡浓度/(mol·L-1) | ||
 | 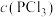 | 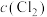 | 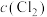 | |
| Ⅰ | 0.4 | 0 | 0 | 0.2 |
| Ⅱ | 0.6 | 0 | 0.2 | |
| Ⅲ | 0.8 | 0 | 0 | |
A.反应达到平衡时,容器I中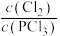 比容器Ⅱ中的小 比容器Ⅱ中的小 |
| B.反应达到平衡时,容器I与容器Ⅱ中的总压强之比为3︰4 |
C.反应达到平衡时,容器Ⅲ中 的体积分数小于 的体积分数小于 |
| D.反应达到平衡时,容器Ⅲ中0.4mol/L<c(PCl5)<0.8 mol/L |
您最近一年使用:0次
2020-09-29更新
|
725次组卷
|
6卷引用:江西省赣州市会昌县七校2021届高三联合9月月考化学试题
12-13高三上·黑龙江·阶段练习
名校
解题方法
7 . 如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2 mol SO2和l mol O2,乙中充入4 mol SO3和1 mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3 (g) ⇌ 2SO2 (g) + O2 (g)。下列有关说法正确的是


| A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强:P乙=P甲 |
| B.若活塞固定在3处不动,达平衡时甲乙两容器中SO3的浓度:c (SO3) 乙>2c (SO3)甲 |
| C.若活塞固定在3处不动,达平衡时甲乙容两器中SO2的体积分数:ψ (SO2)乙>2ψ (SO2)甲 |
| D.若活塞固定在7处不动,达平衡时两容器中SO2的物质的量分数相等 |
您最近一年使用:0次
2020-09-16更新
|
579次组卷
|
7卷引用:2013届黑龙江省哈三中高三10月月考化学试卷
(已下线)2013届黑龙江省哈三中高三10月月考化学试卷2016届黑龙江省哈尔滨三中高三上学期第二次检测化学试卷黑龙江省哈尔滨市第三中学2019-2020学年高二10月月考化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一次阶段考试化学试题(已下线)2012-2013学年黑龙江省哈三中高二上学期期中考试化学试卷浙江省浙北G2(湖州中学、嘉兴一中)2021-2022学年高二上学期期中联考化学试题内蒙古赤峰市红山区2021-2022学年高二上学期期末联考化学试题
名校
解题方法
8 . 运用化学链燃烧技术有利于提高燃料利用率。化学链燃烧技术的基本原理是借助载氧剂(如Fe2O3、FeO等)将燃料与空气直接接触的传统燃烧反应分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
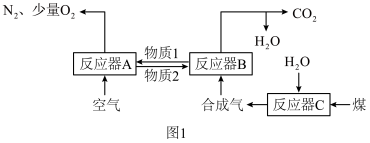
以Fe2O3作载氧剂的化学链燃烧循环转化反应的部分热化学方程式如下,循环转化的原理如图1所示。
①C(s)+H2O(g)═CO(g)+H2(g)△H1=akJ•mol﹣1
②CO(g)+H2(g)+O2(g)═CO2(g)+H2O(g)△H2=bkJ•mol﹣1
(1)写出图1中总反应的热化学方程式:_____
(2)空气经反应器A后得到的尾气_____ (填“能”或“不能”)直接用作工业合成氨的原料气,原因是_____ 。
Ⅱ.用FeO作载氧剂,部分反应的lgKp[K是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]与温度的关系如图2所示。
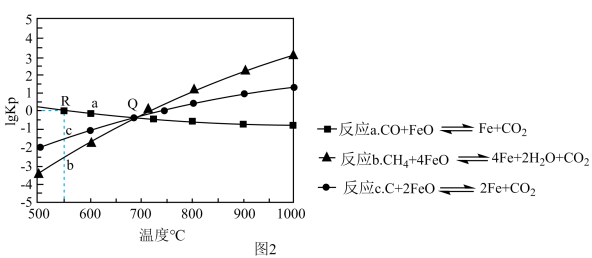
(3)图2涉及的反应中,属于吸热反应的是反应_____ (填字母)。
(4)R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应CO(g)+FeO(s)⇌Fe(s)+CO2(g),则CO的平衡转化率为_____ 。
Ⅲ.在T℃下,向某恒容密闭容器中加入1mol CH4(g)和4mol FeO(s)进行反应:CH4(g)+4FeO(s)⇌4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
(5)T℃下,该反应的Kp=_____ 。
(6)若起始时向该容器中加入1mol CH4(g),4mol FeO(s),1mol H2O(g),0.5mol CO2(g),此时反应向_____ (填“正反应”或“逆反应”)方向进行。
(7)其他条件不变,若将该容器改为恒压密闭容器,则此时CH4(g)的平衡转化率_____ (填“增大”“减小”或“不变”)。

以Fe2O3作载氧剂的化学链燃烧循环转化反应的部分热化学方程式如下,循环转化的原理如图1所示。
①C(s)+H2O(g)═CO(g)+H2(g)△H1=akJ•mol﹣1
②CO(g)+H2(g)+O2(g)═CO2(g)+H2O(g)△H2=bkJ•mol﹣1
(1)写出图1中总反应的热化学方程式:
(2)空气经反应器A后得到的尾气
Ⅱ.用FeO作载氧剂,部分反应的lgKp[K是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]与温度的关系如图2所示。

(3)图2涉及的反应中,属于吸热反应的是反应
(4)R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应CO(g)+FeO(s)⇌Fe(s)+CO2(g),则CO的平衡转化率为
Ⅲ.在T℃下,向某恒容密闭容器中加入1mol CH4(g)和4mol FeO(s)进行反应:CH4(g)+4FeO(s)⇌4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
(5)T℃下,该反应的Kp=
(6)若起始时向该容器中加入1mol CH4(g),4mol FeO(s),1mol H2O(g),0.5mol CO2(g),此时反应向
(7)其他条件不变,若将该容器改为恒压密闭容器,则此时CH4(g)的平衡转化率
您最近一年使用:0次
2020-07-23更新
|
292次组卷
|
5卷引用:云南省昆明市第一中学2020届高三上学期12月月考理综试卷化学试题
名校
9 . 已知反应:2NO2(红棕色)  N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
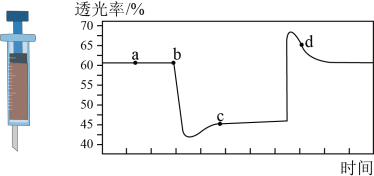
 N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
| A.b点的操作是压缩注射器 |
| B.d 点:v正>v逆 |
| C.c点与a点相比,c(NO2)增大,c(N2O4)减小 |
| D.若不忽略体系温度变化,且没有能量损失,则Tb>Tc |
您最近一年使用:0次
2020-04-30更新
|
836次组卷
|
15卷引用:2015届北京市海淀区高三年级3月适应性训练理综化学试卷
2015届北京市海淀区高三年级3月适应性训练理综化学试卷2015届福建省漳州市高三5月适应性考试化学试卷安徽省涡阳县第一中学2019-2020学年高二12月月考化学试题内蒙古自治区赤峰二中2020-2021学年高二上学期第一次月考化学试题重庆市大足中学2022-2023学年高二上学期学期第一次月考化学试题四川省华蓥中学2023-2024学年高二上学期9月月考化学试题2016-2017学年安徽省师大附中高二上期中化学试卷河北省唐山遵化市2019-2020学年高二上学期期中考试化学试题甘肃省兰州市第一中学2019-2020学年高二上学期期末考试化学试题北京师范大学第二附属中学未来科技城学校2021-2022学年高二上学期期中考试化学试题江西省崇义中学2020-2021学年高一上学期期中考试(A卷)化学试题湖南师范大学附属中学2022-2023学年高一下学期期末考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期开学考试化学试题北京市第一七一中学2023-2024学年高二上学期期中考试化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题
10 . 为了减轻大气污染,可在汽车尾气排放处加装“催化净化器”装置。
(1)通过“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的化学方程式:__ 。
(2)在一定温度下,向1L密闭恒容容器中充入1molNO、2molCO,发生上述反应,10s时反应达到平衡,此时CO的物质的量为1.2mol。请回答下列问题:
①前10s内平均反应速率v(CO)=___ 。
②在该温度下反应的平衡常数K=___ 。
③关于上述反应,下列叙述正确的是___ (填字母)。
A.达到平衡时,移走部分CO2,平衡将向右移动,正反应速率加快
B.扩大容器的体积,平衡将向右移动
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度不变,再向容器中充入0.8molCO和0.4molN2,则此时v正>v逆
④已知上述实验中,c(CO)与反应时间t变化曲线Ⅰ如图:
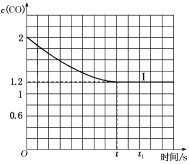
若其他条件不变,将1molNO、2molCO投入2L容器进行反应,请在图中绘出c(CO)与反应时间t1变化曲线Ⅱ___ (不要求标出CO的终点坐标)。
(3)测试某汽车冷启动时的尾气催化处理,CO、NO百分含量随时间变化曲线如图:
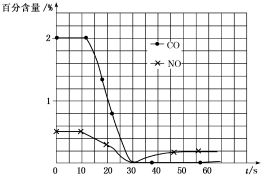
请回答:
前0~10s阶段,CO、NO百分含量没明显变化的原因是___ 。
(1)通过“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的化学方程式:
(2)在一定温度下,向1L密闭恒容容器中充入1molNO、2molCO,发生上述反应,10s时反应达到平衡,此时CO的物质的量为1.2mol。请回答下列问题:
①前10s内平均反应速率v(CO)=
②在该温度下反应的平衡常数K=
③关于上述反应,下列叙述正确的是
A.达到平衡时,移走部分CO2,平衡将向右移动,正反应速率加快
B.扩大容器的体积,平衡将向右移动
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度不变,再向容器中充入0.8molCO和0.4molN2,则此时v正>v逆
④已知上述实验中,c(CO)与反应时间t变化曲线Ⅰ如图:

若其他条件不变,将1molNO、2molCO投入2L容器进行反应,请在图中绘出c(CO)与反应时间t1变化曲线Ⅱ
(3)测试某汽车冷启动时的尾气催化处理,CO、NO百分含量随时间变化曲线如图:

请回答:
前0~10s阶段,CO、NO百分含量没明显变化的原因是
您最近一年使用:0次



