1 .  可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 制备
制备 的原理如下:
的原理如下:
反应1:
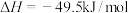
反应2:
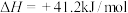 (副反应)
(副反应)
(1) ,该反应的
,该反应的
___________  。
。
(2)将 和
和 按
按 通入密闭容器中发生反应1和反应2,分别在
通入密闭容器中发生反应1和反应2,分别在 、
、 、
、 下改变反应温度,测得
下改变反应温度,测得 的平衡转化率(
的平衡转化率( )以及生成
)以及生成 、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。
、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。 下
下 随温度变化趋势的是曲线
随温度变化趋势的是曲线___________ (填“a”“b”或“c”)。
②随着温度升高,a、b、c三条曲线接近重合的原因是___________ 。
③P点对应的反应2的平衡常数
___________ (保留两位有效数字)。
④分子筛膜反应器可提高反应1的平衡转化率、且实现 选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是
选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是___________ 。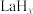 ,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
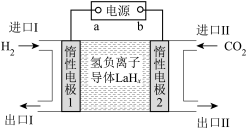
①电极a为电源的___________ (填“正极”或“负极”)。
②生成 的电极反应式为
的电极反应式为___________ 。
③若反应2也同时发生,出口Ⅱ为CO、 、
、 的混合气,且
的混合气,且 ,则惰性电极2的电流效率
,则惰性电极2的电流效率 为
为___________ (
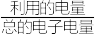 ×100%)。
×100%)。
 可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 制备
制备 的原理如下:
的原理如下:反应1:

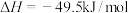
反应2:

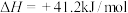 (副反应)
(副反应)(1)
 ,该反应的
,该反应的
 。
。(2)将
 和
和 按
按 通入密闭容器中发生反应1和反应2,分别在
通入密闭容器中发生反应1和反应2,分别在 、
、 、
、 下改变反应温度,测得
下改变反应温度,测得 的平衡转化率(
的平衡转化率( )以及生成
)以及生成 、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。
、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。
 下
下 随温度变化趋势的是曲线
随温度变化趋势的是曲线②随着温度升高,a、b、c三条曲线接近重合的原因是
③P点对应的反应2的平衡常数

④分子筛膜反应器可提高反应1的平衡转化率、且实现
 选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是
选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是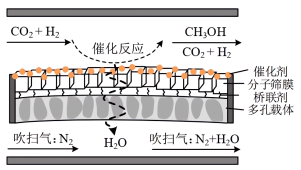
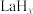 ,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
①电极a为电源的
②生成
 的电极反应式为
的电极反应式为③若反应2也同时发生,出口Ⅱ为CO、
 、
、 的混合气,且
的混合气,且 ,则惰性电极2的电流效率
,则惰性电极2的电流效率 为
为
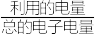 ×100%)。
×100%)。
您最近一年使用:0次
2023-06-03更新
|
704次组卷
|
5卷引用:湖南省宁乡市实验中学等多校联考2024届高三下学期一轮复习总结性考试(月考)化学试题
湖南省宁乡市实验中学等多校联考2024届高三下学期一轮复习总结性考试(月考)化学试题重庆市巴蜀中学校2023学年高三模拟预测化学试题(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)广西名校2023-2024学年高三上学期仿真卷(一)化学试题湖南省长沙市雅礼中学2023-2024学年高三上学期1月期末化学试题
名校
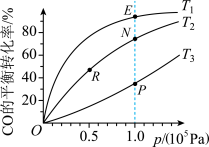
2 . 用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g) CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
 CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
| A.温度:T1>T2>T3 |
| B.正反应速率:v(E)>v(P)、v(N)>v(R) |
| C.平衡常数:K(E)>K(P)、K(N)>K(R) |
| D.平均摩尔质量:M(E)>M(P)、M(N)>M(R) |
您最近一年使用:0次
2023-04-11更新
|
693次组卷
|
3卷引用:河南省焦作市博爱县第一中学2022-2023学年高三下学期5月月考化学试题
名校
解题方法
3 . 在恒压密闭容器中,充入起始量一定的 和
和 ,主要发生下列反应:
,主要发生下列反应:


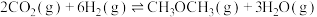
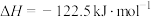
达平衡时, 转化率和CO的选择性
转化率和CO的选择性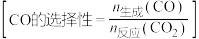 随温度的变化如图所示,下列说法不正确的是
随温度的变化如图所示,下列说法不正确的是
 和
和 ,主要发生下列反应:
,主要发生下列反应:

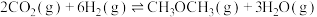
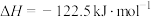
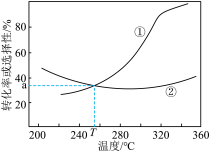
达平衡时,
 转化率和CO的选择性
转化率和CO的选择性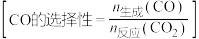 随温度的变化如图所示,下列说法不正确的是
随温度的变化如图所示,下列说法不正确的是
| A.图中曲线①表示平衡时CO的选择性随温度的变化 |
B.温度一定,通过增大压强能提高 的平衡产率 的平衡产率 |
C.一定温度下,增大 ,能提高 ,能提高 平衡转化率 平衡转化率 |
D.T℃时,起始投入2 mol 、6 mol 、6 mol ,达平衡时生成 ,达平衡时生成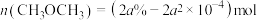 |
您最近一年使用:0次
2023-04-04更新
|
521次组卷
|
3卷引用:湖南省长沙市湖南师大附中2023届高考模拟(一)化学试题
名校
解题方法
4 . CH4和CO2联合重整能减少温室气体的排放。其主要反应为:
①CH4(g)+CO2(g) 2H2(g)+2CO(g)
2H2(g)+2CO(g)
②H2(g)+CO2(g) H2O(g)+CO(g)
H2O(g)+CO(g)
其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。
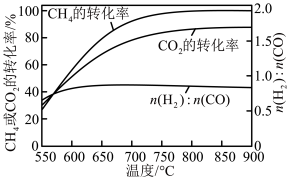
下列说法不正确 的是
①CH4(g)+CO2(g)
 2H2(g)+2CO(g)
2H2(g)+2CO(g)②H2(g)+CO2(g)
 H2O(g)+CO(g)
H2O(g)+CO(g)其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。

下列说法
| A.550~600℃,升温更有利于反应①,反应①先达到平衡 |
| B.n(H2)∶n(CO)始终低于1.0,与反应②有关 |
| C.加压有利于增大CH4和CO2反应的速率但不利于提高二者的平衡转化率 |
| D.若不考虑其他副反应,体系中存在:4[c(CH4)+c(CO)+c(CO2)]=2.3[4c(CH4)+2c(H2)+2c(H2O)] |
您最近一年使用:0次
2023-03-31更新
|
1567次组卷
|
12卷引用:北京市第一○一中学2023-2024学年高三上学期10月月考化学试题
北京市第一○一中学2023-2024学年高三上学期10月月考化学试题北京市清华大学附属中学2023-2024学年高三上学期12月统练(六)化学试题北京市第八中学2023-2024学年高三上学期12月月考化学试题北京市西城区2023届一模考试化学试题(已下线)专题15 化学反应速率和化学平衡(已下线)化学-2023年高考押题预测卷03(江苏卷)(含考试版、全解全析、参考答案、答题卡)江苏省南京师范大学附属中学2023届高三下学期5月模拟考试化学试题北京师范大学附属中学2023-2024学年高三上学期期中考试化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(二)化学试题安徽省淮北市第一中学2023-2024学年高二上学期第三次月考化学试题北京市十一学校2022-2023学年高二下学期期末考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题
名校
解题方法
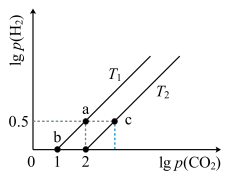
5 . 已知CH4(g)+CO2(g) 2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
 2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
A.a点时对应的Kp= (MPa) (MPa) |
| B.T1>T2 |
| C.c点对应的p(CO2)=1000MPa |
| D.当容器中CH4与CO的压强比为1∶2时,不能说明该反应达平衡状态 |
您最近一年使用:0次
2023-03-20更新
|
484次组卷
|
3卷引用:重庆市巴蜀中学校2023届高三适应性月考卷(七)化学试题
名校
6 . 氮的氧化物既是空气的主要污染物,也是重要的化工原料。回答下列问题:
(1)已知
Ⅰ、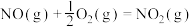 ,
,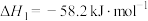 ;
;
Ⅱ、 ,
,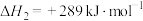 。
。
则反应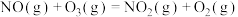 的△H=
的△H=___________ 。又知 ,反应机理为
,反应机理为 (快反应),
(快反应), (慢反应),则活化能较小的是反应是
(慢反应),则活化能较小的是反应是___________ (填“快反应”或“慢反应”)。
(2)若用 、
、 分别表示正、逆反应的速率常数(只受温度影响),反应
分别表示正、逆反应的速率常数(只受温度影响),反应 △H<0的
△H<0的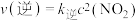 ,
, ,则该反应的正反应速率v(正)、
,则该反应的正反应速率v(正)、 、反应物浓度之间的关系式为
、反应物浓度之间的关系式为___________ 。
(3)在不同压强下,向某恒容密闭容器中通入初始浓度为2
 、6
、6 NO,使其发生反应
NO,使其发生反应
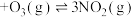 ,
,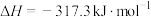 ,测得平衡时
,测得平衡时 的体积百分含量随着温度、压强变化情况如图所示:
的体积百分含量随着温度、压强变化情况如图所示:
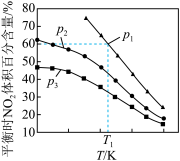
① 、
、 、
、 由大到小的顺序为
由大到小的顺序为___________ ,为提高NO的转化率,可采取的措施是___________ (写两点)。
②若 、
、 时,反应开始到达到平衡的时间为10s,则此阶段中
时,反应开始到达到平衡的时间为10s,则此阶段中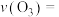
___________ (用分数表示),平衡常数
___________ 。
(1)已知
Ⅰ、
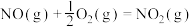 ,
,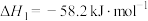 ;
;Ⅱ、
 ,
,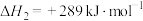 。
。则反应
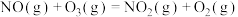 的△H=
的△H= ,反应机理为
,反应机理为 (快反应),
(快反应), (慢反应),则活化能较小的是反应是
(慢反应),则活化能较小的是反应是(2)若用
 、
、 分别表示正、逆反应的速率常数(只受温度影响),反应
分别表示正、逆反应的速率常数(只受温度影响),反应 △H<0的
△H<0的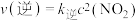 ,
, ,则该反应的正反应速率v(正)、
,则该反应的正反应速率v(正)、 、反应物浓度之间的关系式为
、反应物浓度之间的关系式为(3)在不同压强下,向某恒容密闭容器中通入初始浓度为2

 、6
、6 NO,使其发生反应
NO,使其发生反应
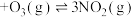 ,
,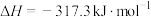 ,测得平衡时
,测得平衡时 的体积百分含量随着温度、压强变化情况如图所示:
的体积百分含量随着温度、压强变化情况如图所示:
①
 、
、 、
、 由大到小的顺序为
由大到小的顺序为②若
 、
、 时,反应开始到达到平衡的时间为10s,则此阶段中
时,反应开始到达到平衡的时间为10s,则此阶段中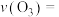

您最近一年使用:0次
名校
解题方法
7 . 随着我国“碳达峰”、“碳中和”目标的确定,二氧化碳资源化利用倍受关注。
Ⅰ.以 和
和 为原料合成尿素:
为原料合成尿素: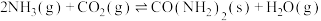
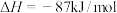 。
。
(1)有利于提高 平衡转化率的措施是_______(填标号)。
平衡转化率的措施是_______(填标号)。
(2)研究发现,合成尿素反应分两步完成,其能量变化如图甲所示。
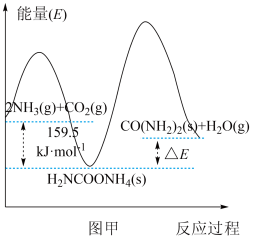
第一步: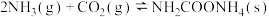

第二步: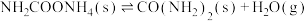

反应速率较快的是反应_______ (填“第一步”或“第二步”)。
Ⅱ.以和催化重整制备合成气: 。
。
(3)在密闭容器中通入物质的量均为0.2mol的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应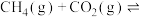
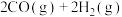 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示:
的平衡转化率随温度、压强的变化关系如图乙所示:
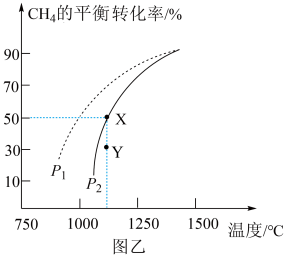
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是_______ (填标号)。
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率: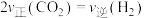 D.同时断裂2mol C—H和1mol H—H
D.同时断裂2mol C—H和1mol H—H
②由图乙可知,压强
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则X点对应温度下的
,则X点对应温度下的
_______ (用含 的代数式表示)。
的代数式表示)。
Ⅲ.电化学法还原二氧化碳制乙烯。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应为_______ ;该装置中使用的是_______ (填“阳”或“阴”)离子交换膜。
Ⅰ.以
 和
和 为原料合成尿素:
为原料合成尿素: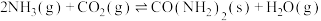
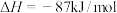 。
。(1)有利于提高
 平衡转化率的措施是_______(填标号)。
平衡转化率的措施是_______(填标号)。| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |

第一步:
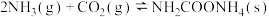

第二步:
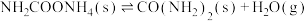

反应速率较快的是反应
Ⅱ.以和催化重整制备合成气:
 。
。(3)在密闭容器中通入物质的量均为0.2mol的
 和
和 ,在一定条件下发生反应
,在一定条件下发生反应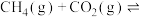
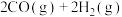 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示:
的平衡转化率随温度、压强的变化关系如图乙所示:
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率:
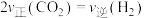 D.同时断裂2mol C—H和1mol H—H
D.同时断裂2mol C—H和1mol H—H②由图乙可知,压强

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ,则X点对应温度下的
,则X点对应温度下的
 的代数式表示)。
的代数式表示)。Ⅲ.电化学法还原二氧化碳制乙烯。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应为
您最近一年使用:0次
2023-02-06更新
|
342次组卷
|
2卷引用:湖南省长沙市雅礼中学2022-2023学年高三下学期月考卷(六)化学试题
2023高三·全国·专题练习
解题方法
8 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)
_______  。
。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为_______ mol﹒L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为_______ 。
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2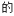 平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
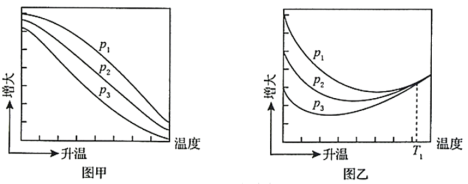
已知:CO2的平衡转化率=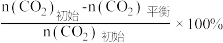
CH3OH的平衡产率=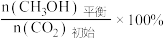
其中纵坐标表示CO2平衡转化率的是图_______ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为_______ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_______ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_______(填标号)。
Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:
(1)

 。
。(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2
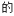 平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知:CO2的平衡转化率=
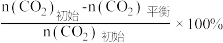
CH3OH的平衡产率=
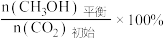
其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_______(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
2023-01-31更新
|
549次组卷
|
4卷引用:山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题
山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题(已下线)专题09 化学反应速率与化学平衡(测)-2023年高考化学二轮复习讲练测(新高考专用)广东北江实验学校2023—2024学年高二上学期10月月考化学试题(已下线)化学反应速率与化学平衡——课时5影响化学平衡的因素
名校
解题方法
9 . 氙的氟化物是优良的氟化剂,稀有气体Xe和F2混合在催化剂作用下同时存在如下反应:
反应I:
反应Ⅱ: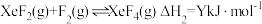
反应Ⅲ: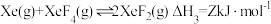
已知:XeF2选择性是指生成XeF2所消耗的Xe的物质的量与初始Xe的物质的量的比值。
回答下列问题:
(1)向刚性密闭容器中加入n mol的Xe和4mol的F2,初始压强为106Pa,测得在相同时间内,上述反应Xe的转化率和XeF2的选择性与温度的关系如图1所示,则制取XeF2的最适宜温度为_______ ;当超过1000℃,XeF2选择性随着温度升高而降低的可能原因是_______ 。
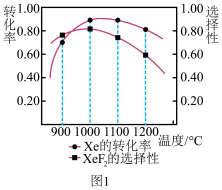
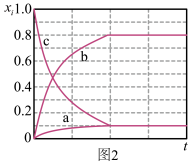
(2)在1000℃时,初始条件同上,xi表示含Xe元素的某物质与含Xe元素各物质的总物质的量之比,xi随时间t变化关系如图2所示。测得平衡时XeF2的选择性为80%,图2中表示XeF4变化的曲线是_______ ,则反应过程能量变化为_______ kJ(用含X、Y的代数式表示),F2的转化率为_______ ,反应I以物质的量分数表示的平衡常数Kx=_______ 。
(3)在1000℃时,反应Ⅲ的平衡常数Kp=_______ ,保持初始其他条件不变,反应达平衡后增大体系压强,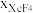 的变化趋势为
的变化趋势为_______ (填“增大”“减小”或“不变”)。
反应I:

反应Ⅱ:
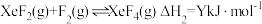
反应Ⅲ:
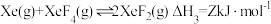
已知:XeF2选择性是指生成XeF2所消耗的Xe的物质的量与初始Xe的物质的量的比值。
回答下列问题:
(1)向刚性密闭容器中加入n mol的Xe和4mol的F2,初始压强为106Pa,测得在相同时间内,上述反应Xe的转化率和XeF2的选择性与温度的关系如图1所示,则制取XeF2的最适宜温度为

(2)在1000℃时,初始条件同上,xi表示含Xe元素的某物质与含Xe元素各物质的总物质的量之比,xi随时间t变化关系如图2所示。测得平衡时XeF2的选择性为80%,图2中表示XeF4变化的曲线是

(3)在1000℃时,反应Ⅲ的平衡常数Kp=
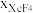 的变化趋势为
的变化趋势为
您最近一年使用:0次
2023-01-15更新
|
531次组卷
|
3卷引用:山东省德州市第一中学2023-2024学年高三上学期1月月考化学试题
山东省德州市第一中学2023-2024学年高三上学期1月月考化学试题山东省潍坊市2022-2023学年高三上学期期末考试化学试题(已下线)化学-2023年高考押题预测卷01(山东卷)(含考试版、全解全析、参考答案、答题卡)
10 . 甲醇是重要的化上原料,研究甲醇的制备及用途在工业上有重要的意义。回答下列问题:
(1)一种重要的工业制备甲醇的反应为
 。
。
已知:①

②
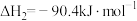
该制备反应的
______ 。升高温度,该制备反应的 的平衡转化率
的平衡转化率______ (填“增大”“减小”或“不变”)。
(2)已知反应 的
的 ,
, ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。
分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。
在540K下,按初始投料比 、
、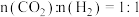 、
、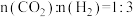 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
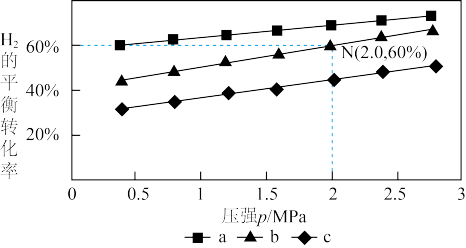
①a、b、c各曲线所表示的投料比由大到小的顺序为______ (用字母表示)。
②N点在b曲线上,540K时的压强平衡常数
______  (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。
③540K条件下,某容器测得某时刻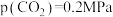 ,
, ,
,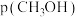
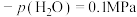 ,此时
,此时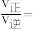
______ (保留两位小数)。
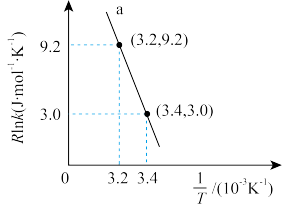
(3)甲醇催化可制取丙烯,反应为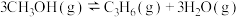 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。该反应的活化能
为活化能,k为速率常数,R和C为常数)。该反应的活化能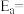
______  。
。
(4)Kistiakowsky曾研究了NOCl光化学分解反应。在一定频率(v)光的照射下,反应的机理为:
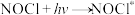

其中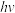 表示一个光子能量,
表示一个光子能量, 表示NOCl的激发态。则吸收1mol光子可分解
表示NOCl的激发态。则吸收1mol光子可分解______ mol NOCl。
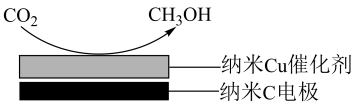
(5)在饱和 电解液中,电解活化的
电解液中,电解活化的 也可以制备
也可以制备 ,其原理如图所示,则阴极的电极反应式为
,其原理如图所示,则阴极的电极反应式为______ 。
(1)一种重要的工业制备甲醇的反应为

 。
。已知:①


②

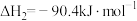
该制备反应的

 的平衡转化率
的平衡转化率(2)已知反应
 的
的 ,
, ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。
分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。在540K下,按初始投料比
 、
、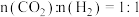 、
、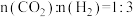 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
①a、b、c各曲线所表示的投料比由大到小的顺序为
②N点在b曲线上,540K时的压强平衡常数

 (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。③540K条件下,某容器测得某时刻
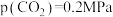 ,
, ,
,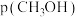
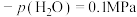 ,此时
,此时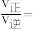
(3)甲醇催化可制取丙烯,反应为
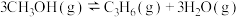 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。该反应的活化能
为活化能,k为速率常数,R和C为常数)。该反应的活化能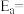
 。
。
(4)Kistiakowsky曾研究了NOCl光化学分解反应。在一定频率(v)光的照射下,反应的机理为:
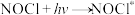

其中
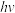 表示一个光子能量,
表示一个光子能量, 表示NOCl的激发态。则吸收1mol光子可分解
表示NOCl的激发态。则吸收1mol光子可分解(5)在饱和
 电解液中,电解活化的
电解液中,电解活化的 也可以制备
也可以制备 ,其原理如图所示,则阴极的电极反应式为
,其原理如图所示,则阴极的电极反应式为
您最近一年使用:0次



