名校
1 . 在 温度下,向1L恒容容器中加入1molCO和
温度下,向1L恒容容器中加入1molCO和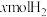 ,发生反应
,发生反应
 ,得到
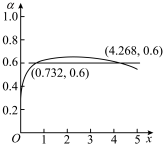
,得到 的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知
的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知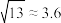 )
)
 温度下,向1L恒容容器中加入1molCO和
温度下,向1L恒容容器中加入1molCO和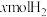 ,发生反应
,发生反应
 ,得到
,得到 的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知
的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知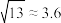 )
)
A.起始时向容器中加入 ,平衡后再加入 ,平衡后再加入 ,再次平衡时 ,再次平衡时 的转化率会减小 的转化率会减小 |
B.其他条件相同,只改变温度和 初始投料,使 初始投料,使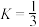 ,x=3,此时 ,x=3,此时 的平衡转化率约为56.7% 的平衡转化率约为56.7% |
C.与x=0.732相比,当x=4.268时,平衡体系中 的体积分数更小 的体积分数更小 |
D.一定温度下,向1L恒容容器中加入HI(g),使其分解达到平衡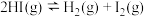 ,当HI投料量增大时,HI的平衡转化率先增大后减小 ,当HI投料量增大时,HI的平衡转化率先增大后减小 |
您最近一年使用:0次
名校
解题方法
2 . 近年来,碳中和、碳达峰成为热点。以CO2、H2为原料生产甲醇是一种有效利用二氧化碳的途径。
途径一:涉及的反应有
I.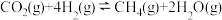
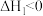
Ⅱ.

III.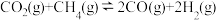
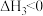
(1)关于反应I,下列描述正确的是___________(填字母序号)。
(2)根据反应I~Ⅲ,计算 ΔH=
ΔH=___________ 。
(3)工业中,对于反应I,通常同时存在副反应IV: ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。
ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。

①图a中,相同温度下,压强越大,CO2的平衡转化率越大,其原因是___________ 。
②由图b可知,ΔH4___________ 0(填“>”、“<”或“=”);H2的物质的量分数随温度升高而增大,原因是___________ 。
(4)在一定条件下(温度为T1℃),往恒容密闭容器中充入1.0molCO2和4.0molH2,发生反应I,初始压强为p0,5min达到平衡,压强为0.8p0,则CO2的平衡转化率为___________ 。
途径二:涉及的反应有
I.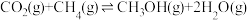
Ⅱ.
III.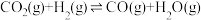
(5)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平行时,容器中CH3OH(g)为amol,CO为bmol,反应Ⅲ的平衡常数为___________ (用含a、b、V的代数式表示)。
途径一:涉及的反应有
I.
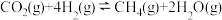
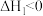
Ⅱ.


III.
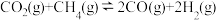
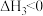
(1)关于反应I,下列描述正确的是___________(填字母序号)。
| A.恒容下达平衡状态时,再充入少量氦气,正逆反应速率不变 |
| B.当混合气体的平均摩尔质量不再发生变化时,反应达平衡状态 |
| C.当反应达平衡状态时,2V正(H2)=V逆(H2O) |
| D.恒温下缩小容器体积,反应物的活化分子百分数增大 |
 ΔH=
ΔH=(3)工业中,对于反应I,通常同时存在副反应IV:
 ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。
ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。
①图a中,相同温度下,压强越大,CO2的平衡转化率越大,其原因是
②由图b可知,ΔH4
(4)在一定条件下(温度为T1℃),往恒容密闭容器中充入1.0molCO2和4.0molH2,发生反应I,初始压强为p0,5min达到平衡,压强为0.8p0,则CO2的平衡转化率为
途径二:涉及的反应有
I.
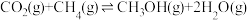
Ⅱ.

III.
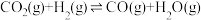
(5)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平行时,容器中CH3OH(g)为amol,CO为bmol,反应Ⅲ的平衡常数为
您最近一年使用:0次
名校
解题方法
3 . 向体积均为1L的两恒容容器中分别充入2molX和1molY发生反应: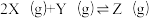
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
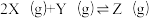
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是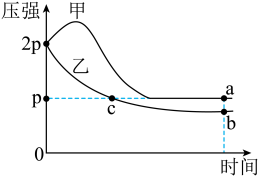
| A.△H>0 | B.气体的总物质的量:na>nc |
| C.a点平衡常数:K<12 | D.反应速率:Va正>Vb正 |
您最近一年使用:0次
2024-03-09更新
|
202次组卷
|
3卷引用:重庆市大足中学2023-2024学年高三下学期3月适应性考试化学试题
名校
解题方法
4 . 研究氮氧化物反应的特征及机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:
(1)氮的氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
Ⅰ.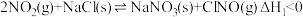
Ⅱ.
①反应: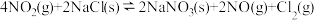 只有在低温时自发进行,则该反应的活化能:
只有在低温时自发进行,则该反应的活化能: (正)
(正)___________  (逆)(填“>”或“<”),。
(逆)(填“>”或“<”),。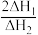 的数值范围是
的数值范围是___________ (填序号)。
A.<-1 B.-1~0 C.0~1 D.>1
②为研究上述反应体系的平衡关系,恒温条件下,向盛有足量NaCl(s)的恒容密闭容器中加入0.2mol 、0.2molNO和0.1mol
、0.2molNO和0.1mol ,初始压强为
,初始压强为 ,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%,
,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%, 的平衡转化率为20%,则平衡反应时
的平衡转化率为20%,则平衡反应时
___________ mol,Ⅱ的压强平衡常数
___________ ( 为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
(2)CO还原氮氧化物的反应如下: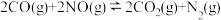
 。
。
①该反应分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图甲所示。
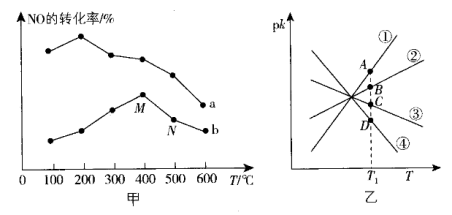
在催化剂作用下,图中M点___________ (填“达到了”或“未达到”)平衡状态。温度高于400℃,NO转化率降低的原因可能是___________ 。
②实验测得 (
( 是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示
是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示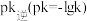 随温度变化的是
随温度变化的是___________ (填序号)升高温度,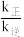
___________ (填“增大”“减小”或“不变”)图中 点的纵坐标分别为
点的纵坐标分别为 ,则温度T1时化学平衡常数
,则温度T1时化学平衡常数
___________ L/mol。
③同温同压下,再向该容器中注入稀有气体氦气,该反应的化学平衡将___________ (填“正向移动”“逆向移动”或“不移动”)。
(1)氮的氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
Ⅰ.
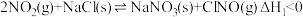
Ⅱ.

①反应:
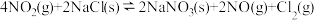 只有在低温时自发进行,则该反应的活化能:
只有在低温时自发进行,则该反应的活化能: (正)
(正) (逆)(填“>”或“<”),。
(逆)(填“>”或“<”),。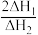 的数值范围是
的数值范围是A.<-1 B.-1~0 C.0~1 D.>1
②为研究上述反应体系的平衡关系,恒温条件下,向盛有足量NaCl(s)的恒容密闭容器中加入0.2mol
 、0.2molNO和0.1mol
、0.2molNO和0.1mol ,初始压强为
,初始压强为 ,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%,
,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%, 的平衡转化率为20%,则平衡反应时
的平衡转化率为20%,则平衡反应时

 为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
为以分压表示的平衡常数,气体分压=气体总压×体积分数)。(2)CO还原氮氧化物的反应如下:
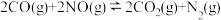
 。
。①该反应分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图甲所示。

在催化剂作用下,图中M点
②实验测得
 (
( 是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示
是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示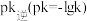 随温度变化的是
随温度变化的是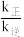
 点的纵坐标分别为
点的纵坐标分别为 ,则温度T1时化学平衡常数
,则温度T1时化学平衡常数
③同温同压下,再向该容器中注入稀有气体氦气,该反应的化学平衡将
您最近一年使用:0次
5 . 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
I.制取氢气
(1)甲醇和水蒸气制取氢气的过程中有下列反应:
CH3OH(g) CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+H2O(g) CO2(g)+H2 (g) △H=-4lkJ·mol-1
CO2(g)+H2 (g) △H=-4lkJ·mol-1
写出以甲醇为原料制取氢气的热化学方程式___________ 。
(2)理论上,能提高H2平衡产率的措施有___________ (写出一条即可)。
II.储存氢气
硼氢化钠(NaBH4) 是研究最广泛的储氢材料之一;
已知: i.B的电负性为2.0 H的电负性为2.1
ii.25℃下NaBH4 在水中的溶解度为55g,NaBO2在水中的溶解度为0.28g
(3)向NaBH4 水溶液中加入催化剂Ru/NGR后,能够迅速反应,生成偏硼酸钠(NaBO2) 和氢气。写出该反应的化学方程式___________ 。
(4)在研究浓度对催化剂Ru/NGR 活性的影响时,发现B 点后(见下图)增加NaBH4的浓度,制氢速率反而下降,推断可能的原因是___________ 。___________ ;
②电解过程中,阴极区溶液pH___________ 。(填“增大”“减小”或“不变”)
I.制取氢气
(1)甲醇和水蒸气制取氢气的过程中有下列反应:
CH3OH(g)
 CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+2H2(g) △H=+91 kJ·mol-1CO(g)+H2O(g)
 CO2(g)+H2 (g) △H=-4lkJ·mol-1
CO2(g)+H2 (g) △H=-4lkJ·mol-1写出以甲醇为原料制取氢气的热化学方程式
(2)理论上,能提高H2平衡产率的措施有
II.储存氢气
硼氢化钠(NaBH4) 是研究最广泛的储氢材料之一;
已知: i.B的电负性为2.0 H的电负性为2.1
ii.25℃下NaBH4 在水中的溶解度为55g,NaBO2在水中的溶解度为0.28g
(3)向NaBH4 水溶液中加入催化剂Ru/NGR后,能够迅速反应,生成偏硼酸钠(NaBO2) 和氢气。写出该反应的化学方程式
(4)在研究浓度对催化剂Ru/NGR 活性的影响时,发现B 点后(见下图)增加NaBH4的浓度,制氢速率反而下降,推断可能的原因是

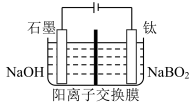
②电解过程中,阴极区溶液pH
您最近一年使用:0次
名校
6 . 纳米二氧化钛催化剂可用于工业上合成甲醇: ,按投料比
,按投料比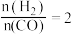 将
将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是

 ,按投料比
,按投料比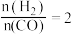 将
将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
A. , ,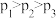 |
B.达到平衡后,再按照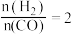 加入气体,平衡后 加入气体,平衡后 的体积分数增大 的体积分数增大 |
| C.M点平衡后,恒温恒容下,向容器中再加入2molCH3OH、3molCO,则平衡不移动 |
D. 、 、 压强下,Q点对应的 压强下,Q点对应的 |
您最近一年使用:0次
名校
7 . 二氧化碳一甲烷重整反应制备合成气(H2+CO)是一种生产高附加值化学品的低碳过程。该过程存在如下化学反应:
①

②
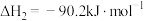
③
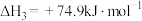
④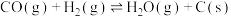
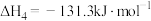
回答下列问题:
(1)
_______ ,反应①_______ 正向自发进行(填标号)。
A.低温下能 B.高温下能 C.任何温度下都能 D.任何温度下都不能
(2)反应体系总压强分别为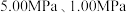 和
和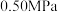 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为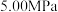 的曲线是
的曲线是_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”),判断依据是_______ 。 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是_______ 。 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为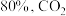 的转化率为
的转化率为 ,碳单质的物质的量为
,碳单质的物质的量为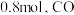 的物质的量为
的物质的量为_______  ,反应①用摩尔分数表示的平衡常数
,反应①用摩尔分数表示的平衡常数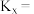
_______ (结果保留两位小数)。
上述平衡时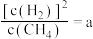 ,向体系通入
,向体系通入 气,重新达到平衡时,
气,重新达到平衡时,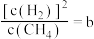 ,则a
,则a_______ b(填“>”“<”或“=”)。(已知反应 的
的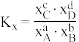 ,物质
,物质 的摩尔分数
的摩尔分数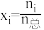 )
)
①


②

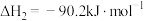
③

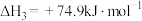
④
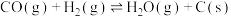
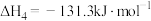
回答下列问题:
(1)

A.低温下能 B.高温下能 C.任何温度下都能 D.任何温度下都不能
(2)反应体系总压强分别为
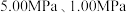 和
和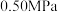 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为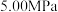 的曲线是
的曲线是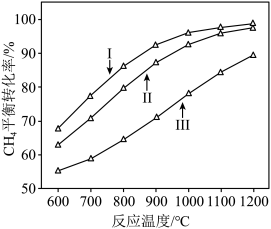
 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是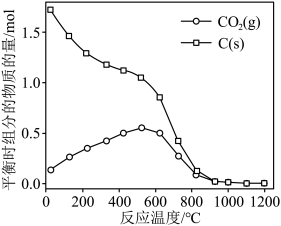
 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为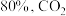 的转化率为
的转化率为 ,碳单质的物质的量为
,碳单质的物质的量为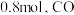 的物质的量为
的物质的量为 ,反应①用摩尔分数表示的平衡常数
,反应①用摩尔分数表示的平衡常数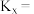
上述平衡时
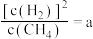 ,向体系通入
,向体系通入 气,重新达到平衡时,
气,重新达到平衡时,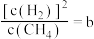 ,则a
,则a 的
的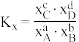 ,物质
,物质 的摩尔分数
的摩尔分数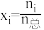 )
)
您最近一年使用:0次
2024-01-20更新
|
1226次组卷
|
4卷引用:湖南省长沙市雅礼中学2023-2024学年高三下学期月考(八)化学试题
湖南省长沙市雅礼中学2023-2024学年高三下学期月考(八)化学试题2024年1月河南普通高等学校招生考试适应性测试化学试题(已下线)T29-原理综合题(已下线)2024年1月“九省联考”河南卷真题完全解读与考后提升
名校
解题方法
8 . 工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理实现绿色环保、废物利用。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ·mol-1
H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为___________ 。
Ⅱ.脱碳:
(2)向2 L密闭容器中加入1mol CO2和3 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) CH3OH(l)+H2O(l) ΔH<0
CH3OH(l)+H2O(l) ΔH<0
①该反应自发进行的条件是___________ (填“低温”“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是___________ (填字母)。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
f. CO2和H2的物质的量之比保持不变 g. v正(CO2) = 3v逆(H2)
(3)工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g) CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
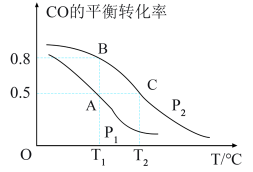
①p1、p2的大小关系是p1___________ p2(填“>”“<"或"=”)。
②A、B、C三点的平衡常数KA、KB、Kc的大小关系是___________ 。
(4)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。
①平衡时H2的体积分数是___________ ;平衡后再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大""不变”成“减小”),CO与CH3OH的浓度比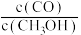
___________ (填"增大”“不变"或“减小")。
②若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___________ v(逆)(填“”“<"或“=”)。
③若p2压强恒定为p,则平衡常数Kp=___________ (Kp用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含p的最简表达式)。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ·mol-1
H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为
Ⅱ.脱碳:
(2)向2 L密闭容器中加入1mol CO2和3 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) ΔH<0
CH3OH(l)+H2O(l) ΔH<0①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
f. CO2和H2的物质的量之比保持不变 g. v正(CO2) = 3v逆(H2)
(3)工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g)
 CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
①p1、p2的大小关系是p1
②A、B、C三点的平衡常数KA、KB、Kc的大小关系是
(4)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。
①平衡时H2的体积分数是
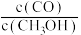
②若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)
③若p2压强恒定为p,则平衡常数Kp=
您最近一年使用:0次
名校
解题方法
9 . “碳达峰”“碳中和”是推动我国经济社会高质量发展的内在要求。通过二氧化碳催化加氢合成二甲醚是一种重要的转化方法,其过程如下:
反应Ⅰ:
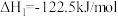
反应Ⅱ:
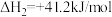
回答下列问题:
(1)二氧化碳与氢气合成CH3OCH3时,通常控制温度为 500℃左右,其可能的原因为_____(填字母)。
(2)在 1L 恒温密闭容器中充入4molCO2和6molH2 ,初始压强为 p,20min 时反应 Ⅰ、Ⅱ都达到平衡状态,体系压强为 0.8p,测得 c(H2O)=3mol/L。
①0~20min 内v(CO)=________ 。
②反应Ⅱ的化学平衡常数Kp=________ 。
③平衡时 CH3OCH3的选择性=________ 。( )
)
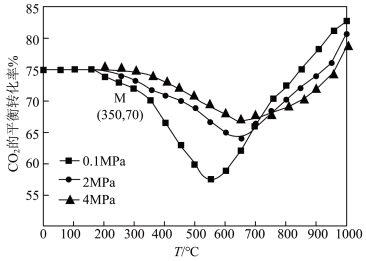
(3)在密闭容器中通入1 nolCO2和3molH2,在铁系催化剂作用下进行反应, 的平衡转化率随温度和压强的变化如图所示。图中,温度大于 800℃时,随着压强的增大, CO2的平衡转化率减小,请解释原因:___________ 。
反应Ⅰ:

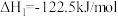
反应Ⅱ:

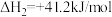
回答下列问题:
(1)二氧化碳与氢气合成CH3OCH3时,通常控制温度为 500℃左右,其可能的原因为_____(填字母)。
| A.反应速率快 | B.平衡的转化率高 |
| C.催化剂活性高 | D.主反应催化剂选择性好 |
(2)在 1L 恒温密闭容器中充入4molCO2和6molH2 ,初始压强为 p,20min 时反应 Ⅰ、Ⅱ都达到平衡状态,体系压强为 0.8p,测得 c(H2O)=3mol/L。
①0~20min 内v(CO)=
②反应Ⅱ的化学平衡常数Kp=
③平衡时 CH3OCH3的选择性=
 )
)(3)在密闭容器中通入1 nolCO2和3molH2,在铁系催化剂作用下进行反应, 的平衡转化率随温度和压强的变化如图所示。图中,温度大于 800℃时,随着压强的增大, CO2的平衡转化率减小,请解释原因:

您最近一年使用:0次
名校
解题方法
10 . 完成下列问题。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: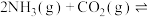
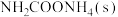
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
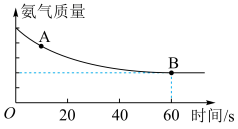
A点正反应速率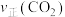
___________ B点逆反应速率 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比___________ (填“下降”、“不变”或“升高”)
(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
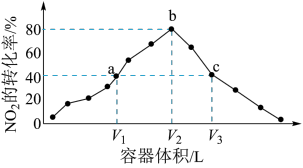
下列说法正确的是___________ 。
A.容器内的压强: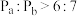
B.图中c点所示条件下,
C.向a点平衡体系中充入一定量的 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大
(3)电解法制取 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
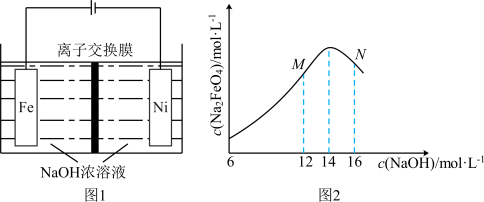
①电解时,Fe电极发生的电极反应式为___________ 。
②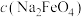 随初始
随初始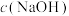 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点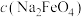 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点___________ ;N点___________ 。
(4)甲醚( )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:
主反应①: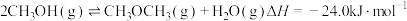 。
。
副反应②: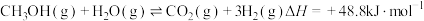 。
。
选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
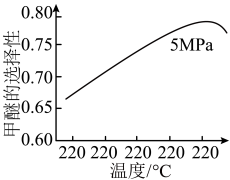
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是___________ 。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的
 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: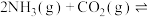
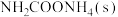
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
A点正反应速率
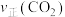
 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol
 ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
下列说法正确的是
A.容器内的压强:
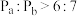
B.图中c点所示条件下,

C.向a点平衡体系中充入一定量的
 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大(3)电解法制取
 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
①电解时,Fe电极发生的电极反应式为
②
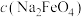 随初始
随初始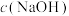 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点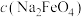 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点(4)甲醚(
 )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:主反应①:
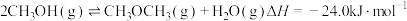 。
。副反应②:
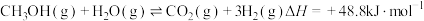 。
。选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。
 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是
您最近一年使用:0次



