名校
1 . 向 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
,发生反应: 。在不同温度下测得
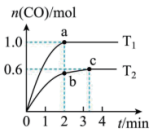
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
,发生反应: 。在不同温度下测得
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
| A.该反应在任意温度下均可自发进行 |
B. 温度下, 温度下, 的平衡转化率是30% 的平衡转化率是30% |
C. 、 、 两点平衡常数: 两点平衡常数: |
D. 温度下,0到 温度下,0到 内,用 内,用 表示的平均反应速率为0.1mol·L-1·min-1 表示的平均反应速率为0.1mol·L-1·min-1 |
您最近一年使用:0次
名校
2 . 利用二氧化碳和氢气合成甲醇可以有效降低二氧化碳的排放量。
已知:①
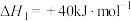

②


回答下面问题:
(1)利用二氧化碳和氢气合成甲醇的反应为:
 。已知该反应能够自发进行,则
。已知该反应能够自发进行,则
_______ (填“<”“>”或“=”)0,
_______ 0。该反应的平衡常数
_______ (用 和
和 表示),随着温度逐渐升高,
表示),随着温度逐渐升高, 将
将_______ (填“增大”或“减小”)。
(2)在某密闭容器中只发生反应②

①下面措施一定能提高CO的平衡转化率的是_______ 。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②该反应的正活化能 (正)
(正)_______ (填“<”“>”或“=”)逆活化能 (逆)。
(逆)。
(3)在某密闭容器中通入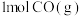 和
和 ,只发生反应②
,只发生反应②
 ,反应中CO的平衡转化率随温度和压强的变化如下:
,反应中CO的平衡转化率随温度和压强的变化如下:
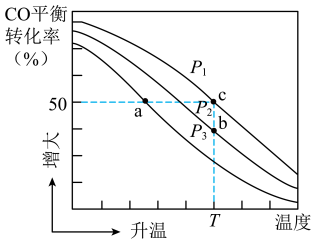
①随温度逐渐升高CO平衡转化率降低的原因是_______ 。
②压强 、
、 、
、 由大到小的顺序是
由大到小的顺序是_______ 。
③a、b、c三点对应的压强平衡常数分别为 、
、 、
、 ,由大到小的顺序是
,由大到小的顺序是_______ 。
④写出c点的压强平衡常数
_______ 。
已知:①

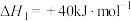

②



回答下面问题:
(1)利用二氧化碳和氢气合成甲醇的反应为:

 。已知该反应能够自发进行,则
。已知该反应能够自发进行,则


 和
和 表示),随着温度逐渐升高,
表示),随着温度逐渐升高, 将
将(2)在某密闭容器中只发生反应②


①下面措施一定能提高CO的平衡转化率的是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②该反应的正活化能
 (正)
(正) (逆)。
(逆)。(3)在某密闭容器中通入
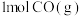 和
和 ,只发生反应②
,只发生反应②
 ,反应中CO的平衡转化率随温度和压强的变化如下:
,反应中CO的平衡转化率随温度和压强的变化如下:
①随温度逐渐升高CO平衡转化率降低的原因是
②压强
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③a、b、c三点对应的压强平衡常数分别为
 、
、 、
、 ,由大到小的顺序是
,由大到小的顺序是④写出c点的压强平衡常数

您最近一年使用:0次
3 . 为了实现“碳中和”,研发 的利用技术成为热点。
的利用技术成为热点。
反应I:
反应Ⅱ:
请回答:
(1)反应I能够自发进行的条件是__________ 。
(2)向 的恒容密闭容器中充入
的恒容密闭容器中充入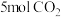 和
和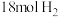 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
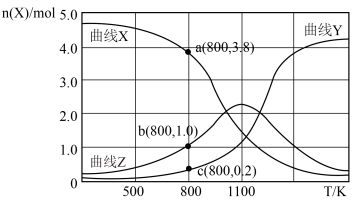
①写出曲线Y表示的含碳元素物质的化学式__________ 。
② 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
__________ [对于气相反应,用某组分 的平衡压强
的平衡压强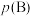 代替物质的量浓度
代替物质的量浓度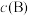 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如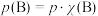 ,
, 为平衡总压强,
为平衡总压强,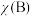 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。
(3)可用 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: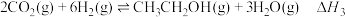 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示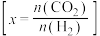 :
:

①上述反应的活化能 (正)
(正)__________  (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
② 、
、 、
、 由大到小的顺序是
由大到小的顺序是__________ 。
③从平衡角度分析,随温度升高,不同投料比时 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因__________ 。
(4)科学家提出由 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为__________ 。

(5)水系可逆 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:

①放电时复合膜中向 极移动的离子是
极移动的离子是__________ 。
②充电时多孔 纳米片电极的电极反应式为
纳米片电极的电极反应式为__________ 。
 的利用技术成为热点。
的利用技术成为热点。反应I:

反应Ⅱ:

请回答:
(1)反应I能够自发进行的条件是
(2)向
 的恒容密闭容器中充入
的恒容密闭容器中充入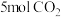 和
和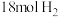 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
①写出曲线Y表示的含碳元素物质的化学式
②
 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
 的平衡压强
的平衡压强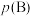 代替物质的量浓度
代替物质的量浓度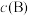 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如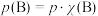 ,
, 为平衡总压强,
为平衡总压强,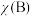 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。(3)可用
 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: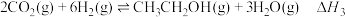 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示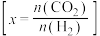 :
:
①上述反应的活化能
 (正)
(正) (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。②
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③从平衡角度分析,随温度升高,不同投料比时
 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因(4)科学家提出由
 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为
(5)水系可逆
 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:
①放电时复合膜中向
 极移动的离子是
极移动的离子是②充电时多孔
 纳米片电极的电极反应式为
纳米片电极的电极反应式为
您最近一年使用:0次
名校
4 . 下列叙述正确的是
| A.稀醋酸中加少量醋酸钠能增大醋酸的电离程度 |
B.25℃时,将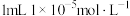 盐酸稀释至1000mL,所得溶液的pH为8 盐酸稀释至1000mL,所得溶液的pH为8 |
| C.蔗糖在水中溶解,这是熵增的过程 |
D.0.1molAgCl和0.1molAgI混合后加入1L水中所得溶液中 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法正确的是
A.一定条件下反应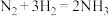 达到平衡时, 达到平衡时,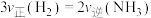 |
B. 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的 |
C.室温下, 的 的 溶液与 溶液与 的 的 溶液等体积混合,溶液 溶液等体积混合,溶液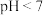 |
D.对于乙酸与乙醇的酯化反应( ),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 ),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
您最近一年使用:0次
2024-03-10更新
|
192次组卷
|
2卷引用:江苏省南京师范大学附属中学2023-2024学年高二上学期 期末考试化学试卷
解题方法
6 .  资源化利用是解决资源和能源短缺、减少碳排放的一种途径。以
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。以 为催化剂,可使
为催化剂,可使 在温和条件下转化为甲醇,反应历程如图所示。
在温和条件下转化为甲醇,反应历程如图所示。 与
与 在活化后的催化剂表面发生可逆反应,每生成1mol
在活化后的催化剂表面发生可逆反应,每生成1mol 放热49.3kJ。
放热49.3kJ。
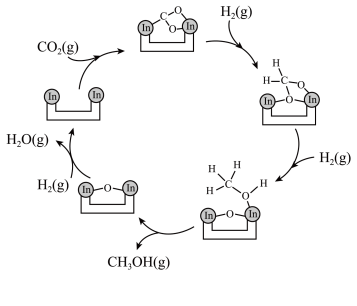
下列说法错误的是
 资源化利用是解决资源和能源短缺、减少碳排放的一种途径。以
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。以 为催化剂,可使
为催化剂,可使 在温和条件下转化为甲醇,反应历程如图所示。
在温和条件下转化为甲醇,反应历程如图所示。 与
与 在活化后的催化剂表面发生可逆反应,每生成1mol
在活化后的催化剂表面发生可逆反应,每生成1mol 放热49.3kJ。
放热49.3kJ。
下列说法错误的是
A.该反应的 |
B.该反应的平衡常数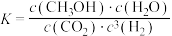 |
C.向容器中充入1mol 和足量 和足量 后,在催化剂存在下充分反应放热49.3kJ 后,在催化剂存在下充分反应放热49.3kJ |
D.该反应中每消耗1molCO2转移电子数为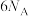 |
您最近一年使用:0次
2024-03-07更新
|
77次组卷
|
2卷引用:河南省焦作市2023-2024学年高二上学期1月期末化学试题
7 . 在常温常压下,下列属于自发过程的是
A. |
B.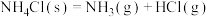 |
C.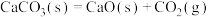 |
D.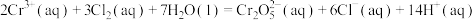 |
您最近一年使用:0次
2024-03-07更新
|
60次组卷
|
2卷引用:湖南省娄底市涟源市2023-2024学年高二上学期1月期末考试化学试题
解题方法
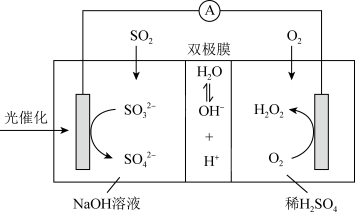
8 . 我国科研人员设计将脱除 的反应与制备
的反应与制备 相结合的协同转化装置如图。在电场作用下,双极膜中间层的
相结合的协同转化装置如图。在电场作用下,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移。已知:①单独制备
,并向两极迁移。已知:①单独制备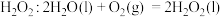 ,不能自发进行;②单独脱除
,不能自发进行;②单独脱除 :
: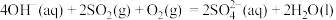 能自发进行。下列说法
能自发进行。下列说法不正确 的是
 的反应与制备
的反应与制备 相结合的协同转化装置如图。在电场作用下,双极膜中间层的
相结合的协同转化装置如图。在电场作用下,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移。已知:①单独制备
,并向两极迁移。已知:①单独制备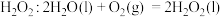 ,不能自发进行;②单独脱除
,不能自发进行;②单独脱除 :
: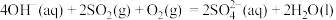 能自发进行。下列说法
能自发进行。下列说法
A.②单独脱除 反应的 反应的 |
B.协同转化工作时, 透过双极膜向左侧移动 透过双极膜向左侧移动 |
C.正极的电极反应式: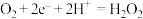 |
D.协同转化总反应: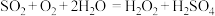 |
您最近一年使用:0次
9 . 随着温室效应越来越严重,降低空气中二氧化碳含量成为研究热点,回答下列问题。
将二氧化碳转化为甲醇是目前重要的碳中和方法,体系中发生如下反应:
主反应:①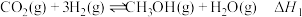
副反应:②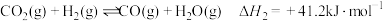
已知: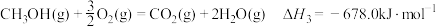

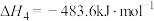
(1)反应①的
___________ (用含 、
、 的代数式表示),该反应在
的代数式表示),该反应在___________ (填“高温”“低温”或“任何温度下”)下有利于自发进行。
(2)密闭容器中通入CO2和H2仅发生反应①,仅改变以下一个条件,能提高H2平衡转化率的措施有___________(填正确答案的编号)。
(3)某温度下,1L恒容密闭容器中加入1molCO2(g)和3molH2(g),发生反应①和反应②,平衡时CO2的转化率为α,CO(g)的物质的量为bmol,计算反应①的平衡常数K=___________ (用含有α、b的计算式表示)。
(4)副反应②在Cu催化时,反应历程如下(*表示吸附在催化剂表面),请写出步骤iv的方程式。
i: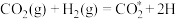
ii: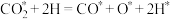
iii:
iv:___________
v: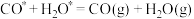
(5)选择不同的温度和催化剂(a、b、c)都对甲醇产率有影响,根据下图,最佳反应条件为___________ 。
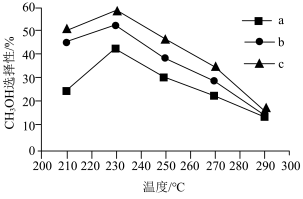
(6)电解还原二氧化碳也能实现碳中和,图2为电解还原CO2制备CO,同时获得两种副产物的装置:
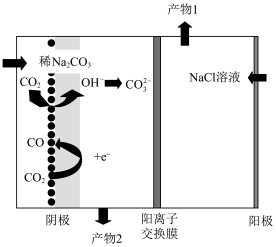
①请写出阳极的电极反应式:___________ 。
②产物2为___________ 。
将二氧化碳转化为甲醇是目前重要的碳中和方法,体系中发生如下反应:
主反应:①
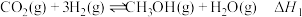
副反应:②
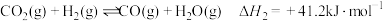
已知:
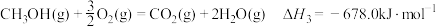

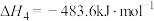
(1)反应①的

 、
、 的代数式表示),该反应在
的代数式表示),该反应在(2)密闭容器中通入CO2和H2仅发生反应①,仅改变以下一个条件,能提高H2平衡转化率的措施有___________(填正确答案的编号)。
| A.恒温恒容时增加CO2(g)用量 | B.恒温恒压下通入惰性气体 |
| C.升高温度 | D.加入催化剂 |
(3)某温度下,1L恒容密闭容器中加入1molCO2(g)和3molH2(g),发生反应①和反应②,平衡时CO2的转化率为α,CO(g)的物质的量为bmol,计算反应①的平衡常数K=
(4)副反应②在Cu催化时,反应历程如下(*表示吸附在催化剂表面),请写出步骤iv的方程式。
i:
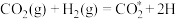
ii:
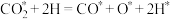
iii:

iv:
v:
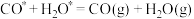
(5)选择不同的温度和催化剂(a、b、c)都对甲醇产率有影响,根据下图,最佳反应条件为

(6)电解还原二氧化碳也能实现碳中和,图2为电解还原CO2制备CO,同时获得两种副产物的装置:

①请写出阳极的电极反应式:
②产物2为
您最近一年使用:0次
10 . 下列说法正确的是
| A.强电解质溶液中不存在分子,弱电解质溶液中存在分子 |
B.将 溶液从常温加热至90℃,水的离子积变大、 溶液从常温加热至90℃,水的离子积变大、 变小 变小 |
| C.在其他外界条件不变的情况下,增大压强能增大活化分子百分数 |
D.反应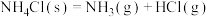 在室温下不能自发进行,说明该反应的 在室温下不能自发进行,说明该反应的 |
您最近一年使用:0次



