1 . 将二氧化碳转化为高附加值化学品和含氮物质的综合处理是目前研究的热点问题
(1)利用CO2合成甲醇
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49kJ/mol
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H2=+41.17kJ/mol
③CO(g)+2H2(g)⇌CH3OH(g) ∆H3
根据以上信息判断反应③___________ (填“高温自发”、“低温自发”或“任何温度下都自发”),该反应中活化能Ea(正)___________ Ea(逆)(填“>”或“<”)。
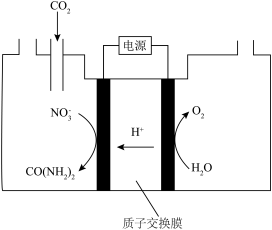
(2)电催化CO2和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的KNO3溶液通入CO2至饱和,经电解获得尿素,其原理如图所示。___________ 。
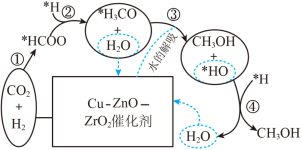
(3)我国科研人员研究出在Cu-ZnO-ZrO2催化剂上CO2氢化合成甲醇的反应历程如图所示。___________ 。
②乙醇胺(HOCH2CH2NH2)可完成对CO2捕集。乙醇胺溶液能够吸收和释放CO2的原因是_______ 。
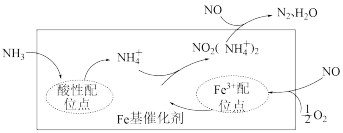
(4)研究脱除烟气中的NO是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示,该过程可描述为___________ 。
(1)利用CO2合成甲醇
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49kJ/mol
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H2=+41.17kJ/mol
③CO(g)+2H2(g)⇌CH3OH(g) ∆H3
根据以上信息判断反应③
(2)电催化CO2和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的KNO3溶液通入CO2至饱和,经电解获得尿素,其原理如图所示。
(3)我国科研人员研究出在Cu-ZnO-ZrO2催化剂上CO2氢化合成甲醇的反应历程如图所示。
②乙醇胺(HOCH2CH2NH2)可完成对CO2捕集。乙醇胺溶液能够吸收和释放CO2的原因是
(4)研究脱除烟气中的NO是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示,该过程可描述为
您最近一年使用:0次
名校
解题方法
2 . 埃林汉姆图,由英国物理化学家哈罗德·埃林汉姆于1944年最先制作,在冶金工业中可用于评估氧化物的热稳定性。图像中,每条直线代表该反应吉布斯自由能( )与温度的关系。
)与温度的关系。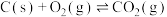 在埃林汉姆图中的斜率近似为0,请简述原因
在埃林汉姆图中的斜率近似为0,请简述原因______ 。
(2)结合图像推测,若以 为原料,理论上
为原料,理论上______ 用热分解法获得铝单质。
A.可以 B.不可以
(3)工业中,以 为原料,采用电解法冶炼金属铝,在______极获得铝单质。
为原料,采用电解法冶炼金属铝,在______极获得铝单质。
(4)写出阳极的电极方程式______ 。
(5)若电解一段时间后,收集到标况下56L气体,则这段时间内电路中转移的电子数目为______ 个。
(6)写出以 为原料,冶炼金属
为原料,冶炼金属 的化学方程式
的化学方程式____________ 。
 )与温度的关系。
)与温度的关系。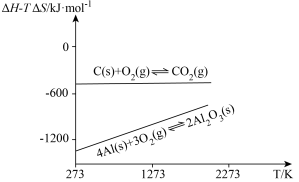
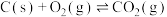 在埃林汉姆图中的斜率近似为0,请简述原因
在埃林汉姆图中的斜率近似为0,请简述原因(2)结合图像推测,若以
 为原料,理论上
为原料,理论上A.可以 B.不可以
(3)工业中,以
 为原料,采用电解法冶炼金属铝,在______极获得铝单质。
为原料,采用电解法冶炼金属铝,在______极获得铝单质。| A.正 | B.负 | C.阳 | D.阴 |
(4)写出阳极的电极方程式
(5)若电解一段时间后,收集到标况下56L气体,则这段时间内电路中转移的电子数目为
(6)写出以
 为原料,冶炼金属
为原料,冶炼金属 的化学方程式
的化学方程式
您最近一年使用:0次
3 . 空间探测器发射时常用肼( )作燃料,以二氧化氮作氧化剂,发生反应①:
)作燃料,以二氧化氮作氧化剂,发生反应①:


已知:②
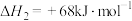
③
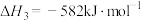
下列说法错误的是
 )作燃料,以二氧化氮作氧化剂,发生反应①:
)作燃料,以二氧化氮作氧化剂,发生反应①:


已知:②

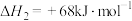
③

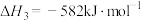
下列说法错误的是
A.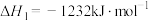 |
| B.反应①在任何温度下都能自发进行 |
C.反应①的平衡常数表达式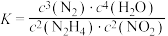 |
D.反应①中每产生1mol  ,转移电子的数目为 ,转移电子的数目为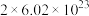 |
您最近一年使用:0次
名校
解题方法
4 . CO2和H2在某催化剂表面合成CH3OH: △H,反应历程如图1所示,其中吸附在催化剂表面上的物种用*标注。△G随温度关系如图2所示。
△H,反应历程如图1所示,其中吸附在催化剂表面上的物种用*标注。△G随温度关系如图2所示。
 △H,反应历程如图1所示,其中吸附在催化剂表面上的物种用*标注。△G随温度关系如图2所示。
△H,反应历程如图1所示,其中吸附在催化剂表面上的物种用*标注。△G随温度关系如图2所示。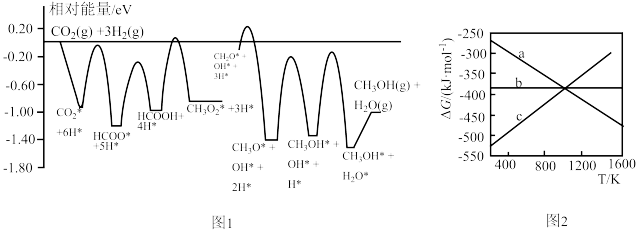
| A.该历程中的基元反应全部是放热反应 |
| B.图2中表示该反应△G随温度的变化的是直线a |
C.该反应历程中活化能最小的基元反应是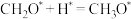 |
D. 过程中发生非极性键的断裂和生成 过程中发生非极性键的断裂和生成 |
您最近一年使用:0次
2024-05-26更新
|
188次组卷
|
3卷引用:浙江省新力量联盟2023-2024学年高二下学期6月期末考试化学试题
浙江省新力量联盟2023-2024学年高二下学期6月期末考试化学试题(已下线)暑假作业08 突破有关反应热的综合考查-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)安徽省合肥市第六中学2024届高三下学期最后一卷(三模)化学试题
解题方法
5 . 下列说法错误的是
A.反应 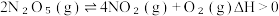 能自发进行的原因为△S>0 能自发进行的原因为△S>0 |
B. 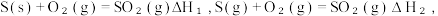 则 则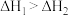 |
| C.合成氨反应采取循环操作的主要原因是为了提高化学反应速率 |
D.一定温度下,对 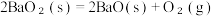 平衡体系缩小体积,再次达到平衡时 c 平衡体系缩小体积,再次达到平衡时 c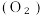 不变 不变 |
您最近一年使用:0次
6 . 丙烯腈(C3H3N)是制备腈纶的单体。一种制备丙烯腈反应的热化学方程式为C3H6(g)+NH3(g)+ O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是
 O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是| A.该反应只有在低温下才能自发进行 |
B.该反应的平衡常数K= |
| C.该反应每消耗1molC3H6,转移电子的物质的量为6mol |
| D.其他条件相同,减压和升温均有利于提高丙烯腊的平衡产率 |
您最近一年使用:0次
解题方法
7 . “氢经济”是“双碳”转型中非常关键的一环。大量安全制空是关键技术之一。
方法一:甲烷-水蒸气催化重整法。其涉及的主要反应如下:
反应I:

反应Ⅱ:
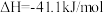
(1)反应 能自发进行的条件是
能自发进行的条件是________ (填“高温”“低温”或“任何温度下”)
(2)为了提高 的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
(3)恒定压强为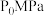 时,将
时,将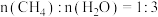 的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是________ (填字母)。
②系统中 的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:________ 。
③600℃时,计算反应Ⅱ的平衡常数
________ ( 是以分压表示的平衡常数,分压=总压
是以分压表示的平衡常数,分压=总压 物质的量分数,结果可用分数表示)。
物质的量分数,结果可用分数表示)。
方法二:甲醇催化脱空法。催化反应的部分机理如下:
历程i: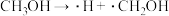 历程ii:
历程ii: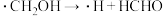
历程iii: 历程iv:
历程iv: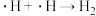
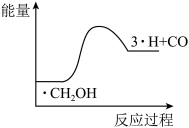
(4)在一个2L恒容密闭容器中投入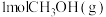 ,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图
,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图________ 。
方法一:甲烷-水蒸气催化重整法。其涉及的主要反应如下:
反应I:


反应Ⅱ:

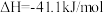
(1)反应
 能自发进行的条件是
能自发进行的条件是(2)为了提高
 的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。| A.使用高效催化剂 | B.升高温度 |
| C.增大压强 | D.增大 和 和 物质的量之比 物质的量之比 |
(3)恒定压强为
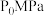 时,将
时,将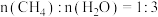 的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。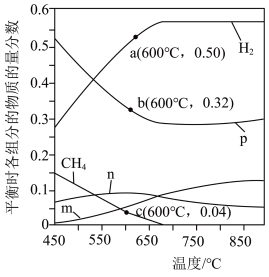
 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是②系统中
 的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:③600℃时,计算反应Ⅱ的平衡常数

 是以分压表示的平衡常数,分压=总压
是以分压表示的平衡常数,分压=总压 物质的量分数,结果可用分数表示)。
物质的量分数,结果可用分数表示)。方法二:甲醇催化脱空法。催化反应的部分机理如下:
历程i:
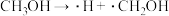 历程ii:
历程ii: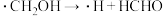
历程iii:
 历程iv:
历程iv: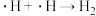
(4)在一个2L恒容密闭容器中投入
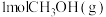 ,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图
,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图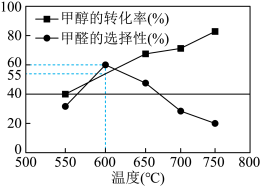
您最近一年使用:0次
8 . 下列说法不正确的是:
A.反应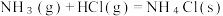 在低温下能自发进行,则该反应的△H>0 在低温下能自发进行,则该反应的△H>0 |
| B.对于2A(g)+B(g)⇌2C(g)△H>0,当温度升高时,平衡向正反应方向移动,V正和V逆均增大 |
| C.对于2A(g)+B(g)⇌2C(g)△H>0,增大A的浓度,平衡向正反应方向移动,V正和V逆均增大 |
| D.升高温度或加入催化剂能使单 |
您最近一年使用:0次
解题方法
9 . 利用 干重整反应:
干重整反应: ,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。
,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。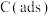 为吸附活性炭,该反应一般认为通过如图步骤来实现:
为吸附活性炭,该反应一般认为通过如图步骤来实现:
 干重整反应:
干重整反应: ,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。
,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。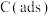 为吸附活性炭,该反应一般认为通过如图步骤来实现:
为吸附活性炭,该反应一般认为通过如图步骤来实现: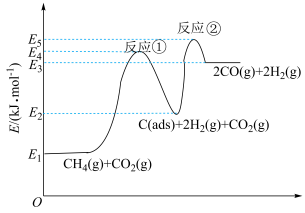
| A.反应①、②在高温条件下均能自发进行 |
| B.该反应速率主要由反应①决定 |
C.该反应的平衡常数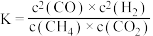 |
D.该反应中每产生 ,转移电子的数目约为 ,转移电子的数目约为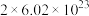 |
您最近一年使用:0次
10 . 气态 的一种工业制法流程如图:
的一种工业制法流程如图: 为阿伏加德罗常数的值②
为阿伏加德罗常数的值② 时,次磷酸(
时,次磷酸( )的电离常数
)的电离常数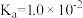 ,下列说法错误的是
,下列说法错误的是
 的一种工业制法流程如图:
的一种工业制法流程如图: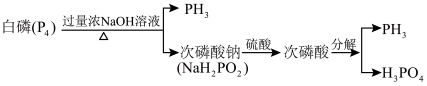
 为阿伏加德罗常数的值②
为阿伏加德罗常数的值② 时,次磷酸(
时,次磷酸( )的电离常数
)的电离常数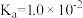 ,下列说法错误的是
,下列说法错误的是| A.液态次磷酸分解反应为熵增过程 |
B. 是非极性分子, 是非极性分子, 所含价层电子对数为 所含价层电子对数为 |
C.白磷与浓 溶液反应生成 溶液反应生成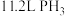 (标准状况下)时,转移电子的数目为 (标准状况下)时,转移电子的数目为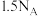 |
D.常温下,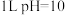 的 的 溶液中由水电离出的 溶液中由水电离出的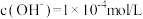 |
您最近一年使用:0次
2024-04-29更新
|
61次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题



