名校
解题方法
1 . 二甲醚( )被称为“21世纪的清洁燃料”。以
)被称为“21世纪的清洁燃料”。以 、
、 为原料制备二甲醚涉及的主要反应如下:
为原料制备二甲醚涉及的主要反应如下:
Ⅰ.
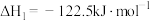
Ⅱ.

回答下列问题:
(1)反应Ⅰ自发进行的条件是_____ (填“高温”或“低温”)。
(2)已知 、
、 下,
下, 、
、 的燃烧热分别为:
的燃烧热分别为: 、
、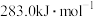 ,
,
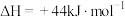 ,则
,则
_____  。
。
(3)保持压强为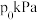 ,按
,按 投料,发生反应Ⅰ、Ⅱ,实验测得
投料,发生反应Ⅰ、Ⅱ,实验测得 平衡转化率和平衡时
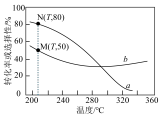
平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。
已知: 的选择性
的选择性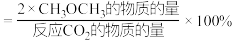
① 时向平衡体系中充入一定量的Ar,M点位置
时向平衡体系中充入一定量的Ar,M点位置_____ (填“上移”“下移”或“不变”),原因是_____ 。
② 时,反应Ⅰ、Ⅱ经4min达到平衡;反应Ⅱ的
时,反应Ⅰ、Ⅱ经4min达到平衡;反应Ⅱ的
_____ 。则该时间段 的平均速率为
的平均速率为_____  (保留小数点后两位)。
(保留小数点后两位)。
③表示平衡时 的选择性的是曲线
的选择性的是曲线_____ (填“a”或“b”);温度低于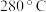 时,曲线b随温度升高而降低的原因是
时,曲线b随温度升高而降低的原因是_____ ;
 )被称为“21世纪的清洁燃料”。以
)被称为“21世纪的清洁燃料”。以 、
、 为原料制备二甲醚涉及的主要反应如下:
为原料制备二甲醚涉及的主要反应如下:Ⅰ.

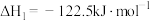
Ⅱ.


回答下列问题:
(1)反应Ⅰ自发进行的条件是
(2)已知
 、
、 下,
下, 、
、 的燃烧热分别为:
的燃烧热分别为: 、
、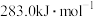 ,
,
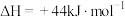 ,则
,则
 。
。(3)保持压强为
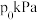 ,按
,按 投料,发生反应Ⅰ、Ⅱ,实验测得
投料,发生反应Ⅰ、Ⅱ,实验测得 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。已知:
 的选择性
的选择性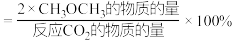
①
 时向平衡体系中充入一定量的Ar,M点位置
时向平衡体系中充入一定量的Ar,M点位置
②
 时,反应Ⅰ、Ⅱ经4min达到平衡;反应Ⅱ的
时,反应Ⅰ、Ⅱ经4min达到平衡;反应Ⅱ的
 的平均速率为
的平均速率为 (保留小数点后两位)。
(保留小数点后两位)。③表示平衡时
 的选择性的是曲线
的选择性的是曲线 时,曲线b随温度升高而降低的原因是
时,曲线b随温度升高而降低的原因是
您最近一年使用:0次
名校
2 . 化石燃料的综合利用既能减少污染,又能提高资源利用率。回答下列问题:
(1)在一定温度下,向某恒容容器中充入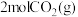 和
和 仅发生反应:
仅发生反应: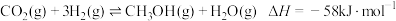 。
。
①该反应的
_______ 0(填“>”、“<”或“=”)0,能在_______ (填“高温”“低温”或“任何温度”)下自发。
②下列情况表明该反应已达到平衡状态的是_______ (填标号)。
A.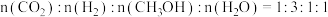
B.混合气体的密度保持不变
C.混合气体的平均摩尔质量保持不变
D. 与
与 的物质的量之比不再改变
的物质的量之比不再改变
E.
F.
(2)向 的恒容密闭容器中充入
的恒容密闭容器中充入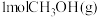 发生反应:
发生反应: 。其他条件不变时,
。其他条件不变时, 的平衡转化率随着温度(T)的变化如图所示。
的平衡转化率随着温度(T)的变化如图所示。

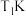 时,反应经过
时,反应经过 达到平衡,用
达到平衡,用 表示该段时间内的平均速率为
表示该段时间内的平均速率为_______  ,该温度下的平衡常数
,该温度下的平衡常数
_______ (用分数表示);该温度下,改变投料,某时刻容器内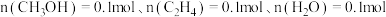 则此时
则此时
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)煤气化过程如下:反应1: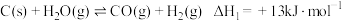
反应2: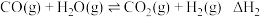
反应3: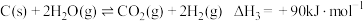
①由反应1、3可得出。
_______ 。
②反应 在催化剂M表面进行,其中
在催化剂M表面进行,其中 生成
生成 的历程如图所示(*表示吸附在催化剂表面的物种,
的历程如图所示(*表示吸附在催化剂表面的物种, 表示过渡态,能量的单位为
表示过渡态,能量的单位为 )。
)。

本历程的决速步骤的反应方程式为_______ 。
(1)在一定温度下,向某恒容容器中充入
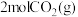 和
和 仅发生反应:
仅发生反应: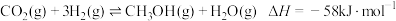 。
。①该反应的

②下列情况表明该反应已达到平衡状态的是
A.
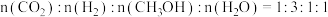
B.混合气体的密度保持不变
C.混合气体的平均摩尔质量保持不变
D.
 与
与 的物质的量之比不再改变
的物质的量之比不再改变E.

F.

(2)向
 的恒容密闭容器中充入
的恒容密闭容器中充入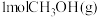 发生反应:
发生反应: 。其他条件不变时,
。其他条件不变时, 的平衡转化率随着温度(T)的变化如图所示。
的平衡转化率随着温度(T)的变化如图所示。
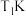 时,反应经过
时,反应经过 达到平衡,用
达到平衡,用 表示该段时间内的平均速率为
表示该段时间内的平均速率为 ,该温度下的平衡常数
,该温度下的平衡常数
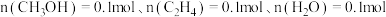 则此时
则此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)煤气化过程如下:反应1:
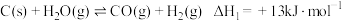
反应2:
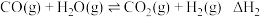
反应3:
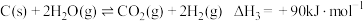
①由反应1、3可得出。

②反应
 在催化剂M表面进行,其中
在催化剂M表面进行,其中 生成
生成 的历程如图所示(*表示吸附在催化剂表面的物种,
的历程如图所示(*表示吸附在催化剂表面的物种, 表示过渡态,能量的单位为
表示过渡态,能量的单位为 )。
)。
本历程的决速步骤的反应方程式为
您最近一年使用:0次
名校
3 . 我国向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。研发利用二氧化碳技术,降低空气中二氧化碳含量成为重要的任务。
(1)倡导绿色低碳的生活方式,下列措施与节能减碳矛盾的是_____
(2) 加氢合成
加氢合成 的反应为
的反应为 。
。
①下列说法正确的是_____
A.调控反应条件不能改变反应限度
B.投入 和
和 能得到
能得到
C.当 的消耗速率等于其生成速率时,该反应已停止
的消耗速率等于其生成速率时,该反应已停止
D.该反应在一定温度下能自发进行,则
②一般认为,该反应经过如下步骤来实现:
反应Ⅰ: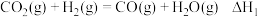 ;
;
反应Ⅱ: 。
。
则总反应的焓变
___________ (用包含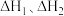 的代数式表示)。若某温度下,反应Ⅰ的平衡常数为
的代数式表示)。若某温度下,反应Ⅰ的平衡常数为 ,反应Ⅱ的平衡常数为
,反应Ⅱ的平衡常数为 ,则总反应的平衡常数
,则总反应的平衡常数
___________ (用包含 的代数式表示)
的代数式表示)
(3)二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应: ;
;
①写出主反应的平衡常数表达式:___________
②某容器中加入一定量的 和
和 ,保持温度和压强不变的情况下,达平衡后再向该容器中注入
,保持温度和压强不变的情况下,达平衡后再向该容器中注入 稀释,主反应的化学平衡将
稀释,主反应的化学平衡将___________ (填“正向移动”、“逆向移动”或“不移动”),达到新平衡后, 的体积分数将
的体积分数将___________ (填“增大”、“减小”或“不变”)
(4) 与
与 是典型的温室气体,
是典型的温室气体, 重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线:
重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线: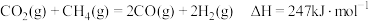
①该反应
___________ 0(填“>”或“<”)
②有传闻 重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?
重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?___________ (填“正确”或“错误”),并写出原因___________ 。
(1)倡导绿色低碳的生活方式,下列措施与节能减碳矛盾的是_____
| A.购物时使用环保袋 | B.就餐时践行光盘行动 |
| C.使用节能灯代替白炽灯 | D.为食品保鲜,冰箱温度越低越好 |
 加氢合成
加氢合成 的反应为
的反应为 。
。①下列说法正确的是
A.调控反应条件不能改变反应限度
B.投入
 和
和 能得到
能得到
C.当
 的消耗速率等于其生成速率时,该反应已停止
的消耗速率等于其生成速率时,该反应已停止D.该反应在一定温度下能自发进行,则

②一般认为,该反应经过如下步骤来实现:
反应Ⅰ:
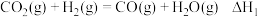 ;
;反应Ⅱ:
 。
。则总反应的焓变

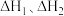 的代数式表示)。若某温度下,反应Ⅰ的平衡常数为
的代数式表示)。若某温度下,反应Ⅰ的平衡常数为 ,反应Ⅱ的平衡常数为
,反应Ⅱ的平衡常数为 ,则总反应的平衡常数
,则总反应的平衡常数
 的代数式表示)
的代数式表示)(3)二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应:
 ;
;①写出主反应的平衡常数表达式:
②某容器中加入一定量的
 和
和 ,保持温度和压强不变的情况下,达平衡后再向该容器中注入
,保持温度和压强不变的情况下,达平衡后再向该容器中注入 稀释,主反应的化学平衡将
稀释,主反应的化学平衡将 的体积分数将
的体积分数将(4)
 与
与 是典型的温室气体,
是典型的温室气体, 重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线:
重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线:
①该反应

②有传闻
 重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?
重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?
您最近一年使用:0次
名校
4 . CO2的捕集、利用与封存成为科学家研究的重要课题,已知CO2经催化加氢可以生成多种低碳有机物。
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1= −49.5kJ·mol-1
CH3OH(g)+H2O(g) ΔH1= −49.5kJ·mol-1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2= +40.9kJ·mol-1
CO(g)+H2O(g) ΔH2= +40.9kJ·mol-1
Ⅲ.CO(g)+2H2(g) CH3OH(g) ΔH3
CH3OH(g) ΔH3
回答下列问题:
(1)反应I在___________ (填“高温”“低温”或“任何温度”)条件下能够自发进行。
(2)反应Ⅲ的ΔH3为___________ 。
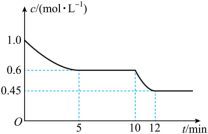
(3)一定温度下,在一容积固定的密闭容器中进行反应I,测得CO2的物质的量浓度随反应时间的变化如图所示,则反应前5 min内,v(H2)=___________ ;10 min时,改变的外界条件可能是___________ (填字母)。
(4)已知一定温度下按照起始比 =3,在一密闭容器中进行反应Ⅲ,保持总压为2.1MPa不变,达到平衡时CO的转化率为50%,则该条件下用平衡体系中各气体分压表示反应Ⅲ的平衡常数Kp=
=3,在一密闭容器中进行反应Ⅲ,保持总压为2.1MPa不变,达到平衡时CO的转化率为50%,则该条件下用平衡体系中各气体分压表示反应Ⅲ的平衡常数Kp=___________ MPa-2(保留2位有效数字) (各气体分压=平衡体系中各气体的物质的量分数×总压)。
(5)C2H6(g)+2CO2(g) 4CO(g)+3H2(g) ΔH= +430 kJ·mol-1,在四种不同条件容器中发生上述反应,若初始温度、容积、压强和反应物用量均相同,则CO2的平衡转化率最高的是___________(填字母)。
4CO(g)+3H2(g) ΔH= +430 kJ·mol-1,在四种不同条件容器中发生上述反应,若初始温度、容积、压强和反应物用量均相同,则CO2的平衡转化率最高的是___________(填字母)。
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1= −49.5kJ·mol-1
CH3OH(g)+H2O(g) ΔH1= −49.5kJ·mol-1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2= +40.9kJ·mol-1
CO(g)+H2O(g) ΔH2= +40.9kJ·mol-1Ⅲ.CO(g)+2H2(g)
 CH3OH(g) ΔH3
CH3OH(g) ΔH3回答下列问题:
(1)反应I在
(2)反应Ⅲ的ΔH3为
(3)一定温度下,在一容积固定的密闭容器中进行反应I,测得CO2的物质的量浓度随反应时间的变化如图所示,则反应前5 min内,v(H2)=
(4)已知一定温度下按照起始比
 =3,在一密闭容器中进行反应Ⅲ,保持总压为2.1MPa不变,达到平衡时CO的转化率为50%,则该条件下用平衡体系中各气体分压表示反应Ⅲ的平衡常数Kp=
=3,在一密闭容器中进行反应Ⅲ,保持总压为2.1MPa不变,达到平衡时CO的转化率为50%,则该条件下用平衡体系中各气体分压表示反应Ⅲ的平衡常数Kp=(5)C2H6(g)+2CO2(g)
 4CO(g)+3H2(g) ΔH= +430 kJ·mol-1,在四种不同条件容器中发生上述反应,若初始温度、容积、压强和反应物用量均相同,则CO2的平衡转化率最高的是___________(填字母)。
4CO(g)+3H2(g) ΔH= +430 kJ·mol-1,在四种不同条件容器中发生上述反应,若初始温度、容积、压强和反应物用量均相同,则CO2的平衡转化率最高的是___________(填字母)。| A.恒温恒容容器 | B.恒容绝热容器 |
| C.恒压绝热容器 | D.恒温恒压容器 |
您最近一年使用:0次
2023-12-25更新
|
144次组卷
|
2卷引用:四川省南充高级中学2023-2024学年高二上学期11月期中化学试题
5 . 电化学与能源、材料、化工等领域紧密联系,应用广泛。
(1)利用CH4燃料电池电解制备Ca(H2PO4)2,并得到副产物H2、Cl2等,装置如图。
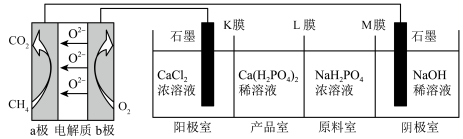
①a极为________ (填“正极”、“负极”、“阴极”或“阳极”),a电极上的电极反应式为________ 。
②K、M、L膜为离子交换膜,其中阳离子交换膜是___________ (填“K膜”、“L膜”、或“M膜”)。
③b极上消耗标准状况下2.24L的O2,理论上阳极室减少___________ molCa2+。
④阴极室的电极反应式为___________ 。
(2)用NaAlO2溶液制备Al2O3的过程如图。
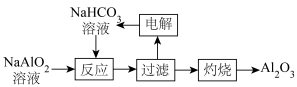
①“灼烧”时得到了Al2O3,该反应能自发的原因是___________ 。
②“电解”时阳极用惰性电极,阳极电极反应式为___________ 。
(1)利用CH4燃料电池电解制备Ca(H2PO4)2,并得到副产物H2、Cl2等,装置如图。

①a极为
②K、M、L膜为离子交换膜,其中阳离子交换膜是
③b极上消耗标准状况下2.24L的O2,理论上阳极室减少
④阴极室的电极反应式为
(2)用NaAlO2溶液制备Al2O3的过程如图。

①“灼烧”时得到了Al2O3,该反应能自发的原因是
②“电解”时阳极用惰性电极,阳极电极反应式为
您最近一年使用:0次
解题方法
6 . 完成下列问题
(1)汽车燃油不完全燃烧时产生 ,有人设想按下列反应除去
,有人设想按下列反应除去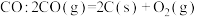 ,已知该反应的
,已知该反应的 ,简述该设想能否实现的依据:
,简述该设想能否实现的依据:___________ 。
(2)超音速飞机在平流层飞行时,尾气中的 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的 和
和 转化成
转化成 和
和 ,化学方程式如下:
,化学方程式如下: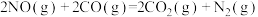 ,反应能够自发进行,则反应的
,反应能够自发进行,则反应的
___________ (填“>”“<”或“=”)0。
(3)工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得到满足不同需求的原料气。在C和 的反应体系中:
的反应体系中:
反应1: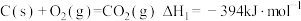
反应2: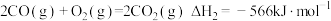
反应3: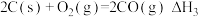
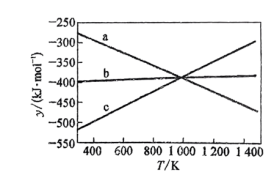
设 ,反应1、2和3的y随温度T的变化关系如图所示,图中对应反应3的线条是
,反应1、2和3的y随温度T的变化关系如图所示,图中对应反应3的线条是___________ (填“a”“b”或“c”)。
(4)一氧化碳变换反应: 。
。
①生产过程中,为了提高变换反应的速率,下列措施中合适的是___________ (填字母)。
A.反应温度越高越好 B.适当增大反应物的压强 C.选择合适的催化剂 D.通入一定量的氮气
②以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离生成MO,能量-反应过程如图所示:
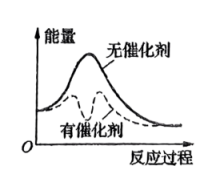
用两个化学方程式表示该催化反应历程(反应机理):
步骤Ⅰ:___________ 。
步骤Ⅱ:___________ 。
(1)汽车燃油不完全燃烧时产生
 ,有人设想按下列反应除去
,有人设想按下列反应除去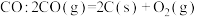 ,已知该反应的
,已知该反应的 ,简述该设想能否实现的依据:
,简述该设想能否实现的依据:(2)超音速飞机在平流层飞行时,尾气中的
 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的 和
和 转化成
转化成 和
和 ,化学方程式如下:
,化学方程式如下: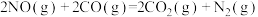 ,反应能够自发进行,则反应的
,反应能够自发进行,则反应的
(3)工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得到满足不同需求的原料气。在C和
 的反应体系中:
的反应体系中:反应1:
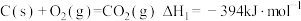
反应2:
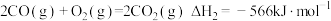
反应3:
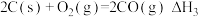
设
 ,反应1、2和3的y随温度T的变化关系如图所示,图中对应反应3的线条是
,反应1、2和3的y随温度T的变化关系如图所示,图中对应反应3的线条是
(4)一氧化碳变换反应:
 。
。①生产过程中,为了提高变换反应的速率,下列措施中合适的是
A.反应温度越高越好 B.适当增大反应物的压强 C.选择合适的催化剂 D.通入一定量的氮气
②以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离生成MO,能量-反应过程如图所示:

用两个化学方程式表示该催化反应历程(反应机理):
步骤Ⅰ:
步骤Ⅱ:
您最近一年使用:0次
7 . 苯乙烯是用于生产苯乙烯系列树脂、丁苯橡胶、离子交换树脂及医药品的原料之一,可通过乙苯的分解制备。
(1)标准状态时,由指定单质生成 物质的焓变称为标准摩尔生成焓,如氨气的标准摩尔生成焓可用
物质的焓变称为标准摩尔生成焓,如氨气的标准摩尔生成焓可用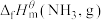 表示。规定
表示。规定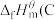 ,石墨
,石墨 和
和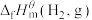 为0,利用标准摩尔生成焓可以求出化学反应热,已知相关物质的标准摩尔生成焓如下表:
为0,利用标准摩尔生成焓可以求出化学反应热,已知相关物质的标准摩尔生成焓如下表:
乙苯分解反应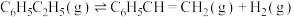 的
的
_______  ,该反应在
,该反应在___________ (填标号)下有利于自发进行。
a.高温 b.低温 c.任何温度
(2)向密闭容器中充入 气态乙苯发生反应
气态乙苯发生反应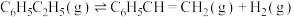 ,其平衡转化率随温度和压强变化的情况如图所示。
,其平衡转化率随温度和压强变化的情况如图所示。
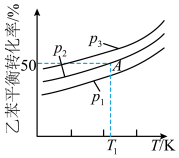
① 由大到小的顺序是
由大到小的顺序是___________ 。
②A点对应的条件下,H2的体积分数为___________ (保留三位有效数字)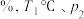 下,该反应的物质的量分数平衡常数[用平衡时各物质的物质的量分数(物质的量分数
下,该反应的物质的量分数平衡常数[用平衡时各物质的物质的量分数(物质的量分数 某组分的物质的量
某组分的物质的量 总物质的量)来代替各物质的平衡浓度,得到的平衡常数称为物质的量分数平衡常数]
总物质的量)来代替各物质的平衡浓度,得到的平衡常数称为物质的量分数平衡常数]
___________ ; 与压强平衡常数
与压强平衡常数 (以分压装示,分压=总压×物质的量分数,
(以分压装示,分压=总压×物质的量分数, 表示总压)的关系为
表示总压)的关系为
___________ (用含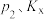 的式子表示)。
的式子表示)。
③向 点平衡体系中加入
点平衡体系中加入 可提高平衡转化率,欲将平衡转化率提高至
可提高平衡转化率,欲将平衡转化率提高至 ,需要向反应器中充入
,需要向反应器中充入___________ 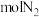 作为稀释气。
作为稀释气。
(1)标准状态时,由指定单质生成
 物质的焓变称为标准摩尔生成焓,如氨气的标准摩尔生成焓可用
物质的焓变称为标准摩尔生成焓,如氨气的标准摩尔生成焓可用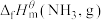 表示。规定
表示。规定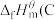 ,石墨
,石墨 和
和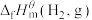 为0,利用标准摩尔生成焓可以求出化学反应热,已知相关物质的标准摩尔生成焓如下表:
为0,利用标准摩尔生成焓可以求出化学反应热,已知相关物质的标准摩尔生成焓如下表:| 物质 | 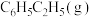 |  |
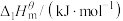 | +29.8 | +147.5 |
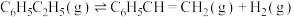 的
的
 ,该反应在
,该反应在a.高温 b.低温 c.任何温度
(2)向密闭容器中充入
 气态乙苯发生反应
气态乙苯发生反应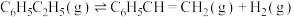 ,其平衡转化率随温度和压强变化的情况如图所示。
,其平衡转化率随温度和压强变化的情况如图所示。
①
 由大到小的顺序是
由大到小的顺序是②A点对应的条件下,H2的体积分数为
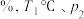 下,该反应的物质的量分数平衡常数[用平衡时各物质的物质的量分数(物质的量分数
下,该反应的物质的量分数平衡常数[用平衡时各物质的物质的量分数(物质的量分数 某组分的物质的量
某组分的物质的量 总物质的量)来代替各物质的平衡浓度,得到的平衡常数称为物质的量分数平衡常数]
总物质的量)来代替各物质的平衡浓度,得到的平衡常数称为物质的量分数平衡常数]
 与压强平衡常数
与压强平衡常数 (以分压装示,分压=总压×物质的量分数,
(以分压装示,分压=总压×物质的量分数, 表示总压)的关系为
表示总压)的关系为
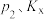 的式子表示)。
的式子表示)。③向
 点平衡体系中加入
点平衡体系中加入 可提高平衡转化率,欲将平衡转化率提高至
可提高平衡转化率,欲将平衡转化率提高至 ,需要向反应器中充入
,需要向反应器中充入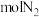 作为稀释气。
作为稀释气。
您最近一年使用:0次
名校
解题方法
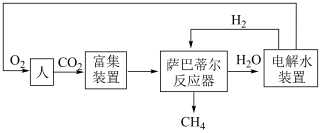
8 . 某空间站利用萨巴蒂尔反应: ,配合水的电解实现氧气再生的流程简图如下。
,配合水的电解实现氧气再生的流程简图如下。
(1)已知:电解液态水制备1mol ,电解反应的
,电解反应的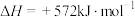 。由此计算
。由此计算 的摩尔燃烧焓
的摩尔燃烧焓
___________  。
。
(2)已知:萨巴蒂尔反应的平衡常数(K)与反应温度(t)之间的关系如图。
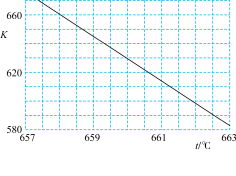
①萨巴蒂尔反应在___________ (选填“高温”或“低温”)下能自发进行。
②某研究小组模拟该反应,温度t下,向容积为10L的密闭容器中通入0.1mol 和0.4mol
和0.4mol ,反应平衡后测得容器中
,反应平衡后测得容器中 。则
。则 的转化率为
的转化率为______ ,反应温度t约为____ ℃。
(3)在相同条件下, 与
与 还会发生不利于氧循环的副反应:
还会发生不利于氧循环的副反应:
 ,在反应器中按
,在反应器中按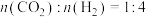 通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中
通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中 、
、 浓度
浓度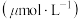 如表。
如表。
若选用催化剂Ⅰ,在350℃条件下反应,0~2min生成 的平均反应速率为
的平均反应速率为_____ 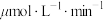 ;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂
;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂___________ (填“Ⅰ”或“Ⅱ”)和
___________ 。
(4)令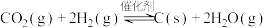 代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是
代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是___________ 。
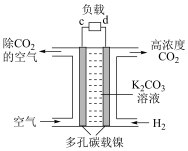
(5)“富集装置”可利用电化学法富集空间站内“空气”中的 作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为
作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为______ 极(填“正”或“负”),b电极上发生的电极反应为___________ 。
 ,配合水的电解实现氧气再生的流程简图如下。
,配合水的电解实现氧气再生的流程简图如下。
(1)已知:电解液态水制备1mol
 ,电解反应的
,电解反应的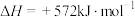 。由此计算
。由此计算 的摩尔燃烧焓
的摩尔燃烧焓
 。
。(2)已知:萨巴蒂尔反应的平衡常数(K)与反应温度(t)之间的关系如图。

①萨巴蒂尔反应在
②某研究小组模拟该反应,温度t下,向容积为10L的密闭容器中通入0.1mol
 和0.4mol
和0.4mol ,反应平衡后测得容器中
,反应平衡后测得容器中 。则
。则 的转化率为
的转化率为(3)在相同条件下,
 与
与 还会发生不利于氧循环的副反应:
还会发生不利于氧循环的副反应: ,在反应器中按
,在反应器中按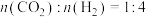 通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中
通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中 、
、 浓度
浓度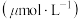 如表。
如表。| 催化剂 | 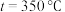 | 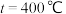 | ||
 |  |  |  | |
| 催化剂Ⅰ | 10.8 | 12722 | 345.2 | 42780 |
| 催化剂Ⅱ | 9.2 | 10775 | 34 | 38932 |
 的平均反应速率为
的平均反应速率为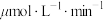 ;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂
;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂
(4)令
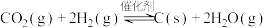 代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是
代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是(5)“富集装置”可利用电化学法富集空间站内“空气”中的
 作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为
作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为
您最近一年使用:0次
名校
解题方法
9 . 工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为: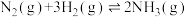
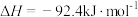 ,
,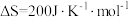 。回答下列问题:
。回答下列问题:
(1)合成氨反应在常温下___________ (填“能”或“不能”)自发。
(2)___________ 温(填“高”或“低”,下同)有利于提高反应速率,________ 温有利于提高平衡转化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用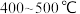 。
。
针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
方案一:双温-双控-双催化剂。使用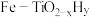 双催化剂,通过光辐射产生温差(如体系温度为495℃时, Fe的温度为:
双催化剂,通过光辐射产生温差(如体系温度为495℃时, Fe的温度为: 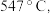 而
而 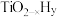 的温度为
的温度为 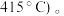
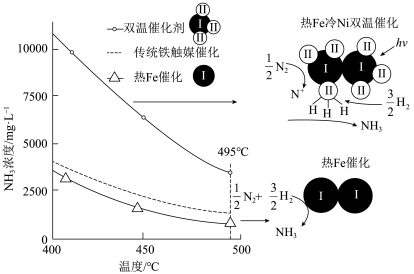
(3)下列说法正确的是___________ 。
a 氨气在“冷Ti”表面生成,有利于提高氨的平衡产率
b. N≡N在“热Fe”表面断裂,有利于提高合成氨反应速率
a.“热Fe”高于体系温度,有利于提高氨的平衡产率
d. “冷 Ti”低于体系温度,有利于提高合成氨反应速率
方案二: 复合催化剂。
复合催化剂。
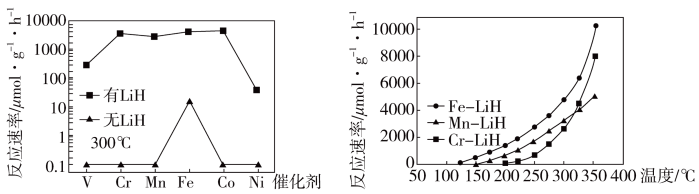
(4)下列说法正确的是___________ 。
a. 300℃时,复合催化剂比单一催化剂效率更高
b. 同温同压下,复合催化剂有利于提高氨的平衡产率
c. 温度越高,复合催化剂活性一定越高
(5)某合成氨速率方程为: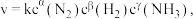 根据表中数据,
根据表中数据,
____________ 。
在合成氨过程中,需要不断分离出氨的原因为___________ 。
a. 有利于平衡正向移动 b. 防止催化剂中毒 c. 提高正反应速率
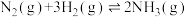
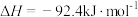 ,
,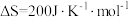 。回答下列问题:
。回答下列问题:(1)合成氨反应在常温下
(2)
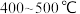 。
。针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
方案一:双温-双控-双催化剂。使用
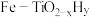 双催化剂,通过光辐射产生温差(如体系温度为495℃时, Fe的温度为:
双催化剂,通过光辐射产生温差(如体系温度为495℃时, Fe的温度为: 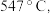 而
而 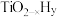 的温度为
的温度为 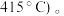

(3)下列说法正确的是
a 氨气在“冷Ti”表面生成,有利于提高氨的平衡产率
b. N≡N在“热Fe”表面断裂,有利于提高合成氨反应速率
a.“热Fe”高于体系温度,有利于提高氨的平衡产率
d. “冷 Ti”低于体系温度,有利于提高合成氨反应速率
方案二:
 复合催化剂。
复合催化剂。
(4)下列说法正确的是
a. 300℃时,复合催化剂比单一催化剂效率更高
b. 同温同压下,复合催化剂有利于提高氨的平衡产率
c. 温度越高,复合催化剂活性一定越高
(5)某合成氨速率方程为:
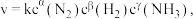 根据表中数据,
根据表中数据,
| 实验 | c(N2)/mol·L-1 | c(H2)/mol·L-1 | c(NH3)/mol·L-1 | v/mol·L-1·s-1 |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
a. 有利于平衡正向移动 b. 防止催化剂中毒 c. 提高正反应速率
您最近一年使用:0次
名校
10 . 化石燃料的综合利用既能减少污染,又能提高资源利用率,回答下列问题:
(1)在一定温度下,向某恒容容器中充入 和
和 ,仅发生反应:
,仅发生反应:
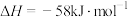 ,
,
①下列情况表明反应已达到平衡状态的是______ (填字母)。
A. 的体积分数保持不变
的体积分数保持不变
B.混合气体的密度保持不变
C. 的转化率保持不变
的转化率保持不变
D. 与
与 的物质的量之比不再改变
的物质的量之比不再改变
②该反应能在______ (填“高温”、“低温”或“任何温度”)下自发。
(2)向2L的恒容密闭容器中充入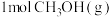 ,发生反应:
,发生反应: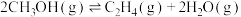
 其他条件不变时,
其他条件不变时, 的平衡转化率随着温度(T)的变化如图所示。
的平衡转化率随着温度(T)的变化如图所示。
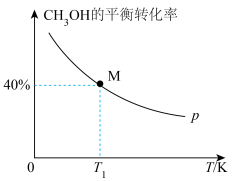
①欲提高 的平衡转化率且加快反应速率,下列措施可能有效的是
的平衡转化率且加快反应速率,下列措施可能有效的是______ (填字母)。
a.降低温度并及时分离出产物
b.加入合适的催化剂并分离出产物
c.再向容器中充入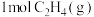
② 时,反应经过20min达到平衡,用
时,反应经过20min达到平衡,用 表示的该段时间内的平均速率为
表示的该段时间内的平均速率为______  ,该温度下,平衡常数
,该温度下,平衡常数
______ ,改变投料,某时刻容器内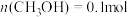 、
、 、
、 ,则此时
,则此时
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(1)在一定温度下,向某恒容容器中充入
 和
和 ,仅发生反应:
,仅发生反应:
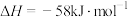 ,
,①下列情况表明反应已达到平衡状态的是
A.
 的体积分数保持不变
的体积分数保持不变B.混合气体的密度保持不变
C.
 的转化率保持不变
的转化率保持不变D.
 与
与 的物质的量之比不再改变
的物质的量之比不再改变②该反应能在
(2)向2L的恒容密闭容器中充入
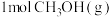 ,发生反应:
,发生反应: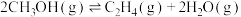
 其他条件不变时,
其他条件不变时, 的平衡转化率随着温度(T)的变化如图所示。
的平衡转化率随着温度(T)的变化如图所示。
①欲提高
 的平衡转化率且加快反应速率,下列措施可能有效的是
的平衡转化率且加快反应速率,下列措施可能有效的是a.降低温度并及时分离出产物
b.加入合适的催化剂并分离出产物
c.再向容器中充入
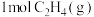
②
 时,反应经过20min达到平衡,用
时,反应经过20min达到平衡,用 表示的该段时间内的平均速率为
表示的该段时间内的平均速率为 ,该温度下,平衡常数
,该温度下,平衡常数
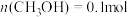 、
、 、
、 ,则此时
,则此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
2023-12-18更新
|
51次组卷
|
2卷引用:内蒙古呼和浩特市第一中学2023-2024学年高二上学期期中考试化学试题



