1 . 25 ℃时,部分物质的电离平衡常数如下表所示:
(1)NH3·H2O的电离方程式是_____________ ,25 ℃时,物质的量浓度为0.10 mol/L的氨水中,c(OH-)=___________ (列出算式即可)。
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa________ (填“>”“<”或“=”)NaClO,请结合题目有关信息说明原因__________ 。
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是_____ ,结合所给数据说明生成该产物的理由__________ 。
化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O |
电离平 衡常数 | Ka=1.75×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Kb=1.8×10-5 |
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是
您最近一年使用:0次
2 . 回答下列问题
(1)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显_______ (填“酸”“碱”或“中”)性,c(CN-)________ (填“>”“<”或“=”)c(HCN)。该溶液中各离子浓度由大到小的顺序为____________ 。
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=______ (小数点后保留4位数字)。
(2)NO2可用氨水吸收生成NH4NO3。25 ℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是___________ (用离子方程式表示)。向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将____________ (填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为____________ mol·L-1(NH3·H2O的电离平衡常数取Kb=2×10-5)。
(3)向氨水中加入0.05 mol·L-1稀硫酸至溶液正好呈中性,则c( )
)________ (填“>”“<”或“=”)2c( ),此时混合溶液中c(NH
),此时混合溶液中c(NH )=176c(NH3·H2O),则NH3·H2O的电离常数Kb为
)=176c(NH3·H2O),则NH3·H2O的电离常数Kb为____________ 。
(4)向10 mL 0.10 mol·L-1的氨水中加入10 mL 0.02 mol·L-1的CaCl2溶液,通过计算说明是否会生成沉淀?____________ 。[已知Ca(OH)2的Ksp=5.5×10-6,氨水中c(OH-)≈ ]
]
(1)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=
(2)NO2可用氨水吸收生成NH4NO3。25 ℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是
(3)向氨水中加入0.05 mol·L-1稀硫酸至溶液正好呈中性,则c(
 )
) ),此时混合溶液中c(NH
),此时混合溶液中c(NH )=176c(NH3·H2O),则NH3·H2O的电离常数Kb为
)=176c(NH3·H2O),则NH3·H2O的电离常数Kb为(4)向10 mL 0.10 mol·L-1的氨水中加入10 mL 0.02 mol·L-1的CaCl2溶液,通过计算说明是否会生成沉淀?
 ]
]
您最近一年使用:0次
解题方法
3 . 某温度下,有浓度均为0.1mol•L-1的下列4种溶液:①NaCN溶液②NaOH溶液③CH3COONa溶液④NaHCO3溶液。
已知:
(1)这4种溶液pH由大到小的顺序是_______ (填序号)。
(2)④的水解平衡常数Kh=_______ 。
(3)此温度下,某HCN和NaCN的混合溶液的pH=11,则 为
为_______ 。
已知:
| HCN | H2CO3 | CH3COOH |
| Ka=5.0×10-10 | Ka1=4×10-7 Ka2=5.0×10-11 | Ka=1.7×10-5 |
(2)④的水解平衡常数Kh=
(3)此温度下,某HCN和NaCN的混合溶液的pH=11,则
 为
为
您最近一年使用:0次
4 . 已知25 ℃时,测得浓度为0.1 mol·L-1的碱BOH的溶液中,c(OH-)=1×10-3 mol·L-1。
(1)写出BOH的电离方程式___________ 。
(2)BOH的电离平衡常数K=___________ 。
(3)某温度t ℃时,BOH的电离平衡常数为1×10-7,结合(2)的计算可知t ℃___________ (填“>”“<”或“=”)25 ℃。若该碱的起始浓度也为0.1 mol·L-1,则溶液中c(B+)=___________ mol·L-1。
(1)写出BOH的电离方程式
(2)BOH的电离平衡常数K=
(3)某温度t ℃时,BOH的电离平衡常数为1×10-7,结合(2)的计算可知t ℃
您最近一年使用:0次
5 . 完成下列问题。
(1)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1,若忽略水的电离及H2CO3的第二级电离,则H2CO3
 +H+的平衡常数K1=
+H+的平衡常数K1=___________ 。(已知:10-5.60=2.5×10-6)
(2)用K2CO3溶液吸收H2S,其原理为 +H2S=HS-+
+H2S=HS-+ 。该反应的平衡常数K=
。该反应的平衡常数K=_______ 。(已知H2CO3的 =4.2×10-7,
=4.2×10-7, =5.6×10-11;H2S的
=5.6×10-11;H2S的 =5.6×10-8,
=5.6×10-8, =1.2×10-15)
=1.2×10-15)
(1)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1,若忽略水的电离及H2CO3的第二级电离,则H2CO3

 +H+的平衡常数K1=
+H+的平衡常数K1=(2)用K2CO3溶液吸收H2S,其原理为
 +H2S=HS-+
+H2S=HS-+ 。该反应的平衡常数K=
。该反应的平衡常数K= =4.2×10-7,
=4.2×10-7, =5.6×10-11;H2S的
=5.6×10-11;H2S的 =5.6×10-8,
=5.6×10-8, =1.2×10-15)
=1.2×10-15)
您最近一年使用:0次
6 . 25 ℃时,0.10 mol·L-1HA溶液中有1%的HA电离,则HA的电离平衡常数Ka为___________ 。
您最近一年使用:0次
7 . 25 ℃时,下列叙述中错误的是
A.0.1 mol·L-1NH4HS溶液中:c <c <c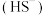 +c +c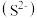 +c +c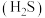 |
B.将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合后,c =c =c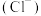 ,则NH3·H2O的电离常数为 ,则NH3·H2O的电离常数为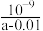 |
| C.10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20 mL |
D.pH相等的① 2SO4溶液,②NH4HSO4溶液,③NH4Cl溶液中,c 2SO4溶液,②NH4HSO4溶液,③NH4Cl溶液中,c 的大小关系:①>③>② 的大小关系:①>③>② |
您最近一年使用:0次
8 . 在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
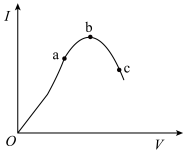
(1)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为___________ 。
(2)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是___________ 。
(3)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是___________ (填字母,下同)。
A.加热 B.加入NaOH稀溶液 C.加入K2CO3固体
D.加水 E.加入CH3COONa固体 F.加入锌粒
(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是___________。

(1)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为
(2)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是
(3)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是
A.加热 B.加入NaOH稀溶液 C.加入K2CO3固体
D.加水 E.加入CH3COONa固体 F.加入锌粒
(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是___________。
| A.c(H+) | B.n(H+) | C.CH3COOH分子数 | D. |
您最近一年使用:0次
2023-08-14更新
|
974次组卷
|
2卷引用:作业(十二) 弱电解质的电离平衡
名校
9 . 醋酸溶液中存在电离平衡:CH3COOH H++CH3COO-。下列叙述不正确的是
H++CH3COO-。下列叙述不正确的是
 H++CH3COO-。下列叙述不正确的是
H++CH3COO-。下列叙述不正确的是| A.0.1 mol·L-1的CH3COOH 溶液加水稀释或加热均可使CH3COO-的物质的量浓度增大 |
| B.0.1 mol·L-1的CH3COOH 溶液加水稀释,c(CH3COO-)·c(H+) 减小 |
| C.向0.1 mol·L-1CH3COOH溶液中加入少量纯醋酸,平衡向右移动,电离程度减小 |
D.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中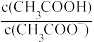 减小 减小 |
您最近一年使用:0次
2023-08-14更新
|
1765次组卷
|
4卷引用:作业(十二) 弱电解质的电离平衡
名校
10 . H2S水溶液中存在电离平衡H2S H++HS-和HS-
H++HS-和HS- H++S2-。下列关于H2S溶液的说法正确的是
H++S2-。下列关于H2S溶液的说法正确的是
 H++HS-和HS-
H++HS-和HS- H++S2-。下列关于H2S溶液的说法正确的是
H++S2-。下列关于H2S溶液的说法正确的是| A.滴加新制氯水,平衡向左移动,溶液pH减小 |
| B.加水,平衡向右移动,溶液中氢离子浓度增大 |
| C.通入过量SO2气体,平衡向左移动,溶液pH增大 |
| D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子的浓度都减小 |
您最近一年使用:0次
2023-08-14更新
|
946次组卷
|
2卷引用:作业(十二) 弱电解质的电离平衡



