名校
1 . 室温下,用含少量 的
的 溶液制备
溶液制备 的过程如题图所示,已知
的过程如题图所示,已知 ,
, 。下列说法正确的是
。下列说法正确的是

 的
的 溶液制备
溶液制备 的过程如题图所示,已知
的过程如题图所示,已知 ,
, 。下列说法正确的是
。下列说法正确的是
A.增大NaF溶液的浓度,可以将 沉淀至浓度为0 沉淀至浓度为0 |
B.“除镁”得到的上层清液中: |
C. 溶液显碱性,则: 溶液显碱性,则: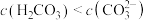 |
D.“沉锰”步骤中的离子方程式为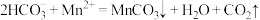 |
您最近一年使用:0次
2023-12-12更新
|
119次组卷
|
2卷引用:湖南省邵东市第三中学2023-2024学年高二上学期第三次月考化学试题
2 . I.实验室由普通锌锰电池的锌皮[主要成分是Zn,还含有少量杂质Fe和粘附的Zn(NH3)2Cl2]为原料制取纳米氧化锌和鸟粪石(MgNH4PO4),其主要实验流程如下:
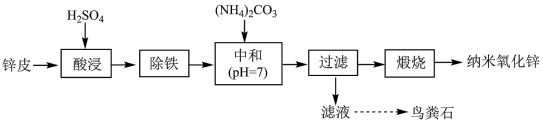
(1)“除铁”包括氧化和沉铁。“氧化”时,向“酸浸”后的溶液中加入过量的双氧水,反应的离子方程式为___________ ;检验“除铁”完全的实验操作是___________ 。
(2)将“过滤”后的滤液与MgSO4、Na2HPO4溶液反应,生成鸟粪石沉淀。
已知常温下:Ksp(MgNH4PO4)=2.5×10-13,Ksp[Mg3(PO4)2]=9.8×10-25,Ksp[Mg(OH)2]=1.8×10-11
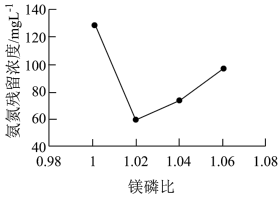
①镁磷比[ ]与氨氮残留浓度的关系如图所示。当镁磷比小于1.02时,随镁磷比的增大,氨氮残留浓度减小的原因是
]与氨氮残留浓度的关系如图所示。当镁磷比小于1.02时,随镁磷比的增大,氨氮残留浓度减小的原因是___________ 。
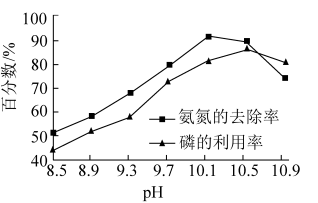
②镁磷比一定,氨氮的去除率和磷的利用率与溶液pH的关系如图所示。当pH为10.1~10.5时,除了生成鸟粪石外,还会生成___________ (填化学式);当pH>10.5时,氨氮去除率和磷的利用率均减小的原因是___________ 。
Ⅱ.室温下,向体积为2L的恒容密闭容器中通入4molH2和1molCO2发生Sabatier反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)(不考虑副反应);若反应时保持温度恒定,测得反应过程中压强随时间的变化如下表所示:
(3)①0~10min内,v(CO2)=___________
②Sabatier反应的速率方程:v正=k正c(CO2)c4(H2),v逆=k逆c(CH4)c2(H2O)(k是速率常数,只与温度有关)。20min时,
___________ 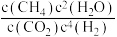 ;反应达平衡时,升高温度,k正增大的倍数
;反应达平衡时,升高温度,k正增大的倍数___________ k逆增大的倍数。(填“>”“<”或“=”)。

(1)“除铁”包括氧化和沉铁。“氧化”时,向“酸浸”后的溶液中加入过量的双氧水,反应的离子方程式为
(2)将“过滤”后的滤液与MgSO4、Na2HPO4溶液反应,生成鸟粪石沉淀。
已知常温下:Ksp(MgNH4PO4)=2.5×10-13,Ksp[Mg3(PO4)2]=9.8×10-25,Ksp[Mg(OH)2]=1.8×10-11
①镁磷比[
 ]与氨氮残留浓度的关系如图所示。当镁磷比小于1.02时,随镁磷比的增大,氨氮残留浓度减小的原因是
]与氨氮残留浓度的关系如图所示。当镁磷比小于1.02时,随镁磷比的增大,氨氮残留浓度减小的原因是
②镁磷比一定,氨氮的去除率和磷的利用率与溶液pH的关系如图所示。当pH为10.1~10.5时,除了生成鸟粪石外,还会生成

Ⅱ.室温下,向体积为2L的恒容密闭容器中通入4molH2和1molCO2发生Sabatier反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)(不考虑副反应);若反应时保持温度恒定,测得反应过程中压强随时间的变化如下表所示:
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强 | 5.00p | 4.60p | 4.30p | 4.15p | 4.06p | 4.00p | 4.00p |
(3)①0~10min内,v(CO2)=
②Sabatier反应的速率方程:v正=k正c(CO2)c4(H2),v逆=k逆c(CH4)c2(H2O)(k是速率常数,只与温度有关)。20min时,

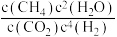 ;反应达平衡时,升高温度,k正增大的倍数
;反应达平衡时,升高温度,k正增大的倍数
您最近一年使用:0次
名校
3 . 回答下列问题
(1)常温下,0.05mol/L硫酸溶液中,pH值为_____ ,水电离的
_____ mol/L。
(2)氨水和稀盐酸反应后的溶液呈中性,所得溶液中的离子浓度大小关系是_____ 。
(3)某温度(t℃)时,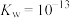 ,将此温度下pH=11的NaOH溶液aL与pH=l的
,将此温度下pH=11的NaOH溶液aL与pH=l的 溶液bL混合,若所得混合溶液为中性,则
溶液bL混合,若所得混合溶液为中性,则
_____ ;
(4)已知 的
的 。则
。则
①某 溶液里
溶液里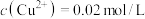 ,如要生成
,如要生成 沉淀,应调整溶液的pH大于
沉淀,应调整溶液的pH大于_____ 。
②要使0.2
 溶液中
溶液中 沉淀完全,则应向溶液里加入NaOH溶液,使溶液的pH为
沉淀完全,则应向溶液里加入NaOH溶液,使溶液的pH为_____ 。
(5)按要求写出下列基态粒子的表示式
Ti的简化电子排布式_____ ,第24号元素的价层电子的轨道表示式_____ 。
(1)常温下,0.05mol/L硫酸溶液中,pH值为

(2)氨水和稀盐酸反应后的溶液呈中性,所得溶液中的离子浓度大小关系是
(3)某温度(t℃)时,
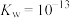 ,将此温度下pH=11的NaOH溶液aL与pH=l的
,将此温度下pH=11的NaOH溶液aL与pH=l的 溶液bL混合,若所得混合溶液为中性,则
溶液bL混合,若所得混合溶液为中性,则
(4)已知
 的
的 。则
。则①某
 溶液里
溶液里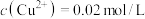 ,如要生成
,如要生成 沉淀,应调整溶液的pH大于
沉淀,应调整溶液的pH大于②要使0.2

 溶液中
溶液中 沉淀完全,则应向溶液里加入NaOH溶液,使溶液的pH为
沉淀完全,则应向溶液里加入NaOH溶液,使溶液的pH为(5)按要求写出下列基态粒子的表示式
Ti的简化电子排布式
您最近一年使用:0次
2023-12-05更新
|
97次组卷
|
2卷引用:湖南省张家界市民族中学2023-2024学年高二上学期第二次月考化学试题
解题方法
4 . 磷酸亚铁锂( )为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池,
)为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池, 废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下:
废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下: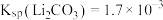
②LiOH、 的溶解度与温度的关系如下表:
的溶解度与温度的关系如下表:
(1)过程I“碱浸”的目的是___________ 。
(2)若浸出液中存在大量 离子,则反应的离子方程式为
离子,则反应的离子方程式为___________ 。
(3)①过程III得到“沉淀Y”的离子方程式为___________ 。
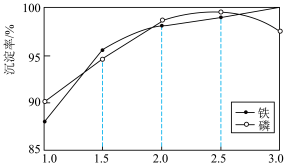
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如下图所示。由图可知,过程III应选取的最佳沉淀时的pH为___________ 。随pH的增加,磷的沉淀率开始下降,而铁沉淀率未下降,分析原因为___________ 。___________ 。
A.NaOH20-40℃ B.NaOH80-100℃
C. 20-40℃ D.
20-40℃ D. 60-80℃
60-80℃
②常温下,测得滤液1中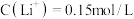 ,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
___________  。
。
 )为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池,
)为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池, 废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下:
废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下: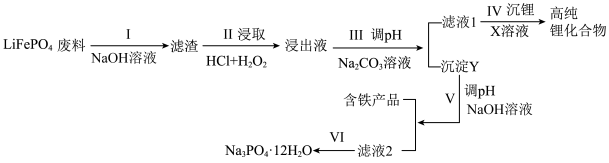
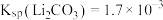
②LiOH、
 的溶解度与温度的关系如下表:
的溶解度与温度的关系如下表:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | LiOH | 11.9 | 12.4 | 13.2 | 14.6 | 16.6 | 19.1 |
 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 | |
(1)过程I“碱浸”的目的是
(2)若浸出液中存在大量
 离子,则反应的离子方程式为
离子,则反应的离子方程式为(3)①过程III得到“沉淀Y”的离子方程式为
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如下图所示。由图可知,过程III应选取的最佳沉淀时的pH为
A.NaOH20-40℃ B.NaOH80-100℃
C.
 20-40℃ D.
20-40℃ D. 60-80℃
60-80℃②常温下,测得滤液1中
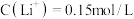 ,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
 。
。
您最近一年使用:0次
2023-12-05更新
|
404次组卷
|
3卷引用:湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题
湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题山西运城新康国际中学2023-2024学年高三上学期一轮复习检测化学试卷(已下线)大题01 化工流程综合题(逐空突破)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
名校
解题方法
5 . 某废钒渣(主要成分为V2O3,含有少量Al2O3、CaO)为原料生产V2O5的工艺流程如图:
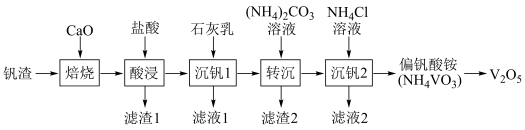
已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为_______ 。
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为_______ 。
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是_______ 。
(4)反应Ca3(VO4)2(s)+3 (aq)⇌2VO
(aq)⇌2VO (aq)+3CaCO3(s)的平衡常数为
(aq)+3CaCO3(s)的平衡常数为_______ (用含m,n的代数式表示),已知:Ksp(CaCO3)=m,Ksp[Ca3(VO4)2]=n。
(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是_______ 。
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLclmol·L-1(NH4)2Fe(SO4)2溶液(VO +2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知
+2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知 被还原为Mn2+,假设杂质不参与反应。
被还原为Mn2+,假设杂质不参与反应。
①滴定时装KMnO4溶液为_______ 滴定管(填“酸式”或“碱式”)
②则产品中V2O5的质量分数是_______ (V2O5的摩尔质量为Mg·mol-1)。
(7)下列操作会导致测定的纯度偏高的是_______。

已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO |  | V2O | VO |
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是
(4)反应Ca3(VO4)2(s)+3
 (aq)⇌2VO
(aq)⇌2VO (aq)+3CaCO3(s)的平衡常数为
(aq)+3CaCO3(s)的平衡常数为(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLclmol·L-1(NH4)2Fe(SO4)2溶液(VO
 +2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知
+2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知 被还原为Mn2+,假设杂质不参与反应。
被还原为Mn2+,假设杂质不参与反应。①滴定时装KMnO4溶液为
②则产品中V2O5的质量分数是
(7)下列操作会导致测定的纯度偏高的是_______。
| A.锥形瓶水洗后未干燥 |
| B.滴定前滴定管尖嘴有气泡,滴定结束无气泡 |
| C.滴定终点时俯视读数 |
| D.滴定管用蒸馏水洗净后未用标准溶液润洗 |
您最近一年使用:0次
名校
解题方法
6 . 工业生产中利用方铅矿(主要成分为PbS,含有 等杂质)制备
等杂质)制备 晶体的工艺流程如图所示。下列说法错误的是
晶体的工艺流程如图所示。下列说法错误的是 难溶于冷水,易溶于热水。
难溶于冷水,易溶于热水。
②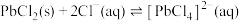
 。
。
③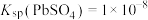 ,
,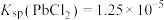 。
。
 等杂质)制备
等杂质)制备 晶体的工艺流程如图所示。下列说法错误的是
晶体的工艺流程如图所示。下列说法错误的是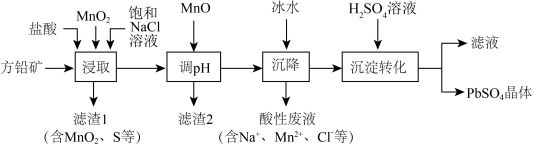
 难溶于冷水,易溶于热水。
难溶于冷水,易溶于热水。②
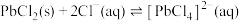
 。
。③
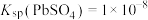 ,
,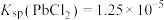 。
。A.“浸取”时加入NaCl的目的是增大 浓度,便于铅元素进入溶液 浓度,便于铅元素进入溶液 |
B.“调pH”时加入MnO,是使平衡 正向移动,除去 正向移动,除去 |
C.“沉降”时加入冰水可使平衡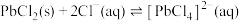 逆向移动 逆向移动 |
D. 经“沉淀转化”后得到 经“沉淀转化”后得到 ,若用 ,若用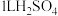 溶液转化 溶液转化 沉淀(忽略溶液体积变化),则 沉淀(忽略溶液体积变化),则 溶液的起始物质的量浓度不得低于 溶液的起始物质的量浓度不得低于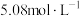 |
您最近一年使用:0次
2023-11-26更新
|
395次组卷
|
4卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期12月阶段性检测化学试题
名校
解题方法
7 . 国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)发电玻璃被誉为“挂在墙上的油田”。一种以镉废渣(含 及少量
及少量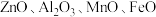 杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
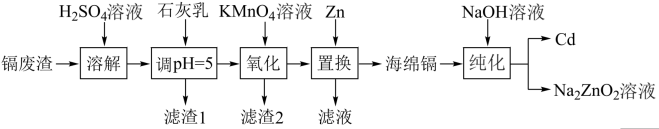
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的 如下表所示:
如下表所示:
 及少量
及少量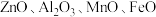 杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的
 如下表所示:
如下表所示:| 金属阳离子 |  |  |  |
开始沉淀时的 | 2.7 | 6.3 | 3.4 |
完全沉淀时的 | 3.2 | 8.3 | 5.0 |
A.滤渣1的主要成分是 |
B. 置换之后的滤液主要成分是 置换之后的滤液主要成分是 和 和 |
C.“纯化”过程中发生的反应为 |
| D.该工艺用到的主要分离操作是过滤 |
您最近一年使用:0次
2023-11-23更新
|
576次组卷
|
4卷引用:湖南省雅礼教育集团2023-2024学年高二上学期期中考试化学试题
名校
解题方法
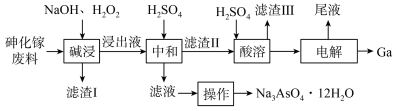
8 . 从砷化镓废料(主要成分为GaAs、 、
、 和
和 )中回收镓和砷的工艺流程如下图所示。下列说法
)中回收镓和砷的工艺流程如下图所示。下列说法不 正确的是
 、
、 和
和 )中回收镓和砷的工艺流程如下图所示。下列说法
)中回收镓和砷的工艺流程如下图所示。下列说法
| A.“碱浸”前,废料先浆化为悬浊液的目的是提高Ga、As元素浸出率 |
B.“碱浸”后,溶液中主要离子有 、 、 、 、 、 、 |
C.滤渣Ⅱ的成分为 和 和 |
D.电解后的尾液中溶质主要成分为 ,可以循环利用 ,可以循环利用 |
您最近一年使用:0次
2023-11-20更新
|
649次组卷
|
4卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题江苏省南通市海安市2023-2024学年高三上学期11月期中化学试题(已下线)江苏省南通市海安高级中学2023-2024学年高三上学期期中考试化学试题江苏省南京市金陵中学2023-2024学年高三上学期期中学业质量监测 化学试卷
名校
解题方法
9 . 钛(Ti)的性质稳定,有良好的耐高温、抗酸碱、高强度、低密度等特性,工业上常用钛铁矿(主要含FeTiO3和少量SiO2、MgO、Al2O3、Fe2O3等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。

已知:①TiO2+易水解,只能存在于强酸性溶液中;
②常温下,相关金属离子开始沉淀和沉淀完全的pH如表所示。
(1)为了提高“酸溶”的速率,可采取的措施有_____ (任写一点)
(2)“酸溶”后,钛主要以TiO2+形式存在,写出相应反应的离子方程式:_____ 。
(3)“分步沉淀”时用氨水逐步调节pH至11.1,依次析出的金属离子是_____ (填离子符号);当Mg2+沉淀完全时,“母液”中Al3+的浓度为_____ mol·L-1。
(4)“水浸”后,过滤、洗涤得水浸渣(TiO2·xH2O),检验TiO2·xH2O已洗涤干净的方法为_____ 。
(5)“氯化”过程在高温下会生成一种有毒气体,写出“氯化”过程的化学方程式_____ 。
(6)“还原”在800~900℃及惰性气体的保护下进行,要在惰性气体的保护下进行的原因是_____ 。

已知:①TiO2+易水解,只能存在于强酸性溶液中;
②常温下,相关金属离子开始沉淀和沉淀完全的pH如表所示。
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 2.2 | 6.5 | 3.5 | 9.5 |
| 沉淀完全(c=1.0×10-5mol/L)的pH | 3.2 | 9.7 | 4.7 | 11.1 |
(1)为了提高“酸溶”的速率,可采取的措施有
(2)“酸溶”后,钛主要以TiO2+形式存在,写出相应反应的离子方程式:
(3)“分步沉淀”时用氨水逐步调节pH至11.1,依次析出的金属离子是
(4)“水浸”后,过滤、洗涤得水浸渣(TiO2·xH2O),检验TiO2·xH2O已洗涤干净的方法为
(5)“氯化”过程在高温下会生成一种有毒气体,写出“氯化”过程的化学方程式
(6)“还原”在800~900℃及惰性气体的保护下进行,要在惰性气体的保护下进行的原因是
您最近一年使用:0次
2023-11-20更新
|
558次组卷
|
2卷引用:湖南省部分校联考2023-2024学年高二上学期期中考试化学试题
名校
10 . 常温下,CaF2、BaF2的沉淀溶解曲线如图所示。下列叙述错误的是
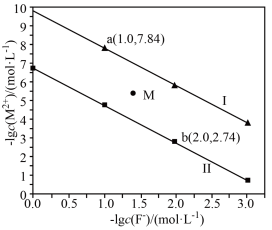
已知:CaF2的溶解度小于BaF2,M代表Ba或Ca

已知:CaF2的溶解度小于BaF2,M代表Ba或Ca
A.曲线Ⅰ代表 与−lgc(F⁻)的关系 与−lgc(F⁻)的关系 |
| B.M点对应的溶液是CaF2的不饱和溶液 |
| C.常温下,Ksp(BaF2)=10-6.74 |
D.BaF2(s)+Ca2+(aq) CaF2(s)+Ba2+(aq)的平衡常数K为103.1 CaF2(s)+Ba2+(aq)的平衡常数K为103.1 |
您最近一年使用:0次
2023-11-20更新
|
459次组卷
|
2卷引用:湖南省部分校联考2023-2024学年高二上学期期中考试化学试题



