1 . 铋 的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为
的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含
,含 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下: 易水解,
易水解, 难溶于冷水。
难溶于冷水。
ii.“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质。
,硫元素转化为硫单质。
iii
 。
。
回答下列问题。
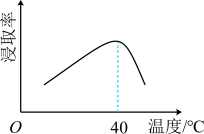
(1)滤渣1的主要成分为______ 。为提高“浸取”速率,采取的措施有:升高温度、__________________ (写出一条)。辉铋矿浸取率随温度的变化曲线如图,高于40℃时浸取率快速下降,其可能的原因是______________________________ 。 和
和 物质的量之比为
物质的量之比为______ 。
(3)“除铜”时发生反应:
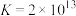 ,则
,则
______ 。
(4)“转化”时,生成 的离子方程式为
的离子方程式为________________________ 。
(5)取 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液使其完全反应,再用
稀溶液使其完全反应,再用
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗
,当溶液紫红色恰好褪去时,消耗 标准溶液。该
标准溶液。该
产品的纯度为______ (用含w,a、b的代数式表示)。
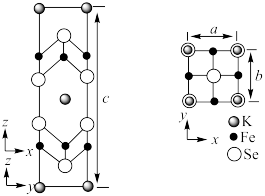
(6)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:__________________ 。
② 的配位数为
的配位数为______ 。
③该晶胞参数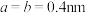 ,
, ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为__________________  (列出计算式)。
(列出计算式)。
 的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为
的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含
,含 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下: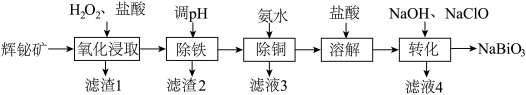
 易水解,
易水解, 难溶于冷水。
难溶于冷水。ii.“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质。
,硫元素转化为硫单质。iii

 。
。回答下列问题。
(1)滤渣1的主要成分为
 和
和 物质的量之比为
物质的量之比为(3)“除铜”时发生反应:

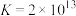 ,则
,则
(4)“转化”时,生成
 的离子方程式为
的离子方程式为(5)取
 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液使其完全反应,再用
稀溶液使其完全反应,再用
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗
,当溶液紫红色恰好褪去时,消耗 标准溶液。该
标准溶液。该产品的纯度为
(6)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
②
 的配位数为
的配位数为③该晶胞参数
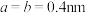 ,
, ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2 . 锰废渣的硫酸浸出液含有大量 、
、 、
、 以及少量的
以及少量的 、
、 、
、 、
、 。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
①萃取剂a和b均为有机物,可用通式HR表示,萃取金属离子时,发生反应: (M代表被萃取的金属)。
(M代表被萃取的金属)。
②已知常温下部分物质的 如表。
如表。
③不同条件下加入 对钙镁去除率的影响如图1、图2。
对钙镁去除率的影响如图1、图2。___________ 。
(2)写出加入 后发生反应的离子方程式
后发生反应的离子方程式___________ 。
(3)滤渣①的主要成分___________ 。
(4)根据图1、图2,选择除去钙镁离子的最适宜温度和pH分别是___________ 、___________ ,如果pH过低带来影响是___________ 。
(5)用平衡移动原理解释加入反萃取剂的作用___________ 。
(6)最后得到 溶液中,调节溶液
溶液中,调节溶液 ,加入
,加入 让
让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于___________ 。[已知: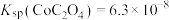 ,
,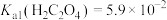 ,
, 结果保留三位小数]
结果保留三位小数]
 、
、 、
、 以及少量的
以及少量的 、
、 、
、 、
、 。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。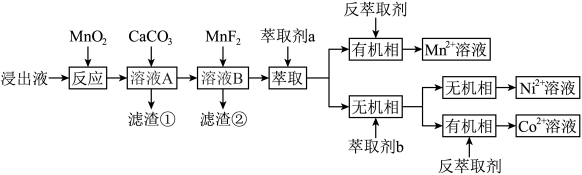
①萃取剂a和b均为有机物,可用通式HR表示,萃取金属离子时,发生反应:
 (M代表被萃取的金属)。
(M代表被萃取的金属)。②已知常温下部分物质的
 如表。
如表。| 物质 |  |  |  |  |  |  |  |
 |  |  |  | 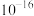 | 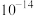 |  |  |
 对钙镁去除率的影响如图1、图2。
对钙镁去除率的影响如图1、图2。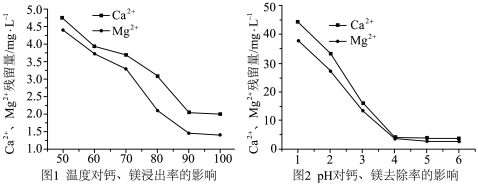
(2)写出加入
 后发生反应的离子方程式
后发生反应的离子方程式(3)滤渣①的主要成分
(4)根据图1、图2,选择除去钙镁离子的最适宜温度和pH分别是
(5)用平衡移动原理解释加入反萃取剂的作用
(6)最后得到
 溶液中,调节溶液
溶液中,调节溶液 ,加入
,加入 让
让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于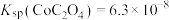 ,
,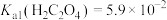 ,
, 结果保留三位小数]
结果保留三位小数]
您最近一年使用:0次
3 . 赤泥是氧化铝生产排放的固体废弃物。由赤泥(主要成分为 、
、 、
、 、FeO、CaO、
、FeO、CaO、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下。
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下。 的空间结构是
的空间结构是______ 。
(2)“焙烧”时,需将赤泥粉碎的目的是______ 。
(3)酸浸渣的主要成分是______ (填化学式)。
(4)“氧化”时发生反应的离子方程式为______ 。室温下,向氧化后的溶液中滴加NaOH溶液至pH=4时,溶液中的
______  [已知25℃,
[已知25℃, 的
的 ]。
]。
(5)为了测试所制得的聚合硫酸铝铁的性能,取某水样,在不同pH条件下加入PAFS 并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析pH<7时,去浊率较低的可能原因是
并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析pH<7时,去浊率较低的可能原因是______ 。______ ,若晶体密度为 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为______ pm(阿伏加德罗常数的值用 表示,写出计算式即可)。
表示,写出计算式即可)。
 、
、 、
、 、FeO、CaO、
、FeO、CaO、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下。
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下。
 的空间结构是
的空间结构是(2)“焙烧”时,需将赤泥粉碎的目的是
(3)酸浸渣的主要成分是
(4)“氧化”时发生反应的离子方程式为

 [已知25℃,
[已知25℃, 的
的 ]。
]。(5)为了测试所制得的聚合硫酸铝铁的性能,取某水样,在不同pH条件下加入PAFS
 并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析pH<7时,去浊率较低的可能原因是
并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析pH<7时,去浊率较低的可能原因是
 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为 表示,写出计算式即可)。
表示,写出计算式即可)。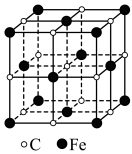
您最近一年使用:0次
名校
4 . 利用含锌废水制备ZnCO3·2Zn(OH)2的工艺流程如图,下列有关说法正确的是
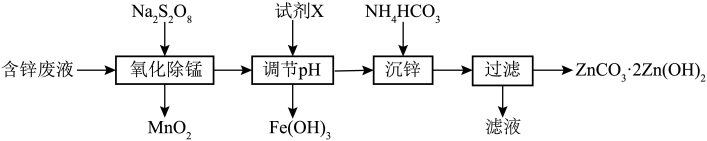
已知:①
②Zn2+ 可以与氨水反应生成[ Zn(NH3)4 ]2+

已知:①
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 |
| Ksp | 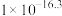 | 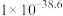 | 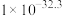 | 1.2 x 10-17 |
| A.Na2S2O8中硫元素的化合价为+7价 |
| B.氧化除锰步骤中氧化剂和还原剂的物质的量之比为2:1 |
C.沉锌时发生反应的离子方程式主要是: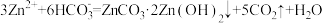 |
| D.调节pH值除铁时,应选用的试剂X为氨水,调节pH值应大于9,以便将铁完全沉淀。 |
您最近一年使用:0次
解题方法
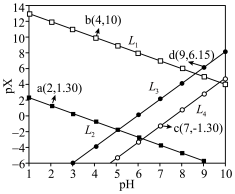
5 . 常温下,分别在 溶液中滴加
溶液中滴加 溶液,溶液
溶液,溶液 代表
代表 ]与
]与 关系如图所示。已知:
关系如图所示。已知: 。
。
 溶液中滴加
溶液中滴加 溶液,溶液
溶液,溶液 代表
代表 ]与
]与 关系如图所示。已知:
关系如图所示。已知: 。
。
A.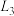 代表 代表 代表 代表 |
B. 的数量级为 的数量级为 |
C.若在同溶液中产生这两种沉淀时, |
D. 的平衡常数 的平衡常数 |
您最近一年使用:0次
名校
6 . 一定温度下, 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中
溶液中 随pH的变化如图1所示,
随pH的变化如图1所示, 溶液中含A微粒的物质的量分数随pH的变化如图2所示。
溶液中含A微粒的物质的量分数随pH的变化如图2所示。
①MA、 均为难溶物;
均为难溶物;
②初始 。
。
下列说法错误的是
 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中
溶液中 随pH的变化如图1所示,
随pH的变化如图1所示, 溶液中含A微粒的物质的量分数随pH的变化如图2所示。
溶液中含A微粒的物质的量分数随pH的变化如图2所示。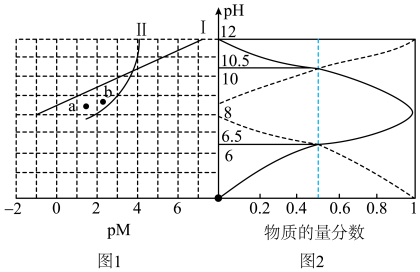
①MA、
 均为难溶物;
均为难溶物;②初始
 。
。下列说法错误的是
A.曲线Ⅰ表示 溶解平衡曲线 溶解平衡曲线 |
B.初始状态a点发生反应: |
C. 时, 时, |
D.初始状态的b点,平衡后溶液中存在 |
您最近一年使用:0次
7 . 298K时,用NaOH溶液分别滴定等物质的量浓度的HR、 、
、 三种溶液。pM[p表示负对数,M表示
三种溶液。pM[p表示负对数,M表示 、
、 、
、 ]随溶液pH变化的关系如图所示。
]随溶液pH变化的关系如图所示。 ,当离子浓度
,当离子浓度 时,该离子完全沉淀。
时,该离子完全沉淀。
下列推断正确的是
 、
、 三种溶液。pM[p表示负对数,M表示
三种溶液。pM[p表示负对数,M表示 、
、 、
、 ]随溶液pH变化的关系如图所示。
]随溶液pH变化的关系如图所示。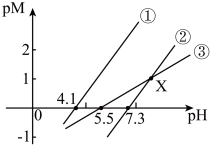
 ,当离子浓度
,当离子浓度 时,该离子完全沉淀。
时,该离子完全沉淀。下列推断正确的是
A.①代表滴定 溶液的变化关系 溶液的变化关系 |
B.调节pH=5时,溶液中 完全沉淀 完全沉淀 |
C.滴定HR溶液至X点时,溶液中: |
D.经计算, 能完全溶于HR溶液 能完全溶于HR溶液 |
您最近一年使用:0次
2024-06-04更新
|
294次组卷
|
5卷引用:湖南师大附中2024届高三下学期第三次模拟考试化学试题
(已下线)湖南师大附中2024届高三下学期第三次模拟考试化学试题2024届河南省五市高三下学期二模理综试题-高中化学2024届四川省成都市第七中学高三下学期5月模拟考试理科综合试题-高中化学(已下线)T13-溶液中的离子平衡2024届四川省射洪中学校高三下学期考前热身理综试题-高中化学
解题方法
8 . 下列实验操作及现象与对应结论不匹配的是
| 实验操作 | 现象 | 结论 | |
| A | 加热麦芽糖和稀硫酸的混合溶液,冷却后加入NaOH溶液至碱性,再加入银氨溶液,加热 | 有银镜产生 | 水解产物中一定含有还原糖 |
| B | 将TiCl4液体和FeCl3固体分别暴露在潮湿空气中 | 只有前者会冒“白烟” | 水解程度:TiCl4>FeCl3 |
| C | 向0.1mol/LNaOH溶液滴入MgSO4溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 |  |
| D | 在硬质试管中对石蜡油加强热,将产生的气体通入酸性KMnO4溶液中 | 酸性KMnO4溶液褪色 | 气体中含有不饱和烃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 已知:常温下, 、
、 、
、 的溶度积依次为
的溶度积依次为 、
、 、
、 ,化学反应中,平衡常数
,化学反应中,平衡常数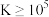 即认为反应能完全进行,不可逆,下列叙述正确的是
即认为反应能完全进行,不可逆,下列叙述正确的是
 、
、 、
、 的溶度积依次为
的溶度积依次为 、
、 、
、 ,化学反应中,平衡常数
,化学反应中,平衡常数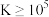 即认为反应能完全进行,不可逆,下列叙述正确的是
即认为反应能完全进行,不可逆,下列叙述正确的是A.溶解度: |
B.向含 废水中加入 废水中加入 ,可完全除去 ,可完全除去 |
C.在含 、 、 、 、 的溶液中通入 的溶液中通入 ,一定最先析出 ,一定最先析出 |
D.在饱和 溶液中, 溶液中, |
您最近一年使用:0次
名校
解题方法
10 . 室温下,用 溶液吸收
溶液吸收 的过程如图所示。
的过程如图所示。 ,
, 。
。
下列说法正确的是
 溶液吸收
溶液吸收 的过程如图所示。
的过程如图所示。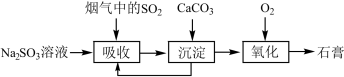
 ,
, 。
。下列说法正确的是
A.吸收烟气后的溶液中: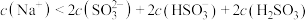 |
B.用0.100 的 的 溶液吸收 溶液吸收 ,当溶液的pH=7时,溶液中: ,当溶液的pH=7时,溶液中: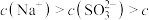  |
| C.检测“氧化”操作得到的产物的实验方案:取少量氧化产物溶于水,静置,在上层清液中滴加氯化钡溶液,若有白色沉淀生成,则说明已被氧化 |
D.“沉淀”操作得到的上层清液中: |
您最近一年使用:0次



