1 . 铊(Tl)本身是一种剧毒物质,为毒性最大的金属元素之一,但是铊在工业中的用途非常广泛,主要存在于一些矿物和工业废水中,也可以从含铊的合金中提取.从某铅锌厂的富铊灰(主要成分为 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示:
①在氯化物-硫酸水溶液中,铊元素以 形式存在;
形式存在;
(2)萃取过程的反应原理为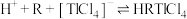 .
.
请回答下列问题:
(1)基态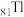 原子核外电子的运动状态有
原子核外电子的运动状态有________ 种.
(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有________________ (写出两条).
(3)写出“浸取I”中 发生反应的化学方程式:
发生反应的化学方程式:________________ ,“滤渣”的主要成分是________ (填化学式).
(4)请从化学平衡的角度解释“反萃取”过程中加入 溶液的原因:
溶液的原因:________________ .
(5)写出“还原氯化沉淀”中反应的离子方程式:________________ .
(6)通过沉淀法也可以去除工业废水中的 和
和 .
.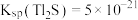 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中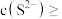
________  (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).
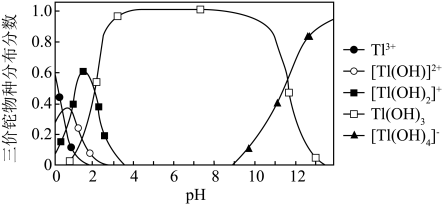
②向含铊废水中加入溴水,使 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是________________ .
 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示: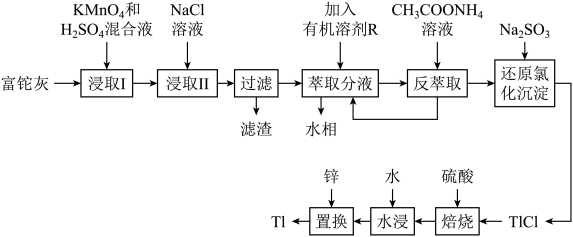
①在氯化物-硫酸水溶液中,铊元素以
 形式存在;
形式存在;(2)萃取过程的反应原理为
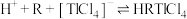 .
.请回答下列问题:
(1)基态
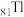 原子核外电子的运动状态有
原子核外电子的运动状态有(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有
(3)写出“浸取I”中
 发生反应的化学方程式:
发生反应的化学方程式:(4)请从化学平衡的角度解释“反萃取”过程中加入
 溶液的原因:
溶液的原因:(5)写出“还原氯化沉淀”中反应的离子方程式:
(6)通过沉淀法也可以去除工业废水中的
 和
和 .
.
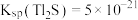 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中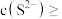
 (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).②向含铊废水中加入溴水,使
 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
您最近一年使用:0次
名校
2 . 利用某钒废渣(主要成分为 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如图。
的工艺流程如图。 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;
Ⅱ. (有机层)
(有机层)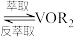 (有机层)
(有机层) ;
;
Ⅲ.溶液中 与
与 可相互转化:
可相互转化: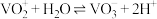 。
。
下列说法错误的是
 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如图。
的工艺流程如图。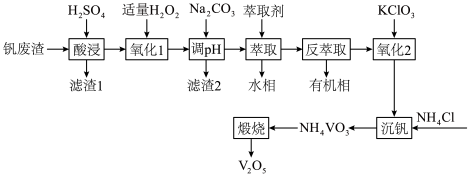
 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;Ⅱ.
 (有机层)
(有机层)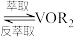 (有机层)
(有机层) ;
;Ⅲ.溶液中
 与
与 可相互转化:
可相互转化: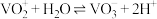 。
。下列说法错误的是
| A.“氧化1”中,不适宜用升温的方式加快转化速率 |
B.“滤渣2”的成分为 |
| C.有机萃取剂可循环使用 |
D.“沉钒”时还需通 调节溶液的酸碱性 调节溶液的酸碱性 |
您最近一年使用:0次
2024-05-28更新
|
519次组卷
|
4卷引用:2024届湖南省湖南大学附属中学高三下学期二模 化学试题
2024届湖南省湖南大学附属中学高三下学期二模 化学试题 (已下线)江苏省姜堰中学、如东中学、前黄中学三校2023-2024学年高三下学期联考化学试题福建省福州市八县市一中2024届高三下学期模拟联考化学试题江苏省部分学校2024届高三下学期高考模拟化学试题
3 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下 中含有的 中含有的 键数为 键数为 |
B. 葡萄糖 葡萄糖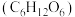 含羟基 含羟基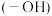 数目为 数目为 |
C.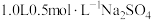 水溶液中含有的氧原子数为 水溶液中含有的氧原子数为 |
D.25℃时, ,则 ,则 饱和溶液中 饱和溶液中 数目为 数目为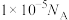 |
您最近一年使用:0次
4 .  可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以独居石为原料制备
等物质。以独居石为原料制备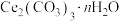 的工艺流程如下:
的工艺流程如下:
 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以独居石为原料制备
等物质。以独居石为原料制备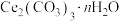 的工艺流程如下:
的工艺流程如下: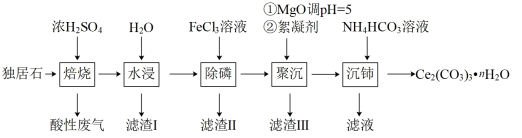
| A.焙烧过程中产生的酸性废气可用于刻蚀玻璃 |
B.滤渣Ⅲ的主要成分是 和 和 |
C.“沉铈”步骤,也可以用 沉淀得到 沉淀得到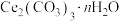 |
D.分离出 的方法为过滤,需用到的玻璃仪器:漏斗、烧杯和玻璃棒 的方法为过滤,需用到的玻璃仪器:漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
5 . 某化学兴趣小组欲探究氢氧化镁固体在氯化铵中溶解的原因,进行了如下实验:
已知:①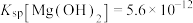 ;②常温下,
;②常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。
关于以上实验,下列说法错误的是
| 操作 | 实验序号 | 试剂X | 实验现象 |
| 实验一 | 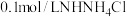 溶液,5.0mL 溶液,5.0mL | 白色浊液逐渐变澄清 |
| 实验二 | 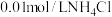 溶液,5.0mL 溶液,5.0mL | 白色浊液变化不明显 | |
| 实验三 | 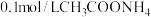 溶液,5.0mL 溶液,5.0mL | 白色浊液逐渐变澄清 | |
| 实验四 | 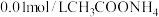 溶液,5.0mL 溶液,5.0mL | 白色浊液变化不明显 | |
| 实验五 | 0.01mol/L蒸馏水,5.0mL | 白色浊液变化不明显 |
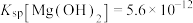 ;②常温下,
;②常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。关于以上实验,下列说法错误的是
| A.只通过实验一和二,氢氧化镁溶解可能是铵根或者氢离子作用的结果 |
B.若加入试剂X为0.1mol/LHCl溶液5mL,实验现象为白色浊液逐渐变澄清,与实验一形成对照,可以说明 被 被 溶解 溶解 |
C.实验三和四中加入 可以排除 可以排除 的干扰,因为 的干扰,因为 溶液显中性 溶液显中性 |
D.通过以上四个实验证明, 溶解的原因是和 溶解的原因是和 形成了更难电离的 形成了更难电离的 |
您最近一年使用:0次
6 . 下列描述对应方程式错误的是
A. 溶液在冷水和热水中颜色不同: 溶液在冷水和热水中颜色不同: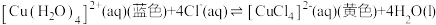  |
B.施加适量石膏降低盐碱地土壤的碱性: |
C.用FeS除去废水中的 : :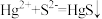 |
D.硅酸钠溶液存放过程中变浑浊: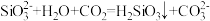 |
您最近一年使用:0次
名校
7 . 一定温度下, 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中pM[
溶液中pM[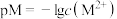 ]随pH的变化如图1,
]随pH的变化如图1, 溶液中含A微粒的物质的量分数随pH的变化如图2。
溶液中含A微粒的物质的量分数随pH的变化如图2。
①MA, 均为难溶物;
均为难溶物;
②初始 。
。
下列说法错误的是
 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中pM[
溶液中pM[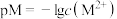 ]随pH的变化如图1,
]随pH的变化如图1, 溶液中含A微粒的物质的量分数随pH的变化如图2。
溶液中含A微粒的物质的量分数随pH的变化如图2。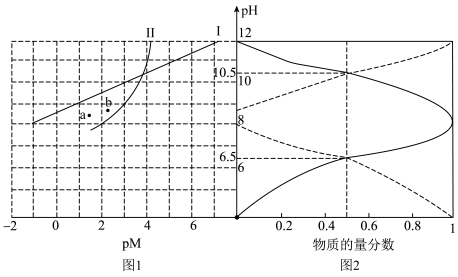
①MA,
 均为难溶物;
均为难溶物;②初始
 。
。下列说法错误的是
A.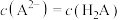 时,pH=8.5 时,pH=8.5 |
B.初始状态a点主要发生反应: |
C.Ⅰ曲线上的点满足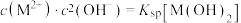 |
D.初始状态的b点,平衡后溶液中存在 |
您最近一年使用:0次
名校
8 . 铬的化合物应用广泛,工业上以铬铁矿(含Al、Si氧化物等杂质)为主要原料制备红矾钠( )的工艺流程如下图。已知:①
)的工艺流程如下图。已知:① 中Cr的化合价为+3;②焙烧的目的是将
中Cr的化合价为+3;②焙烧的目的是将 转化为
转化为 ,并将Al、Si氧化物转化为可溶性钠盐。
,并将Al、Si氧化物转化为可溶性钠盐。
(1)与基态铬原子的最外层电子数相同且同周期的元素有_________ 种。
(2)为了提高“焙烧”效果,可采取的一种措施是____________ 。
(3)“浸取”所得的滤渣为 由此推断
由此推断 “焙烧”时发生主要反应的化学方程式为
“焙烧”时发生主要反应的化学方程式为________ 。
(4)常温下,矿物中相关元素可溶性组分物质的量浓度的对数[ ]与pH的关系如图所示。当溶液中可溶性组分浓度
]与pH的关系如图所示。当溶液中可溶性组分浓度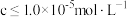 时,可认为已除尽。则“中和”时pH的理论范围为
时,可认为已除尽。则“中和”时pH的理论范围为________ ;“酸化”过程中的离子方程式为____________ 。 的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生
的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生 和
和 沉淀。
沉淀。
①若电解后溶液中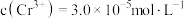 ,则
,则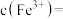
__________  {已知
{已知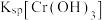
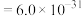 ,
,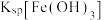 可从第(4)小题图中计算得出}。
可从第(4)小题图中计算得出}。
②电解法处理含 的酸性废水,下列有关原理的说法正确的是
的酸性废水,下列有关原理的说法正确的是_________ (填标号)。
A.阳极反应为
B.电解过程中溶液pH不会变化
C.如果石墨作阳极,电解过程不变
D.电路中每转移12mol电子,阳极有1mol 被还原
被还原
 )的工艺流程如下图。已知:①
)的工艺流程如下图。已知:① 中Cr的化合价为+3;②焙烧的目的是将
中Cr的化合价为+3;②焙烧的目的是将 转化为
转化为 ,并将Al、Si氧化物转化为可溶性钠盐。
,并将Al、Si氧化物转化为可溶性钠盐。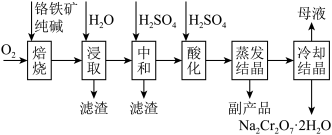
(1)与基态铬原子的最外层电子数相同且同周期的元素有
(2)为了提高“焙烧”效果,可采取的一种措施是
(3)“浸取”所得的滤渣为
 由此推断
由此推断 “焙烧”时发生主要反应的化学方程式为
“焙烧”时发生主要反应的化学方程式为(4)常温下,矿物中相关元素可溶性组分物质的量浓度的对数[
 ]与pH的关系如图所示。当溶液中可溶性组分浓度
]与pH的关系如图所示。当溶液中可溶性组分浓度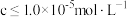 时,可认为已除尽。则“中和”时pH的理论范围为
时,可认为已除尽。则“中和”时pH的理论范围为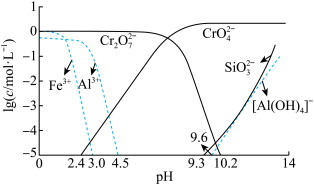
 的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生
的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生 和
和 沉淀。
沉淀。①若电解后溶液中
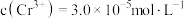 ,则
,则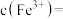
 {已知
{已知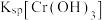
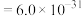 ,
,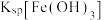 可从第(4)小题图中计算得出}。
可从第(4)小题图中计算得出}。②电解法处理含
 的酸性废水,下列有关原理的说法正确的是
的酸性废水,下列有关原理的说法正确的是A.阳极反应为

B.电解过程中溶液pH不会变化
C.如果石墨作阳极,电解过程不变
D.电路中每转移12mol电子,阳极有1mol
 被还原
被还原
您最近一年使用:0次
9 .  难溶于水,25℃时,不同
难溶于水,25℃时,不同 的溶液中含铅物种存在以下平衡:
的溶液中含铅物种存在以下平衡:
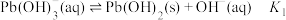 ;
;
 ;
;
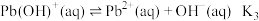 。
。
如图是溶液中各含铅物种的 图。下列说法错误的是
图。下列说法错误的是
 难溶于水,25℃时,不同
难溶于水,25℃时,不同 的溶液中含铅物种存在以下平衡:
的溶液中含铅物种存在以下平衡: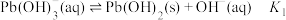 ;
; ;
;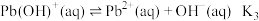 。
。如图是溶液中各含铅物种的
 图。下列说法错误的是
图。下列说法错误的是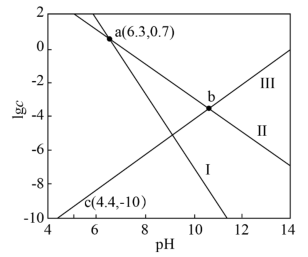
A.直线I和Ⅲ分别表示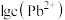 与 与 与 与 的变化关系 的变化关系 |
B. 的平衡常数K的数量级是 的平衡常数K的数量级是 |
C. 饱和溶液的 饱和溶液的 |
D.b点对应溶液的 为10.7 为10.7 |
您最近一年使用:0次
2024-05-24更新
|
205次组卷
|
2卷引用:湖南省长沙市一中2024届高三下学期高考适应性演练(三)化学试题
名校
解题方法
10 . 下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将 固体粉末加入过量 固体粉末加入过量 溶液中,充分搅拌,溶解得到无色溶液 溶液中,充分搅拌,溶解得到无色溶液 |  既体现碱性又体现酸性 既体现碱性又体现酸性 |
| B | 向含有少量FeCl3的MgCl2溶液中加入足量粉MgO末,搅拌一段时间后过滤 | 除去MgCl2溶液中少量FeCl3 |
| C | 向NaCl、NaI混合溶液中滴入少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)大于Ksp(AgI) |
| D | 检验某有机物( | 该有机物中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

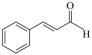 )中是否含有醛基
)中是否含有醛基

