1 . 铍作为一种稀有元素,在航空航天、电子加工等领域具有重要意义。用铍矿石(含BeO及少量Ca、Mg、Mn元素)与配料生产工业氧化铍的工艺流程如下: 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:
(1)若缺少粉碎步骤,产生的影响为_______ 。
(2)烧结时,若铍矿石中BeO恰好转化为 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为_______ 。
(3)水浸后溶液中仍有未反应的 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)水浸后溶液中Mn元素以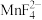 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液______ 时说明反应结束。结合平衡移动原理解释酸洗时控制溶液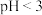 的原因:
的原因:______ 。
(5)碱化时,室温下加入NaOH,控制 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中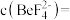
___  。已知
。已知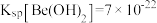 ,
,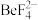 的解离常数
的解离常数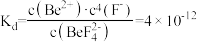
(6)碱化后浸出液中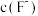 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成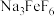 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为____ (填标号)。
A. B.
B. C.
C.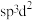
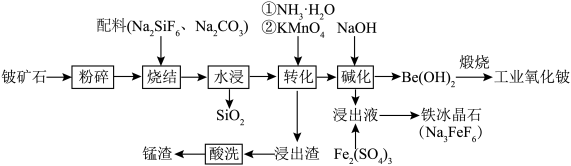
 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:(1)若缺少粉碎步骤,产生的影响为
(2)烧结时,若铍矿石中BeO恰好转化为
 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为(3)水浸后溶液中仍有未反应的
 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为(4)水浸后溶液中Mn元素以
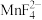 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液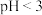 的原因:
的原因:(5)碱化时,室温下加入NaOH,控制
 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中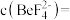
 。已知
。已知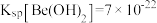 ,
,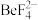 的解离常数
的解离常数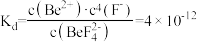
(6)碱化后浸出液中
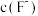 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成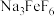 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为A.
 B.
B. C.
C.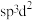
您最近一年使用:0次
解题方法
2 . 25℃时,将含有I-的溶液逐滴加入到含有Hg2+的溶液中,发生一系列可逆反应生成HgI+、HgI2(s)、 、
、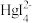 。其中,Hg2+、HgI+、
。其中,Hg2+、HgI+、 、
、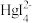 四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
 、
、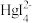 。其中,Hg2+、HgI+、
。其中,Hg2+、HgI+、 、
、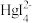 四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是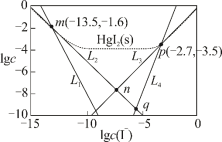
| A.Ksp(HgI2)的数量级为10-28 |
| B.n点的坐标为(-7.15,-7.95) |
C.反应 (aq) (aq) HgI2(s)+I-(aq)的平衡常数为K=10-0.8 HgI2(s)+I-(aq)的平衡常数为K=10-0.8 |
D.q点溶液中存在:c(H+)+2c(Hg2+)=c(OH-)+c(I-)+c(HgI )+c(HgI )+c(HgI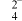 ) ) |
您最近一年使用:0次
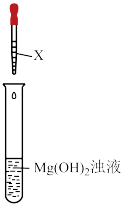
3 . 某化学兴趣小组欲探究氢氧化镁固体在氯化铵中溶解的原因,进行了如下实验:
已知:①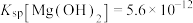 ;②常温下,
;②常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。
关于以上实验,下列说法错误的是
| 操作 | 实验序号 | 试剂X | 实验现象 |
| 实验一 | 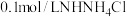 溶液,5.0mL 溶液,5.0mL | 白色浊液逐渐变澄清 |
| 实验二 | 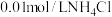 溶液,5.0mL 溶液,5.0mL | 白色浊液变化不明显 | |
| 实验三 | 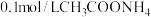 溶液,5.0mL 溶液,5.0mL | 白色浊液逐渐变澄清 | |
| 实验四 | 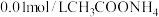 溶液,5.0mL 溶液,5.0mL | 白色浊液变化不明显 | |
| 实验五 | 0.01mol/L蒸馏水,5.0mL | 白色浊液变化不明显 |
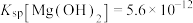 ;②常温下,
;②常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。关于以上实验,下列说法错误的是
| A.只通过实验一和二,氢氧化镁溶解可能是铵根或者氢离子作用的结果 |
B.若加入试剂X为0.1mol/LHCl溶液5mL,实验现象为白色浊液逐渐变澄清,与实验一形成对照,可以说明 被 被 溶解 溶解 |
C.实验三和四中加入 可以排除 可以排除 的干扰,因为 的干扰,因为 溶液显中性 溶液显中性 |
D.通过以上四个实验证明, 溶解的原因是和 溶解的原因是和 形成了更难电离的 形成了更难电离的 |
您最近一年使用:0次
名校
4 .  可用于玻璃和陶瓷的着色剂。由含钴可矿(
可用于玻璃和陶瓷的着色剂。由含钴可矿( 元素主要以
元素主要以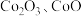 的形式存在,还含有
的形式存在,还含有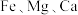 元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示:
元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示: 常用作食品抗氧化剂。
常用作食品抗氧化剂。
②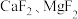 难溶于水。
难溶于水。
③部分金属阳离子形成氢氧化物沉淀的 如表所示:
如表所示:
回答下列问题:
(1)“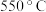 焙烧”的目的是
焙烧”的目的是__________________ 。
(2)“浸取”的过程中, 的主要作用是
的主要作用是__________________ (用离子方程式表示)。若用盐酸代替 和
和 的混合液也能达到目的,从环保角度分析不采用盐酸的原因
的混合液也能达到目的,从环保角度分析不采用盐酸的原因__________________ 。
(3)“滤液1”中加入 溶液,反应过程中氧化剂与还原剂的物质的量之比为
溶液,反应过程中氧化剂与还原剂的物质的量之比为_________ 。
(4)“滤渣2”的主要成分为_________ (填化学式)。
(5)已知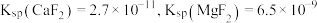 ,当
,当 恰好沉淀完全时(浓度为
恰好沉淀完全时(浓度为 ),溶液中
),溶液中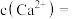
_________ (保留3位有效数字)。
(6)钴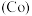 的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含
的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含 的水溶液制备金属钴的装置如图2、3所示。
的水溶液制备金属钴的装置如图2、3所示。 电极应连接乙醇燃料电池的
电极应连接乙醇燃料电池的_________ 极(填“a”或“b”)。
②电解过程中Ⅱ室溶液 变小,则离子交换膜2为
变小,则离子交换膜2为_________ (填“阴”或“阳”)离子交换膜。
 可用于玻璃和陶瓷的着色剂。由含钴可矿(
可用于玻璃和陶瓷的着色剂。由含钴可矿( 元素主要以
元素主要以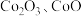 的形式存在,还含有
的形式存在,还含有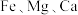 元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示:
元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示: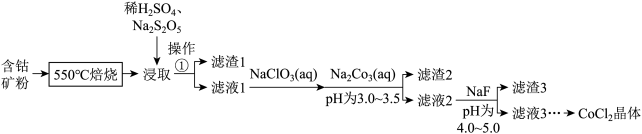
 常用作食品抗氧化剂。
常用作食品抗氧化剂。②
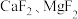 难溶于水。
难溶于水。③部分金属阳离子形成氢氧化物沉淀的
 如表所示:
如表所示:
|
|
|
|
| |
开始沉淀 | 0.3 | 2.7 | 7.2 | 7.6 | 9.6 |
完全沉淀 | 1.1 | 3.2 | 9.2 | 9.6 | 11.1 |
(1)“
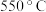 焙烧”的目的是
焙烧”的目的是(2)“浸取”的过程中,
 的主要作用是
的主要作用是 和
和 的混合液也能达到目的,从环保角度分析不采用盐酸的原因
的混合液也能达到目的,从环保角度分析不采用盐酸的原因(3)“滤液1”中加入
 溶液,反应过程中氧化剂与还原剂的物质的量之比为
溶液,反应过程中氧化剂与还原剂的物质的量之比为(4)“滤渣2”的主要成分为
(5)已知
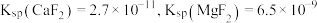 ,当
,当 恰好沉淀完全时(浓度为
恰好沉淀完全时(浓度为 ),溶液中
),溶液中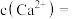
(6)钴
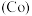 的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含
的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含 的水溶液制备金属钴的装置如图2、3所示。
的水溶液制备金属钴的装置如图2、3所示。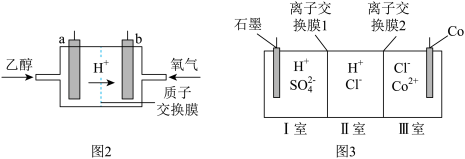
 电极应连接乙醇燃料电池的
电极应连接乙醇燃料电池的②电解过程中Ⅱ室溶液
 变小,则离子交换膜2为
变小,则离子交换膜2为
您最近一年使用:0次
名校
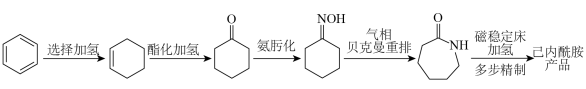
5 . 2023年12月具有完全知识产权、全球首套己内酰胺的绿色生产线正式在中国石化岳阳巴陵石化子公司投产。其生产流程如下:
(1)已知:①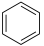
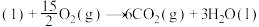
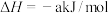
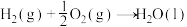

 的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
___________ 。(填写计算式)
Ⅱ.苯选择加氢制环己烯是实现环己酮绿色合成新途径的关键,从热力学的角度来看极为不利,可选择更高效的催化剂,加快环己烯从催化剂的表面脱附,从而提高环己烯的选择性。采用的新型催化剂为:Ru-Zn纳米粒子@BZSS碱式复盐,通过调控BZSS滞水膜厚度进一步提高了环己烯选择性,使用该催化剂使苯的转化率达到70%以上,环己烯的选择性达到80%。已知:苯在水中的溶解度大于环己烯在水中的溶解度,新型负载型催化剂具有亲水性。
(3)请解释Ru-Zn纳米粒子@BZSS碱式复盐能提高环己烯选择性的原因(请从溶解性的角度解释):___________ 。
Ⅲ.中国石化环己酮氨肟化技术以微米级空心TS-1分子筛原粉为催化剂,并成功开发浆态床/膜分离组合新工艺,从而实现微米级催化剂的分离与连续循环使用。该环节中用蒽醌法生产过氧化氢的反应进程如下: 的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。
的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。
(4)有关该反应过程,说法不正确的是___________(填标号)。
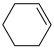
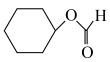
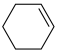
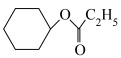
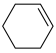
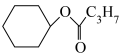
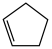
(5)已知环己烯与羧酸发生加成反应的机理如下:
8S3SiIH催化的环烯烃与羧酸加成酯化反应结果
从表格中得出,环己烯与不同羧酸加成,其中与HCOOH反应的产率最高,最有可能的原因是___________ (从分子结构的角度解释)。而环己烯与环戊烯相比,在同样的催化剂条件下,相同温度下,环戊烯加成的产率更高的原因可能是___________ 。
(6)已知在标准状况下,AgCl的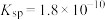 ,
, 的
的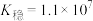 ,若把足量AgCl溶于10mol/L的氨水中,则形成的
,若把足量AgCl溶于10mol/L的氨水中,则形成的 的浓度为
的浓度为___________ mol/L(已知: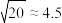 ,结果保留两位有效数字)。
,结果保留两位有效数字)。
(1)已知:①

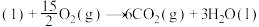
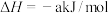
②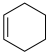
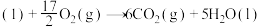
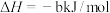
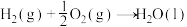

则:
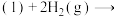

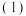

①
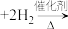
 、
、
②
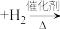
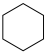 。
。
 的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
Ⅱ.苯选择加氢制环己烯是实现环己酮绿色合成新途径的关键,从热力学的角度来看极为不利,可选择更高效的催化剂,加快环己烯从催化剂的表面脱附,从而提高环己烯的选择性。采用的新型催化剂为:Ru-Zn纳米粒子@BZSS碱式复盐,通过调控BZSS滞水膜厚度进一步提高了环己烯选择性,使用该催化剂使苯的转化率达到70%以上,环己烯的选择性达到80%。已知:苯在水中的溶解度大于环己烯在水中的溶解度,新型负载型催化剂具有亲水性。
(3)请解释Ru-Zn纳米粒子@BZSS碱式复盐能提高环己烯选择性的原因(请从溶解性的角度解释):
Ⅲ.中国石化环己酮氨肟化技术以微米级空心TS-1分子筛原粉为催化剂,并成功开发浆态床/膜分离组合新工艺,从而实现微米级催化剂的分离与连续循环使用。该环节中用蒽醌法生产过氧化氢的反应进程如下:
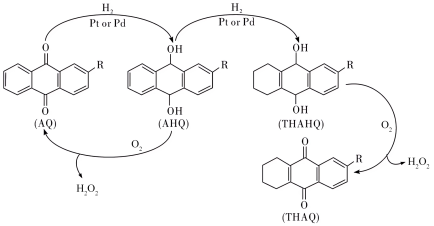
 的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。
的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。(4)有关该反应过程,说法不正确的是___________(填标号)。
A.从AQ到AHQ的反应中,发生变化的碳原子的杂化类型由 到 到 |
B.由THAHQ制备 的反应方程式为 的反应方程式为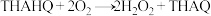 |
C.在AHQ的氧化过程中,生成的 和有机物AQ、AHQ的分离方法为蒸馏 和有机物AQ、AHQ的分离方法为蒸馏 |
| D.我国采用的浆态蒽醌氢化法,使用更高效的Pd基细颗粒催化剂,有利于提高催化的效率 |
(5)已知环己烯与羧酸发生加成反应的机理如下:

8S3SiIH催化的环烯烃与羧酸加成酯化反应结果
| 序号 | 羧酸 | 环烯烃 | 温度/℃ | 产物 | 产率/% |
| 1 | HCOOH |
| 95 |
| 90 |
| 2 |  |
| 110 |
| 82 |
| 3 |  |
| 120 |
| 62 |
| 4 | 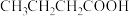 |
| 130 |
| 51 |
| 5 | HCOOH |
| 95 |
| 93 |
(6)已知在标准状况下,AgCl的
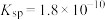 ,
, 的
的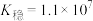 ,若把足量AgCl溶于10mol/L的氨水中,则形成的
,若把足量AgCl溶于10mol/L的氨水中,则形成的 的浓度为
的浓度为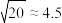 ,结果保留两位有效数字)。
,结果保留两位有效数字)。
您最近一年使用:0次
名校
6 . 湖南稀土资源丰富,其中红土钪矿富含钪元素。钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从红土钪矿(含钪、钛、铁、锰等元素)中提取氧化钪( )的一种流程如下:
)的一种流程如下: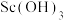 为两性氢氧化物,可与强碱反应生成
为两性氢氧化物,可与强碱反应生成 。
。
②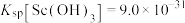 。
。
③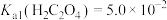 ,
,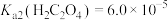 。
。
(1)为提高酸浸速率,可通过研磨、___________ 等措施(举2例)。请从原子结构的角度解释加入双氧水易将酸浸液中某种金属阳离子氧化的原因:___________ 。该步骤中选用足量的 ,理由是
,理由是___________ 。
(2)25℃时加入NaOH溶液调节 以除去
以除去 ,沉锰过程中钪也会经历沉淀的过程,
,沉锰过程中钪也会经历沉淀的过程, 完全沉淀的
完全沉淀的
___________ (已知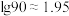 )。
)。
(3)向含 的溶液中加入草酸后可以将其沉淀,
的溶液中加入草酸后可以将其沉淀, 的草酸溶液中
的草酸溶液中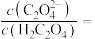
___________ 。
(4)草酸钪在空气中灼烧的化学方程式为___________ 。
(5)Y、Sc(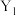 /NC,
/NC,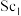 /NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用
/NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用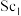 /NC单原子催化剂的反应历程中,决速步的方程式为
/NC单原子催化剂的反应历程中,决速步的方程式为___________ 。
 )的一种流程如下:
)的一种流程如下:
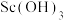 为两性氢氧化物,可与强碱反应生成
为两性氢氧化物,可与强碱反应生成 。
。②
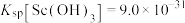 。
。③
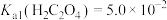 ,
,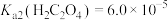 。
。(1)为提高酸浸速率,可通过研磨、
 ,理由是
,理由是(2)25℃时加入NaOH溶液调节
 以除去
以除去 ,沉锰过程中钪也会经历沉淀的过程,
,沉锰过程中钪也会经历沉淀的过程, 完全沉淀的
完全沉淀的
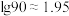 )。
)。(3)向含
 的溶液中加入草酸后可以将其沉淀,
的溶液中加入草酸后可以将其沉淀, 的草酸溶液中
的草酸溶液中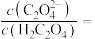
(4)草酸钪在空气中灼烧的化学方程式为
(5)Y、Sc(
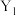 /NC,
/NC, /NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用
/NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用 /NC单原子催化剂的反应历程中,决速步的方程式为
/NC单原子催化剂的反应历程中,决速步的方程式为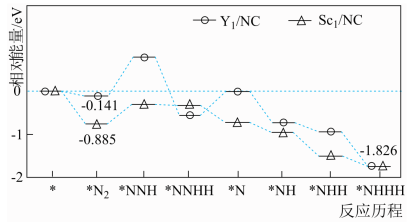
您最近一年使用:0次
名校
7 . 工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、 等)回收Se。
等)回收Se。 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。
②Se难溶于水,沸点684.9℃,易与 反应。
反应。
③反应的 ,代表可完全转化。室温下
,代表可完全转化。室温下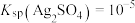 ,
,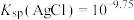 。
。
下列说法正确的是
 等)回收Se。
等)回收Se。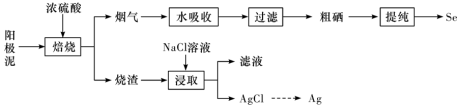
 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。②Se难溶于水,沸点684.9℃,易与
 反应。
反应。③反应的
 ,代表可完全转化。室温下
,代表可完全转化。室温下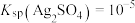 ,
,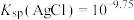 。
。下列说法正确的是
A.理论上,发生反应的 和 和 的物质的量之比为1∶2 的物质的量之比为1∶2 |
| B.在真空中可进行粗硒提纯,可降低体系中硒的沸点 |
C.“滤液”为 溶液 溶液 |
D.加入NaCl溶液浸取时发生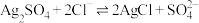 ,该反应过程不可完全转化 ,该反应过程不可完全转化 |
您最近一年使用:0次
名校
解题方法
8 . 化学与生活联系紧密。下列说法错误的是
| A.碳酸钠和碳酸氢钠均可作食用碱或工业用碱 |
| B.抗坏血酸(维生素C)能被氧化为脱氢抗血酸而发挥抗氧化作用 |
| C.水果中因含有低级酯类物质而具有特殊香味 |
| D.牙齿釉质层的主要成分是难溶的羟基磷灰石,属于有机物 |
您最近一年使用:0次
解题方法
9 . GaN是研制高温大功率电子器件和高频微波器件的重要材料。以废旧太阳能电池(主要成分为 )为原料制备GaN的流程如图。请根据所学知识回答问题。
)为原料制备GaN的流程如图。请根据所学知识回答问题。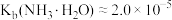 ,
, 。
。
(1) 在315℃开始凝华成有光泽的针状结晶,试推测该结晶的晶体类型:
在315℃开始凝华成有光泽的针状结晶,试推测该结晶的晶体类型:___________ 。
(2)“酸浸氧化”时,温度不宜超过50℃,原因为___________ 。
(3)加氨水调pH的目的是除铜,该步骤中分两步进行,第一步:
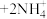 ,第二步是生成的
,第二步是生成的 溶解于氨水。
溶解于氨水。
①根据所给信息,计算第一步反应的平衡常数
___________ 。
②写出 溶解于氨水的离子方程式:
溶解于氨水的离子方程式:___________ 。
(4)“回流过滤”中, (一种液态化合物,遇水易发生水解)与
(一种液态化合物,遇水易发生水解)与 反应的化学方程式为
反应的化学方程式为___________ ;该工序分离 和
和 利用的原理是
利用的原理是___________ 。
(5) 气体在270℃左右以二聚物存在,请写出该二聚物的结构:
气体在270℃左右以二聚物存在,请写出该二聚物的结构:___________ 。
(6)“高温气相沉积”需要将蓝宝石基板(温度高达1000℃)放在沉积炉内,然后以很低的流速将氮化镓气体从上面吹入炉内。研究发现平放基板时氮化镓分子无法稳定沉积到基板上,而将基板按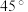 倾角斜放,却获得了非常均匀的氮化镓结晶,试分析其原因:
倾角斜放,却获得了非常均匀的氮化镓结晶,试分析其原因:___________ 。
 )为原料制备GaN的流程如图。请根据所学知识回答问题。
)为原料制备GaN的流程如图。请根据所学知识回答问题。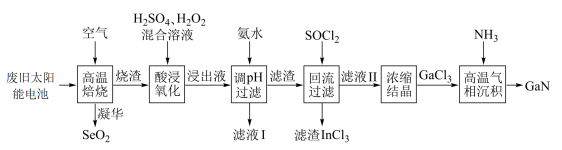
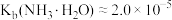 ,
, 。
。(1)
 在315℃开始凝华成有光泽的针状结晶,试推测该结晶的晶体类型:
在315℃开始凝华成有光泽的针状结晶,试推测该结晶的晶体类型:(2)“酸浸氧化”时,温度不宜超过50℃,原因为
(3)加氨水调pH的目的是除铜,该步骤中分两步进行,第一步:

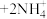 ,第二步是生成的
,第二步是生成的 溶解于氨水。
溶解于氨水。①根据所给信息,计算第一步反应的平衡常数

②写出
 溶解于氨水的离子方程式:
溶解于氨水的离子方程式:(4)“回流过滤”中,
 (一种液态化合物,遇水易发生水解)与
(一种液态化合物,遇水易发生水解)与 反应的化学方程式为
反应的化学方程式为 和
和 利用的原理是
利用的原理是(5)
 气体在270℃左右以二聚物存在,请写出该二聚物的结构:
气体在270℃左右以二聚物存在,请写出该二聚物的结构:(6)“高温气相沉积”需要将蓝宝石基板(温度高达1000℃)放在沉积炉内,然后以很低的流速将氮化镓气体从上面吹入炉内。研究发现平放基板时氮化镓分子无法稳定沉积到基板上,而将基板按
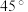 倾角斜放,却获得了非常均匀的氮化镓结晶,试分析其原因:
倾角斜放,却获得了非常均匀的氮化镓结晶,试分析其原因:
您最近一年使用:0次
解题方法
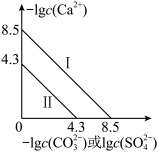
10 . 沉淀的转化在生产中具有重要的应用价值。为了除去水垢中的 ,可先用
,可先用 溶液处理,使
溶液处理,使 转化为疏松、易溶于酸的
转化为疏松、易溶于酸的 ,下列说法正确的是
,下列说法正确的是
已知: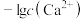 与
与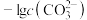 或
或 的关系如图所示,且
的关系如图所示,且 。
。
 ,可先用
,可先用 溶液处理,使
溶液处理,使 转化为疏松、易溶于酸的
转化为疏松、易溶于酸的 ,下列说法正确的是
,下列说法正确的是已知:
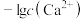 与
与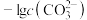 或
或 的关系如图所示,且
的关系如图所示,且 。
。
A. 中 中 的杂化轨道类型是 的杂化轨道类型是 |
B.反应 的平衡常数 的平衡常数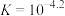 |
C. 中存在的化学键为 中存在的化学键为 键、 键、 键和范德华力 键和范德华力 |
D. 的 的 溶液中,一定存在 溶液中,一定存在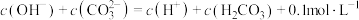 |
您最近一年使用:0次