名校
解题方法
1 . I.现有常温下的3份溶液:
①0.01mol•L-1CH3COOH溶液;②0.01mol•L-1HCl溶液;③pH=12的氨水
(1)3份溶液中,水的电离程度最大的是______ (填序号)。
(2)若②③混合后所得溶液的pH=7,则消耗溶液的体积:②______ ③(填“>”“<”或“=”)。
(3)等体积的①②溶液分别与足量锌粒反应,生成氢气的体积:①______ ②(填“>”“<”或“=”)。
II.NaH2PO4、Na2HPO4可用于合成化工原料三聚磷酸钠(Na5P3O10)。
(4)能说明Na2HPO4溶液显弱碱性的离子方程式为______ 。
(5)测定某三聚磷酸钠试样中Na5P3O10的含量可用间接滴定法,其流程如下:样品1.3000g H3PO4
H3PO4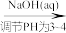 NaH2PO4→配成100.00mL溶液取25.00mL溶液
NaH2PO4→配成100.00mL溶液取25.00mL溶液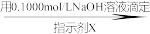 Na2HPO4
Na2HPO4
①滴定时所用的指示剂X可为______ 。
②滴定实验所得数据记录如表(样品中杂质不与酸或碱反应)。
试计算样品中Na5P3O10(Mr=368)的质量分数(结果保留到小数点后一位)______ %。
①0.01mol•L-1CH3COOH溶液;②0.01mol•L-1HCl溶液;③pH=12的氨水
(1)3份溶液中,水的电离程度最大的是
(2)若②③混合后所得溶液的pH=7,则消耗溶液的体积:②
(3)等体积的①②溶液分别与足量锌粒反应,生成氢气的体积:①
II.NaH2PO4、Na2HPO4可用于合成化工原料三聚磷酸钠(Na5P3O10)。
(4)能说明Na2HPO4溶液显弱碱性的离子方程式为
(5)测定某三聚磷酸钠试样中Na5P3O10的含量可用间接滴定法,其流程如下:样品1.3000g
 H3PO4
H3PO4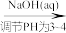 NaH2PO4→配成100.00mL溶液取25.00mL溶液
NaH2PO4→配成100.00mL溶液取25.00mL溶液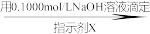 Na2HPO4
Na2HPO4①滴定时所用的指示剂X可为
②滴定实验所得数据记录如表(样品中杂质不与酸或碱反应)。
| 滴定次数 | 待测溶液的体积(mL) | 0.1mol•L-1NaOH溶液的体积 | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
您最近一年使用:0次
2 . 铝及其化合物在生产、生活等方面有广泛的应用。
(1)铝元素位于周期表中第________ 周期________ 族。硼、镓与铝位于同一主族,现有下列三种物质:①NaAlO2、②NaBO2、③NaGaO2,浓度相同的这三种物质的溶液pH由大到小的顺序为________ (用序号表示)。
(2)将20.0 mL 0.1 mol·L-1 Ba(OH)2溶液和20.0 mL 0.1 mol·L-1 NH4Al(SO4)2溶液混合,所得溶液中Al3+、NH 、SO
、SO 、OH-、H+的浓度由大到小的顺序为
、OH-、H+的浓度由大到小的顺序为________________________ 。
(3)氮化铝(AlN)是一种新型的无机非金属材料,可用作热交换器材料。某AlN样品中仅含有Al2O3杂质,为测定AlN的含量,甲组同学设计了如下流程:

已知:AlN+NaOH+H2O=NaAlO2+NH3↑。
①过滤时用到的玻璃仪器有烧杯、漏斗和________ 。
②实验过程中,称得样品的质量为4.2 g,最后得到的固体为5.1 g,则样品中AlN的质量分数为________ 。(不考虑整个过程中的损耗)
(1)铝元素位于周期表中第
(2)将20.0 mL 0.1 mol·L-1 Ba(OH)2溶液和20.0 mL 0.1 mol·L-1 NH4Al(SO4)2溶液混合,所得溶液中Al3+、NH
 、SO
、SO 、OH-、H+的浓度由大到小的顺序为
、OH-、H+的浓度由大到小的顺序为(3)氮化铝(AlN)是一种新型的无机非金属材料,可用作热交换器材料。某AlN样品中仅含有Al2O3杂质,为测定AlN的含量,甲组同学设计了如下流程:

已知:AlN+NaOH+H2O=NaAlO2+NH3↑。
①过滤时用到的玻璃仪器有烧杯、漏斗和
②实验过程中,称得样品的质量为4.2 g,最后得到的固体为5.1 g,则样品中AlN的质量分数为
您最近一年使用:0次
2019-12-05更新
|
213次组卷
|
4卷引用:2016-2017学年山西省临汾一中等三校高二上第二次联考化学试卷
2016-2017学年山西省临汾一中等三校高二上第二次联考化学试卷(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密北京市2020届高三化学一轮复习11月月考化学试题(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练
3 . 碲(Te)及其化合物是重要的半导体材料,碲兼具金属和非金属性质,常用于半导体、合金、化工、橡胶、玻璃等工业;电解法精炼铜的阳极泥是碲的主要来源,经预处理后的阳极泥中含TeO2及铁、铅、铜的化合物等,通过如图所示流程制备高纯碲:

已知:①TeO2是两性氧化物,微溶于水,可溶于强酸或强碱;
②部分难溶物的Ksp如表: (溶液中离子浓度小于10-5 mol/L时,视为沉淀完全)
回答下列问题:
(1)碲是第VIA族元素,其原子结构示意图为_______
(2)滤液中加入Na2S的目的是_______ , 为达到该目的滤液1中c(S2-)≥_______ mol/L。
(3)“沉碲”发生反应的离子方程式为_______ ,此过程用NH4NO3沉碲而不用H2SO4的原因是_______ 。
(4)常温,向0. 1 mol/L Na2TeO3溶液中滴加盐酸,当溶液中c(TeO ):c(H2TeO3) =1:5时,溶液pH=
):c(H2TeO3) =1:5时,溶液pH=_______ 。(已知:H2TeO3的Ka1=1.0×10-3、Ka2=2.0×10-8)
(5)“酸溶” 后,将SO2通入溶液中进行“还原”得到粗碲。若阳极泥中含TeO2的质量分数为8%,提取过程中碲元素无损失,则处理1 kg阳极泥最少需要通入SO2_______ L (标准状况下)。

已知:①TeO2是两性氧化物,微溶于水,可溶于强酸或强碱;
②部分难溶物的Ksp如表: (溶液中离子浓度小于10-5 mol/L时,视为沉淀完全)
| 化合物 | Fe(OH)2 | Pb(OH)2 | Cu(OH)2 | FeS | PbS | CuS |
| Ksp | 8×10-16 | 1.2×10-15 | 1.3×10-20 | 4×10-19 | 1×10-28 | 6×10-36 |
(1)碲是第VIA族元素,其原子结构示意图为
(2)滤液中加入Na2S的目的是
(3)“沉碲”发生反应的离子方程式为
(4)常温,向0. 1 mol/L Na2TeO3溶液中滴加盐酸,当溶液中c(TeO
 ):c(H2TeO3) =1:5时,溶液pH=
):c(H2TeO3) =1:5时,溶液pH=(5)“酸溶” 后,将SO2通入溶液中进行“还原”得到粗碲。若阳极泥中含TeO2的质量分数为8%,提取过程中碲元素无损失,则处理1 kg阳极泥最少需要通入SO2
您最近一年使用:0次
名校
4 . 设 NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1 mol CH4与足量Cl2光照下反应生成CCl4的分子数为 0.1NA |
| B.l mol Na与O2完全反应,转移的电子数一定为NA |
| C.25℃时,pH=1的硫酸溶液中含有的 H+数目为0.1NA |
| D.100 g质量分数为 17%的H2O2溶液中极性键数目为NA |
您最近一年使用:0次
5 . 下列叙述与图像对应符合的是


A.图1表示达到平衡状态的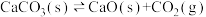  ,在 ,在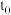 时刻增大压强,平衡逆向移动 时刻增大压强,平衡逆向移动 |
B.对于反应  ,图2中y轴可以表示Y的百分含量 ,图2中y轴可以表示Y的百分含量 |
| C.图3表示等体积、等浓度的盐酸和醋酸溶液分别与过量的Mg反应 |
| D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则HB酸性强 |
您最近一年使用:0次
2022-11-03更新
|
488次组卷
|
2卷引用:浙江省A9协作体2022-2023学年高二上学期期中联考化学试题
名校
解题方法
6 . 某溶液中发生反应的过程中存在Fe2+、 、Fe3+、
、Fe3+、 、H+和水六种微粒,在反应过程中测得Fe3+、
、H+和水六种微粒,在反应过程中测得Fe3+、 的含量随时间变化的曲线如图所示,下列判断错误的是
的含量随时间变化的曲线如图所示,下列判断错误的是

 、Fe3+、
、Fe3+、 、H+和水六种微粒,在反应过程中测得Fe3+、
、H+和水六种微粒,在反应过程中测得Fe3+、 的含量随时间变化的曲线如图所示,下列判断错误的是
的含量随时间变化的曲线如图所示,下列判断错误的是
A. 被还原,发生还原反应 被还原,发生还原反应 | B.还原性:Fe2+> |
| C.还原剂与氧化剂的个数比为6:1 | D.反应后溶液的pH增大 |
您最近一年使用:0次
2022-10-23更新
|
171次组卷
|
2卷引用:黑龙江省哈尔滨市第三中学2022-2023学年高三上学期第二次验收考试化学试题
名校
解题方法
7 . 下列实验过程可以达到实验目的的是( )
| 选项 | 实验目的 | 实验过程 |
| A | 配制一定质量分数的FeCl3溶液 | 将称量好的FeCl3固体用适量的浓盐酸溶解,冷却后加蒸馏水稀释到需要的质量 |
| B | 测定0.1mol•L-1NH4Cl溶液的pH | 用洁净的玻璃棒蘸取少许该溶液滴在湿润的pH试纸上,立刻与标准比色卡比较 |
| C | 在铁制的钥匙表面镀一层金属铜 | 将钥匙和纯铜分别与直流电源的正极和负极相连,同时插入CuSO4溶液中 |
| D | 验证元素非金属性强弱:Cl>P | 比较同浓度的盐酸和磷酸分别与等量同样的Zn粒发生反应的速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 根据信息回答下列问题:
(1)25℃时,将0.02mol/L的Ba(OH)2溶液与物质的量浓度相同的NaHSO4溶液等体积混合,所得的溶液的pH=_______ 。
(2)25℃时,有0.1mol·L-1的四种溶液:①HCl②Na2CO3③CH3COOH④NaOH。上述四种溶液中,其中水的电离程度最大的是_______ (填序号,下同),溶液的pH值由大到小的顺序是_______ 。
(3)向碳酸钠溶液中加入明矾会产生沉淀和气体,反应的离子方程式为:_______ 。
(4)25℃某浓度的NaHCO3溶液的pH=9,则此时溶液中c(CO ):c(HCO
):c(HCO )=
)=_______ 。(已知H2CO3的电离常数:K1=4.4×10-7,K2=4.7×10-11.)
(5)食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于0.035g/mL。选择酚酞作指示剂,用标准NaOH溶液可以测定食醋中醋酸的浓度,以检测白醋是否符合国家标准。某品牌白醋的醋酸浓度测定过程如图所示,回答下列问题:

①滴定达到终点时的现象是_______ 。
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则所用NaOH溶液的体积为_______ mL。

③若通过实验测得稀释后白醋的浓度为0.0600mol·L-1,则该白醋_______ (填“符合”或“不符合”)国家标准。
(1)25℃时,将0.02mol/L的Ba(OH)2溶液与物质的量浓度相同的NaHSO4溶液等体积混合,所得的溶液的pH=
(2)25℃时,有0.1mol·L-1的四种溶液:①HCl②Na2CO3③CH3COOH④NaOH。上述四种溶液中,其中水的电离程度最大的是
(3)向碳酸钠溶液中加入明矾会产生沉淀和气体,反应的离子方程式为:
(4)25℃某浓度的NaHCO3溶液的pH=9,则此时溶液中c(CO
 ):c(HCO
):c(HCO )=
)=(5)食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于0.035g/mL。选择酚酞作指示剂,用标准NaOH溶液可以测定食醋中醋酸的浓度,以检测白醋是否符合国家标准。某品牌白醋的醋酸浓度测定过程如图所示,回答下列问题:

①滴定达到终点时的现象是
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则所用NaOH溶液的体积为

③若通过实验测得稀释后白醋的浓度为0.0600mol·L-1,则该白醋
您最近一年使用:0次
9 . 下列叙述与图象对应符合的是


A.图1表示达到平衡状态的 在 在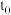 时刻充入了一定量的 时刻充入了一定量的 ,平衡逆向移动 ,平衡逆向移动 |
B.图2表示等体积,等pH值的盐酸和醋酸溶液分别与过量的 反应 反应 |
C.图3表示常温下,稀释 、 、 两种酸的稀溶液时,溶液 两种酸的稀溶液时,溶液 随加水量的变化,则 随加水量的变化,则 酸性强 酸性强 |
D.对于反应  ,若 ,若 ,y可以表示Z的百分含量 ,y可以表示Z的百分含量 |
您最近一年使用:0次
2021-11-05更新
|
364次组卷
|
3卷引用:广东省广州市部分学校2021-2022学年高二上学期期中联考化学试题
10 . “84消毒液”(主要成分为 )作为肺炎疫情的环境消毒剂,是家庭必备品。
)作为肺炎疫情的环境消毒剂,是家庭必备品。
(1)该消毒液呈_______ (填“酸性”、“碱性”或“中性”),原因是_______ (用离子方程式表示)。
(2)该消毒液与洁厕剂(主要成分为盐酸)混合使用会产生黄绿色气体,反应的离子方程式为_______ 。
(3)已知常温下相关弱电解质的电离平衡常数如表:
常温下,pH相同的① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液,三种溶液中溶质的物质的量浓度由大到小的顺序为
溶液,三种溶液中溶质的物质的量浓度由大到小的顺序为_______ (填编号)。
(4)“84消毒液”随放置时间增加逐渐失败,某小组实验测得30℃时,各 不同浓度的“84消毒液”中
不同浓度的“84消毒液”中 的质量百分含量随时间变化如表:
的质量百分含量随时间变化如表:
①由表可知,“84消毒液”失效速率最快的是第_______ (填“Ⅰ”、“Ⅱ”、“Ⅲ”)组,试从碰撞理论角度分析其原因_______ ;
②前8天,第Ⅱ组实验中以 浓度变化表示的平均速率
浓度变化表示的平均速率
_______  (计算结果保留2位有效数字,假定密度为
(计算结果保留2位有效数字,假定密度为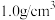 ,忽略溶液体积变化)。
,忽略溶液体积变化)。
 )作为肺炎疫情的环境消毒剂,是家庭必备品。
)作为肺炎疫情的环境消毒剂,是家庭必备品。(1)该消毒液呈
(2)该消毒液与洁厕剂(主要成分为盐酸)混合使用会产生黄绿色气体,反应的离子方程式为
(3)已知常温下相关弱电解质的电离平衡常数如表:
| 化学式 |  |  |  |
| 电离常数 | 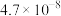 | 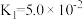 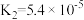 |  |
常温下,pH相同的①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液,三种溶液中溶质的物质的量浓度由大到小的顺序为
溶液,三种溶液中溶质的物质的量浓度由大到小的顺序为(4)“84消毒液”随放置时间增加逐渐失败,某小组实验测得30℃时,各
 不同浓度的“84消毒液”中
不同浓度的“84消毒液”中 的质量百分含量随时间变化如表:
的质量百分含量随时间变化如表: | 0 | 4 | 8 | 12 | 16 | 20 |
| 第Ⅰ组 | 9.0% | 6.5% | 5.1% | 4.1% | 3.4% | 2.8% |
| 第Ⅱ组 | 5.4% | 4.8% | 4.2% | 3.7% | 3.3% | 3.1% |
| 第Ⅲ组 | 2.1% | 2.0% | 1.9% | 1.8% | 1.7% | 1.6% |
①由表可知,“84消毒液”失效速率最快的是第
②前8天,第Ⅱ组实验中以
 浓度变化表示的平均速率
浓度变化表示的平均速率
 (计算结果保留2位有效数字,假定密度为
(计算结果保留2位有效数字,假定密度为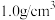 ,忽略溶液体积变化)。
,忽略溶液体积变化)。
您最近一年使用:0次



