解题方法
1 . 草酸亚铁晶体 FeC2O4·2H2O (其相对分子质量为180)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:


(1)仪器A的名称是_______ 。
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是(用化学方程式表示)_______ 。
(3)“洗涤”步骤的操作方法_______ 。
(4)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量稀硫酸溶解,用0.05000mol·L-1酸性KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液15.00mL。计算样品中FeC2O4·2H2O的纯度_______ (保留四位有效数字)
(5)实验中烘干后得到的草酸亚铁晶体FeC2O4·2H2O,称取5.40 g该样品在氩气气氛中进行热重法分析,得到剩余固体的质量随温度变化的曲线如图所示:

①上述FeC2O4·2H2O在氩气气氛进行热重法分析的原因是_______ 。
②分析图中数据,根据信息写出B对应的产物为_______ (填化学式)。
③600℃时剩余固体只有一种铁的氧化物, 且生成两种物质的量相等的气体。试写出B至C进程中所发生的化学反应方程式_______ 。


(1)仪器A的名称是
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是(用化学方程式表示)
(3)“洗涤”步骤的操作方法
(4)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量稀硫酸溶解,用0.05000mol·L-1酸性KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液15.00mL。计算样品中FeC2O4·2H2O的纯度
(5)实验中烘干后得到的草酸亚铁晶体FeC2O4·2H2O,称取5.40 g该样品在氩气气氛中进行热重法分析,得到剩余固体的质量随温度变化的曲线如图所示:

①上述FeC2O4·2H2O在氩气气氛进行热重法分析的原因是
②分析图中数据,根据信息写出B对应的产物为
③600℃时剩余固体只有一种铁的氧化物, 且生成两种物质的量相等的气体。试写出B至C进程中所发生的化学反应方程式
您最近一年使用:0次
解题方法
2 . 湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。Ag+与Cl-可结合生成多种络合物,在水溶液中存在如下平衡:AgCl43-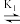 AgCl32-
AgCl32-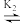 AgCl2-
AgCl2-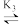 AgCl
AgCl Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是

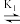 AgCl32-
AgCl32-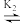 AgCl2-
AgCl2-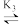 AgCl
AgCl Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
| A.25℃时,Ksp(AgCl)=10-5.08 |
B.曲线c表示AgCl |
C.当c(Cl-)=10-2mol·L-1时,溶液中(AgCl )>c(Ag+)>c(AgCl )>c(Ag+)>c(AgCl ) ) |
| D.25℃时,平衡常数K2=10-0.2 |
您最近一年使用:0次
3 . 根据下列实验操作和现象,得到的结论错误的是
选项 | 实验操作和现象 | 结论 |
A | 向盛 溶液的试管中滴加 溶液的试管中滴加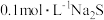 溶液至不再有白色沉淀产生,再向其中滴加 溶液至不再有白色沉淀产生,再向其中滴加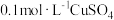 溶液,白色沉淀转化为黑色沉淀 溶液,白色沉淀转化为黑色沉淀 | 证明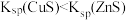 |
B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,有白色沉淀生成,溶液红色变浅 | 证明纯碱溶液呈碱性是由CO 水解引起的 水解引起的 |
C | 向淀粉溶液中加适量20%H2SO4溶液,加热,冷却后加NaOH溶液至碱性,再滴加少量碘水,溶液未变蓝 | 淀粉完全水解 |
D | 压缩装有H2、I2(g)和HI混合气体(已平衡)的密闭容器,观察到气体颜色加深 | 无法证明平衡发生了移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列离子方程书写错误的是
| A.向 FeI2、FeBr2的混合溶液中通入少量氯气:2I-+Cl2= I2+2Cl- |
B.过量Ca(HCO3)2溶液与Ca(OH)2溶液反应:HCO + Ca2+ + OH- = CaCO3↓ + H2O + Ca2+ + OH- = CaCO3↓ + H2O |
C.向 NaHCO3溶液中加入氯化铁溶液:3HCO +Fe3+ =3CO2↑+Fe(OH)3↓ +Fe3+ =3CO2↑+Fe(OH)3↓ |
| D.AgCl悬浊液中滴入Na2S溶液:2Ag++S2- =Ag2S↓ |
您最近一年使用:0次
名校
解题方法
5 . 碲(Te)广泛用于太阳能、电子、医药等领域,对碲的综合回收利用尤为重要。工业上,从含碲化亚铜的废渣(主要成分Cu2Te,还有少量的Ag、Cu)中提取碲的流程如图:

回答下列问题:
(1)写出碲元素在元素周期表中的位置____ 。
(2)“酸浸”过程中生成TeOSO4的离子方程式为____ 。
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgCl)=1.8×10-10。向含Ag2SO4滤渣中加入浓盐酸,Ag2SO4能否充分转化为AgCl?通过计算说明____ 。
(4)电解除铜时,铜、碲沉淀的关系如表。
①电解初始阶段阴极的电极反应式是____ 。
②最佳电解时间为30min,原因是____ 。
(5)向“滤液II”中通入SO2反应一段时间后,Te(IV)的浓度从5.0g/L下降到0.2g/L,写出TeOSO4生成Te的化学方程式____ ,其中Te元素的回收率为____ (忽略溶液体积变化,结果用百分数表示,保留二位有效数字)。
(6)整个过程中可循环利用的物质为____ (填化学式)。

回答下列问题:
(1)写出碲元素在元素周期表中的位置
(2)“酸浸”过程中生成TeOSO4的离子方程式为
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgCl)=1.8×10-10。向含Ag2SO4滤渣中加入浓盐酸,Ag2SO4能否充分转化为AgCl?通过计算说明
(4)电解除铜时,铜、碲沉淀的关系如表。
| 电解时间(min) | 铜沉淀率 | 碲沉淀率 |
| 10 | 25% | 0.1% |
| 20 | 40% | 0.2% |
| 30 | 62% | 0.4% |
| 40 | 65% | 2.0% |
②最佳电解时间为30min,原因是
(5)向“滤液II”中通入SO2反应一段时间后,Te(IV)的浓度从5.0g/L下降到0.2g/L,写出TeOSO4生成Te的化学方程式
(6)整个过程中可循环利用的物质为
您最近一年使用:0次
2022-05-05更新
|
667次组卷
|
3卷引用:江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题
江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题(已下线)微专题28 有关工艺流程和实验探究方程式的书写-备战2023年高考化学一轮复习考点微专题陕西师范大学附属中学、渭北中学等2022-2023学年高三上学期期初检测化学联考试题
名校
解题方法
6 . 下列指定反应的离子方程式正确的是
A.向Ba(OH)2溶液中加入过量NH4HSO4溶液:Ba2++2OH-+NH +H++SO +H++SO =BaSO4↓+NH3·H2O+H2O =BaSO4↓+NH3·H2O+H2O |
B.向PbS固体中滴加硫酸铜溶液:Cu2++SO +PbS=CuS+PbSO4 +PbS=CuS+PbSO4 |
| C.将Fe(OH)3固体溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
D.苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+CO |
您最近一年使用:0次
2022-05-05更新
|
940次组卷
|
7卷引用:江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题
江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题东北育才学校超常教育实验部(少32届)2022届高三第十次模拟考试化学试题(已下线)专题03离子反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题03离子反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题03离子反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题03 离子反应-三年(2020-2022)高考真题分项汇编湖南省永州市第一中学2023届高三下学期第五次月考化学试题
解题方法
7 . 下列有关实验操作、现象及结论都正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝色 | Fe3+的氧化性比I2的强 |
| B | 将淀粉和稀硫酸混合加热一段时间后,再加入新制的Cu(OH)2悬浊液,加热 | 产生砖红色沉淀 | 淀粉在稀硫酸、加热条件下水解为葡萄糖 |
| C | 取一支试管装入2 mL2 mol/LNaOH溶液,先滴加1 mL1 mol/LMgCl2溶液,溶液再滴加几滴1mol/LCuCl2 | 先生成白色沉淀,后沉淀变为蓝色 | Ksp[Cu(OH)2<Ksp[Mg(OH)2 |
| D | 两支试管各盛4mL0.1mol/L酸性高锰酸钾溶液,分别加入2mL0.1mol/L的草酸溶液和2mL0.2mol/L草酸溶液 | 加入0.2mol/L草酸溶液的试管中,高锰酸钾溶液完全褪色时间更短 | 反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 以碳酸锰铜矿(主要成分为MnCO3、CuCO3,还含有Fe2O3、FeO等杂质)为原料制备硫酸锰的一种工艺流程如下:
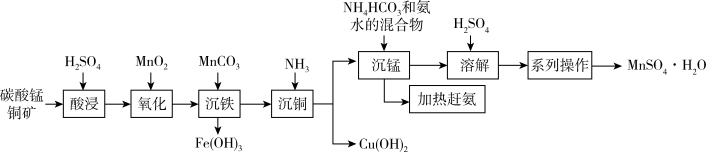
(1)“氧化”时,反应的离子方程式为_______ 。可用一种试剂检验氧化后的溶液中是否含有Fe2+,该试剂为_______ (写化学式)。
(2)加入MnCO3调节pH=3.3时可以将Fe3+转化为Fe(OH)3而除去,该反应的离子方程式为_______ 。
(3)“沉铜"时,若滤液中c(Mn2+)=0.21mol·L-1,向其中缓慢通入氨气,为了使铜离子完全沉淀而又避免生成Mn(OH)2,应控制pH的范围为_______ 。[已知:常温下,Ksp[Cu(OH)2]=1×10-20,Ksp[Mn(OH)2]=2.1×10-13,离子浓度小于或等于10-5mol/L可视为沉淀完全]
(4)本工艺中可循环使用的物质是_______ 。
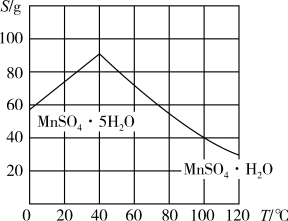
(5)结合图象,分析获得(MnSO4·H2O)晶体的“系列操作”步骤为:_______ 、_______ ,酒精洗涤,低温干燥。

(1)“氧化”时,反应的离子方程式为
(2)加入MnCO3调节pH=3.3时可以将Fe3+转化为Fe(OH)3而除去,该反应的离子方程式为
(3)“沉铜"时,若滤液中c(Mn2+)=0.21mol·L-1,向其中缓慢通入氨气,为了使铜离子完全沉淀而又避免生成Mn(OH)2,应控制pH的范围为
(4)本工艺中可循环使用的物质是
(5)结合图象,分析获得(MnSO4·H2O)晶体的“系列操作”步骤为:

您最近一年使用:0次
2022-04-13更新
|
677次组卷
|
6卷引用:江西省九江市2022届第二次高考模拟统一考试理综化学试题
江西省九江市2022届第二次高考模拟统一考试理综化学试题江西省安义中学2022-2023学年高三上学期中考试化学试题(已下线)专题15工艺流程题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题16工艺流程题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
9 . 铊(Tl)在工业中的用途非常广泛,其中铊锡合金可作超导材料:铊镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、Fe2O3、 FeO、Tl2O等)中提炼,具体工艺流程如图。
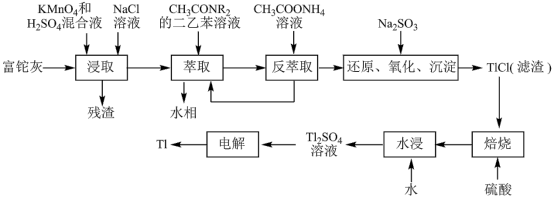
已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H+ +CH3CONR2+TlCl
 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。
回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供H+,另一作用为_______ 。
(2)在实验室中,“萃取”过程使用的玻璃仪器有_______ ,用平衡移动解释“反萃取”过程的原理和目的_______ 。
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为_______ ,为提高经济效益充分利用原料,该反应的滤液可加入_______ 步骤循环使用最合适。
(4)Tl+对人体毒性很大,难溶盐KFe[Fe(CN)6]可通过离子交换治疗Tl2SO4中毒,将其转化为沉淀同时生成K2SO4溶液,写出治疗Tl2SO4中毒的离子方程式:_______ 。
(5)电解Tl2SO4溶液制备金属Tl的装置如图所示。石墨(C)上电极反应式为_______ 。


已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H+ +CH3CONR2+TlCl

 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供H+,另一作用为
(2)在实验室中,“萃取”过程使用的玻璃仪器有
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为
(4)Tl+对人体毒性很大,难溶盐KFe[Fe(CN)6]可通过离子交换治疗Tl2SO4中毒,将其转化为沉淀同时生成K2SO4溶液,写出治疗Tl2SO4中毒的离子方程式:
(5)电解Tl2SO4溶液制备金属Tl的装置如图所示。石墨(C)上电极反应式为

您最近一年使用:0次
2022-04-10更新
|
765次组卷
|
2卷引用:江西省八所重点中学2022届高三联考理科综合化学试题
名校
10 . 已知SrF2属于难溶于水、可溶于酸的盐。常温下,用HCl调节SrF2浊液的pH,测得在不同pH条件下,体系中-1gc(X)(X为Sr2+或F-)与1g[ ]的关系如图所示。
]的关系如图所示。

下列说法错误的是
 ]的关系如图所示。
]的关系如图所示。
下列说法错误的是
A.L1代表-lgc(Sr2+)与lg[ ]的变化曲线 ]的变化曲线 |
| B.Ksp(SrF2)的数量级为10-9 |
| C.a、c两点的溶液中均存在2c(Sr2+)=c(F-)+c(HF) |
| D.c点的溶液中存在c(Cl-)>c(Sr2+)=c(HF)>c(H+) |
您最近一年使用:0次
2022-03-11更新
|
2215次组卷
|
7卷引用:江西师范大学附属中学2022届高三下学期三模理科综合化学试题
江西师范大学附属中学2022届高三下学期三模理科综合化学试题河北省石家庄市2021-2022学年下学期高中毕业班教学质量检测(一)化学试题山东省泰安市2022届高三二轮验收考试化学试题(已下线)专题13 水溶液中的离子平衡-备战2023年高考化学母题题源解密(全国通用)山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题广东省茂名市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)T13-溶液中的离子平衡



