1 . 已知K、Ka、Kw、Kh、Ksp分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是_____________ .
a.它们都能反映一定条件下对应变化进行的程度
b.它们的大小都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
d.一定温度下,在CH3COONa溶液中KW=Ka·Kh
(2)25℃时,将a mol·L−1的氨水与0.01mol·L−1的盐酸等体积混合所得溶液中c(NH4 +)=c(Cl−),则溶液显____________ (填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离平衡常数Kb=_______________ .
(3)25℃时,H2SO3⇌HSO3−+H+的电离常数Ka=1×10−2mol·L−1,则该温度下pH=3、c(HSO3−)=0.1mol·L−1的NaHSO3溶液中c(H2SO3)=_____________________ ,
已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0×10−38、1.0×10−11,向浓度均为0.1mol/L的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是__________________ .(已知lg 2=0.3)
(1)有关上述常数的说法正确的是
a.它们都能反映一定条件下对应变化进行的程度
b.它们的大小都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
d.一定温度下,在CH3COONa溶液中KW=Ka·Kh
(2)25℃时,将a mol·L−1的氨水与0.01mol·L−1的盐酸等体积混合所得溶液中c(NH4 +)=c(Cl−),则溶液显
(3)25℃时,H2SO3⇌HSO3−+H+的电离常数Ka=1×10−2mol·L−1,则该温度下pH=3、c(HSO3−)=0.1mol·L−1的NaHSO3溶液中c(H2SO3)=
已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0×10−38、1.0×10−11,向浓度均为0.1mol/L的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是
您最近一年使用:0次
名校
解题方法
2 . Ⅰ.在0.1 mol·L-1的重铬酸钾(K2Cr2O7)溶液中存在如下平衡:
Cr2O72-+H2O 2HCrO4
2HCrO4 2CrO42-+2H+
2CrO42-+2H+
(1)重铬酸钾溶液呈______ 性,在强碱溶液中,铬元素的主要存在形式为________ (填离子符号),向重铬酸钾溶液中加入适量稀硫酸,溶液中c(Cr2O72-)/c(CrO42-)将______ (填“增大”、“减小”或“不变”)。
Ⅱ.已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)若溶液中只溶解了一种溶质,则该溶质是________ ,上述四种离子浓度的大小顺序为________ (选填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为________ ;
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_______ c(NH3·H2O) (填“大于”“小于”或“等于”)。
III.重金属离子对河流海洋造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含有Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1。排放前拟用沉淀法除去这两种
离子,查找有关数据如下:
(1)你认为往废水中投入________________ (填字母序号),沉淀效果最好。
A. NaOH B.Na2S C.KI D. Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=_______ 。
Cr2O72-+H2O
 2HCrO4
2HCrO4 2CrO42-+2H+
2CrO42-+2H+(1)重铬酸钾溶液呈
Ⅱ.已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)若溶液中只溶解了一种溶质,则该溶质是
(2)若上述关系中③是正确的,则溶液中的溶质为
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
III.重金属离子对河流海洋造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含有Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1。排放前拟用沉淀法除去这两种
离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
(1)你认为往废水中投入
A. NaOH B.Na2S C.KI D. Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
您最近一年使用:0次
2018-11-19更新
|
417次组卷
|
2卷引用:江西省南昌市八一中学2018-2019学年高二上学期12月月考化学试题
名校
解题方法
3 . “分子筛”是一种具有多孔结构的铝硅酸盐(NaAlSiO4·nH2O),其中有许多笼状孔穴和通道,能让直径比孔穴小的分子通过而将大的分子留在外面,故此得名。利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备“分子筛”的一种工艺流程如下:

(1)“分子筛”的化学式用氧化物形式可表示为_______________ 。
(2)铝灰水解产生的气体为________ (填化学式);“水解”在加热条件下而不在室温下进行的原因是________________________ 。
(3)“酸溶”时,发生氧化还原反应的离子方程式为_________________________________ 。
(4)该工艺中滤渣的颜色为________________________ 。
(5)某学习小组设计实验模拟从浓缩海水(含Ca2+、Mg2+、SO42-)中提取试剂级NaCl:
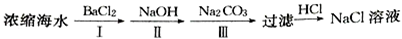
①实验中若向浓缩海水中加入的是Na2CO3浓溶液,则有难溶的Mg2(OH)2CO3生成,同时有气体逸出。该反应的离子方程式为__________________________________ 。
②该学习小组发现上述实验即使BaCl2用量不足,第Ⅲ步沉淀中依然含有少量BaCO3。从平衡角度分析其原因:_____________________________________________ 。

(1)“分子筛”的化学式用氧化物形式可表示为
(2)铝灰水解产生的气体为
(3)“酸溶”时,发生氧化还原反应的离子方程式为
(4)该工艺中滤渣的颜色为
(5)某学习小组设计实验模拟从浓缩海水(含Ca2+、Mg2+、SO42-)中提取试剂级NaCl:
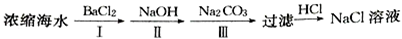
①实验中若向浓缩海水中加入的是Na2CO3浓溶液,则有难溶的Mg2(OH)2CO3生成,同时有气体逸出。该反应的离子方程式为
②该学习小组发现上述实验即使BaCl2用量不足,第Ⅲ步沉淀中依然含有少量BaCO3。从平衡角度分析其原因:
您最近一年使用:0次
名校
解题方法
4 . 三盐基硫酸铅(3PbO·PbSO4·H2O)简称“三盐”,白色或微黄色粉末,热稳定性能优良,主要用作聚氯乙烯的热稳定剂。“三盐”是由可溶性铅盐中加入硫酸生成硫酸铅,再加氢氧化钠而制得。以100.0吨铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示

已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13;铅与冷盐酸、冷硫酸几乎不起作用。
请回答下列问题:
(1)写出步骤①“转化”的化学方程式_________________________________ 。
(2)步骤②“过滤1”后所得滤渣的主要成分为_____________ 。
(3)步骤③“酸溶”,最适合选用的酸为___________ ,为提高酸溶速率,可采取的措施是____________________________________ (任意写出一条)。
(4)若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)=_________ mol·L-1。
(5)从原子利用率的角度分析该流程的优点为___________________ 。
(6)步骤⑥“合成”三盐的化学方程式为____________________ 。

已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13;铅与冷盐酸、冷硫酸几乎不起作用。
请回答下列问题:
(1)写出步骤①“转化”的化学方程式
(2)步骤②“过滤1”后所得滤渣的主要成分为
(3)步骤③“酸溶”,最适合选用的酸为
(4)若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)=
(5)从原子利用率的角度分析该流程的优点为
(6)步骤⑥“合成”三盐的化学方程式为
您最近一年使用:0次
2018-08-29更新
|
975次组卷
|
5卷引用:【全国百强校】江西省上高二中2019届高三上学期第四次月考理科综合化学试题
5 . 工业制备氯化铜时,将浓盐酸加热至80 ℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤。请回答以下问题:
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
(1)将浓盐酸溶解粗CuO粉末后,溶液中的金属阳离子含有___________ ,第一步除去该溶液中的Fe2+,能否直接调整溶液pH=9.6,将Fe2+沉淀除去?_____ ,(填“能” 或“不能”)理由是 _____________________________________________________________
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的pH将Fe3+沉淀除去:你认为用NaClO作氧化剂是否妥当?_____ (填“是” 或“否”),现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有________ (有几个选几个,填代号,下同)。
A.浓HNO3 B.Cl2 C.KMnO4 D.H2O2
(3)①加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的___________ 。
A.CuO B.NH3·H2O C.NaOH D.Cu(OH)2
②加上述物质调节溶液的pH为3.2~4.7,原因是________________________________________________
(4)最后能不能直接将溶液蒸发得到CuCl2·2H2O?______ (填“能”或者“不能”)。若不能,应该如何操作才能得到CuCl2·2H2O____________________________________________ (若填“能”,此空不用回答)
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.6 | 6.7 |
(1)将浓盐酸溶解粗CuO粉末后,溶液中的金属阳离子含有
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的pH将Fe3+沉淀除去:你认为用NaClO作氧化剂是否妥当?
A.浓HNO3 B.Cl2 C.KMnO4 D.H2O2
(3)①加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的
A.CuO B.NH3·H2O C.NaOH D.Cu(OH)2
②加上述物质调节溶液的pH为3.2~4.7,原因是
(4)最后能不能直接将溶液蒸发得到CuCl2·2H2O?
您最近一年使用:0次
名校
解题方法
6 . 金属镁性质活泼,能与许多物质反应。
I.某校课外活动小组根据镁能在二氧化碳中燃烧,推测Mg也能在NO2燃烧,可能产物为MgO、N2和Mg3N2。通过如图所示实验装置来验证反应产物(夹持装置省略,部分仪器可重复使用)。已知:NO2气体能被NaOH吸收,Mg3N2极易与水反应。
(1)实验中,装置依次连按的顺序为A_____ (填字母序号);装置B的作用是______ ;
(2)用来检验N2的实验装置为____ (填字母序号);
(3)设计实验证明:产物中存在Mg3N2、____ ;
Ⅱ.工业上以菱镁矿为原料(主要成分为MgCO3,还有SiO2、FeCO3等杂质)制备纳米氧化镁。
(4)根据反应流程要求,先除去FeCO3,采用先酸浸再氧化的方法,其中加入H2O2时,发生反应的离子方程式为_____ 。
(5)已知:在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,流程后期,当除杂完成后,再加入CO(NH2)2开始沉淀Mg2+,该过程中发生的两个主要反应为(用化学方程式或离子反应方程式表示)_______ ;_______ 。
I.某校课外活动小组根据镁能在二氧化碳中燃烧,推测Mg也能在NO2燃烧,可能产物为MgO、N2和Mg3N2。通过如图所示实验装置来验证反应产物(夹持装置省略,部分仪器可重复使用)。已知:NO2气体能被NaOH吸收,Mg3N2极易与水反应。
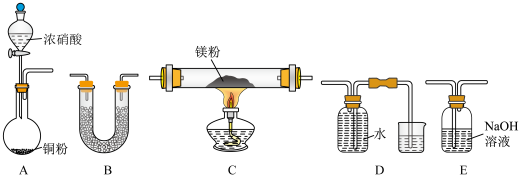
(1)实验中,装置依次连按的顺序为A
(2)用来检验N2的实验装置为
(3)设计实验证明:产物中存在Mg3N2、
Ⅱ.工业上以菱镁矿为原料(主要成分为MgCO3,还有SiO2、FeCO3等杂质)制备纳米氧化镁。
(4)根据反应流程要求,先除去FeCO3,采用先酸浸再氧化的方法,其中加入H2O2时,发生反应的离子方程式为
(5)已知:在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,流程后期,当除杂完成后,再加入CO(NH2)2开始沉淀Mg2+,该过程中发生的两个主要反应为(用化学方程式或离子反应方程式表示)
您最近一年使用:0次
2017-05-05更新
|
306次组卷
|
3卷引用:江西省重点中学盟校2017届高三第二次联考理综化学试题
解题方法
7 . 七水硫酸镁(MgSO4·7H2O)可用于印染加重剂,制造瓷器、颜料和防火材料。在医药上用作泻剂,在微生物工业作培养基成分等。可利用化工厂生产硼砂的废渣——硼镁泥制取七水硫酸镁(MgSO4·7H2O),硼镁泥的主要成分是MgCO3,还含有其它杂质(MgO、Na2B4O7、SiO2、Fe2O3、CaO、Al2O3、MnO等)。
硼镁泥制取七水硫酸镁的工艺流程图如下:

表l:部分阳离子开好成淀和完全沉淀时溶液的pH
据此试回答下列问题:
(1)写出生成H3BO3的离子方程式______________ 。
(2)NaClO具有强氧化性,能直接将溶液中Fe2+和Mn2+分别氧化成______ (填化学式)。
(3)能否直接控制pH除去Mn2+______ ,理由__________ 。
(4)若检验时溶液呈红色,说明滤液B中还含有_______ 未除尽(填离子符号),应补加_______ 再煮沸趁热过滤(填化学式)。
(5)沉淀D的化学式_______________ 。
硼镁泥制取七水硫酸镁的工艺流程图如下:

表l:部分阳离子开好成淀和完全沉淀时溶液的pH
| Fe3+ | Fe2+ | Mn2+ | Mg2+ | Al3+ | |
| 开始沉淀的pH | 1.9 | 7.9 | 8.6 | 9.6 | 3.1 |
| 完全沉淀的pH | 3.2 | 9.0 | 10.l | 11 | 5.4 |
(1)写出生成H3BO3的离子方程式
(2)NaClO具有强氧化性,能直接将溶液中Fe2+和Mn2+分别氧化成
(3)能否直接控制pH除去Mn2+
(4)若检验时溶液呈红色,说明滤液B中还含有
(5)沉淀D的化学式
您最近一年使用:0次
8 . 软锰矿的主要成分为MnO2,含少量Al2O3和SiO2。闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如下(中间产物的固体部分已经略去)。
已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是_________________ (任写一种)。①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式______________________ 。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是_________ 。
(3)步骤③中MnO2的其作用是__________________ ,另外一种物质X可以是__________ 。
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式__________ 。
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为__________________ 。在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L―1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS―浓度为1.0×10―4 mol·L―1时,Mn2+开始沉淀,则a=______ 。[已知:Ksp(MnS)=1.4×10―15]

已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是
(3)步骤③中MnO2的其作用是
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为
您最近一年使用:0次
2017-02-26更新
|
306次组卷
|
2卷引用:2017届江西省新余市第四中学、宜春中学高三下学期开学联考理科综合化学试卷
2013·江苏·一模
解题方法
9 . 利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
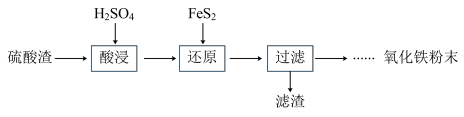
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,②____________ 。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为 ,该反应的离子方程式为
,该反应的离子方程式为_____________________________________________________________ 。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:
准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++
Sn2++4Cl-+2HgCl2= +Hg2Cl2↓
+Hg2Cl2↓
6Fe2++ +14H+=6Fe3++2Cr3++7H2O
+14H+=6Fe3++2Cr3++7H2O
①若SnCl2不足量,则测定的Fe3+量___________ (填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量_______________ 。
(4)①可选用_____________ (填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是__________ (用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:______________________________ ;
b.沉淀:_______________________________ ;
c.分离,洗涤;
d.烘干,研磨。

(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,②
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:
准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++

Sn2++4Cl-+2HgCl2=
 +Hg2Cl2↓
+Hg2Cl2↓6Fe2++
 +14H+=6Fe3++2Cr3++7H2O
+14H+=6Fe3++2Cr3++7H2O①若SnCl2不足量,则测定的Fe3+量
②若不加HgCl2,则测定的Fe3+量
(4)①可选用
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:
b.沉淀:
c.分离,洗涤;
d.烘干,研磨。
您最近一年使用:0次
2016-12-09更新
|
460次组卷
|
7卷引用:2015届江西省景德镇市高三下学期第三次质检考试理综化学试卷
2015届江西省景德镇市高三下学期第三次质检考试理综化学试卷(已下线)2013届江苏省苏锡常镇徐连六市高三3月教学情况调研(一)化学试卷(已下线)2013-2014河南省洛阳市高三下学期统考二练理综化学试卷2015届宁夏回族自治区银川一中高三一模理综化学试卷2017届河南省郑州市二砂寄宿学校高三第一次月考理综化学试卷2017届江苏省无锡市三校联合体高三上第一次月考化学试卷内蒙古赤峰市红山区2021-2022学年高二上学期期末联考化学试题
名校
10 . 炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下:
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。试回答下列问题:
(1)“浸出”时用到的“试剂X”为______________ (填名称)。
(2)写出“氧化”过程的离子方程式_______________________________________ 。
(3)“调pH”过程可以选用_______________ (填序号)。
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是______________________________ (填化学式,下同)。
(4)“试剂Y”是__________________ 。
(5)“操作1”的方法是__________ ;在“操作1”时,必须采取的实验措施是_____________ 。
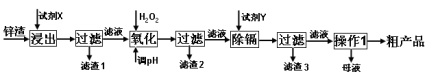
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。试回答下列问题:
(1)“浸出”时用到的“试剂X”为
(2)写出“氧化”过程的离子方程式
(3)“调pH”过程可以选用
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是
(4)“试剂Y”是
(5)“操作1”的方法是
您最近一年使用:0次



