解题方法
1 . a、b、c、d、e、f是原子序数依次增大的非0族元素,位于元素周期表的前四周期。a的一种核素无中子,b的s能级电子数与p能级的电子数之比为4:3,c与e同主族,未成对电子数为2,d在同周期元素中的原子半径最大,f在同周期元素中的未成对电子数最多。请回答下列问题:
(1)上述元素中,位于元素周期表p区的元素有________ (填元素符号),其中基态c原子中电子占据的最高能级的原子轨道形状是________ 。
(2)基态e原子的核外电子排布式为_______ ,其核外有____ 种不同空间运动状态的电子。
(3)b、c、d、e简单离子半径由大到小的顺序为_____ (用离子符号表示)。
(4)基态f原子的未成对电子数与成对电子数之比为______ 。
(1)上述元素中,位于元素周期表p区的元素有
(2)基态e原子的核外电子排布式为
(3)b、c、d、e简单离子半径由大到小的顺序为
(4)基态f原子的未成对电子数与成对电子数之比为
您最近一年使用:0次
名校
解题方法
2 . 铜盐中毒可用青霉胺解毒,解毒原理如下: 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
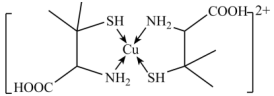
 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
A.比较硫化氢与氨气键角的大小: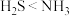 |
| B.第二周期主族元素中,第一电离能大于N的元素有1种 |
| C.该环状络合物易溶于水的主要原因是其与水可形成分子间氢键 |
| D.该环状络合物中,VSEPR模型为四面体或正四面体的非金属原子共有13个 |
您最近一年使用:0次
名校
解题方法
3 . DF-31洲际弹道导弹是我国大国地位和国防实力的象征,其制作材料包含了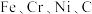 等多种元素。回答下列问题:
等多种元素。回答下列问题:
(1)基态铁原子的电子排布式为_______ , 具有较强的还原性,原因是
具有较强的还原性,原因是_______ 。
(2) 的第二电离能
的第二电离能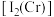 和
和 的第二电离能
的第二电离能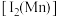 分别为
分别为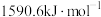 、
、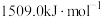 ,
, 的原因是
的原因是_______ ;过氧化铬 中
中 的化合价为
的化合价为 ,则分子中
,则分子中 键、π键的数目之比为
键、π键的数目之比为_______ 。
(3)下图中表示的碳原子能量最高的是_______(填字母)。
(4)超临界流体是物质介于气态和液态之间的新状态,目前应用最广泛的是超临界 。超临界
。超临界 流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。
流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。 中C原子的杂化方式为
中C原子的杂化方式为_______ ,分子中的化学键为_______ (填“极性键”或“非极性键”),分子属于_______ (填“极性”或“非极性”)分子。
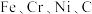 等多种元素。回答下列问题:
等多种元素。回答下列问题:(1)基态铁原子的电子排布式为
 具有较强的还原性,原因是
具有较强的还原性,原因是(2)
 的第二电离能
的第二电离能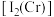 和
和 的第二电离能
的第二电离能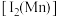 分别为
分别为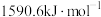 、
、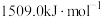 ,
, 的原因是
的原因是 中
中 的化合价为
的化合价为 ,则分子中
,则分子中 键、π键的数目之比为
键、π键的数目之比为(3)下图中表示的碳原子能量最高的是_______(填字母)。
A. | B.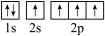 |
C.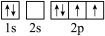 | D.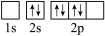 |
 。超临界
。超临界 流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。
流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。 中C原子的杂化方式为
中C原子的杂化方式为
您最近一年使用:0次
名校
解题方法
4 . 氯吡苯脲是一种常用的膨大剂,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。其结构简式如下:
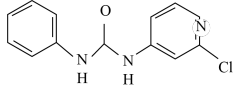
回答下列问题:
(1)基态氯原子价电子排布式为_______ 。
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为_______ ,该物质易溶于水的原因是_______ 。
(3)氯吡苯脲晶体中,微粒间的作用力类型有_______ (填字母)。
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

反应过程中,每生成 氯吡苯脲,形成
氯吡苯脲,形成_______ 个 键、断裂
键、断裂_______ 个π键。
(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有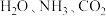 等,请用共价键理论解释
等,请用共价键理论解释 分子比
分子比 分子稳定的原因:
分子稳定的原因:_______ 。

回答下列问题:
(1)基态氯原子价电子排布式为
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为
(3)氯吡苯脲晶体中,微粒间的作用力类型有
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

反应过程中,每生成
 氯吡苯脲,形成
氯吡苯脲,形成 键、断裂
键、断裂(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有
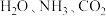 等,请用共价键理论解释
等,请用共价键理论解释 分子比
分子比 分子稳定的原因:
分子稳定的原因:
您最近一年使用:0次
名校
解题方法
5 . 硫及其化合物用途非常广泛。回答下列问题:
(1)基态S原子的电子占据最高能级的电子云轮廓图为_______ 形。
(2)O和S处于同一主族。 及
及 中,中心原子的杂化方式相同,键长及键角如图1所示。
中,中心原子的杂化方式相同,键长及键角如图1所示。
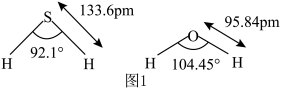
① 分子中的键长比
分子中的键长比 中的键长短,其原因是
中的键长短,其原因是_______ 。
② 分子中的键角
分子中的键角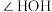 比
比 分子中的键角
分子中的键角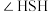 大,其原因是
大,其原因是_______ 。
(3)①单质硫与热的 浓溶液反应的产物之一为
浓溶液反应的产物之一为 。
。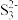 的空间构型为
的空间构型为_______ 。
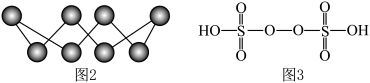
②S单质的常见形式为 ,其环状结构如图2所示,S原子采用的轨道杂化方式是
,其环状结构如图2所示,S原子采用的轨道杂化方式是_______ 。
③钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为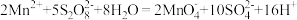 。已知
。已知 的结构如图3所示,上述反应每生成
的结构如图3所示,上述反应每生成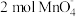 ,
, 层断裂的共价键数目为
层断裂的共价键数目为_______  。
。
(4)噻吩( )广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有
)广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有_______ 个 键。噻吩的沸点为
键。噻吩的沸点为 ,吡咯(
,吡咯(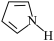 )的沸点在
)的沸点在 之间,后者沸点较高,其原因
之间,后者沸点较高,其原因_______ 。
(1)基态S原子的电子占据最高能级的电子云轮廓图为
(2)O和S处于同一主族。
 及
及 中,中心原子的杂化方式相同,键长及键角如图1所示。
中,中心原子的杂化方式相同,键长及键角如图1所示。
①
 分子中的键长比
分子中的键长比 中的键长短,其原因是
中的键长短,其原因是②
 分子中的键角
分子中的键角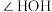 比
比 分子中的键角
分子中的键角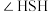 大,其原因是
大,其原因是(3)①单质硫与热的
 浓溶液反应的产物之一为
浓溶液反应的产物之一为 。
。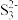 的空间构型为
的空间构型为②S单质的常见形式为
 ,其环状结构如图2所示,S原子采用的轨道杂化方式是
,其环状结构如图2所示,S原子采用的轨道杂化方式是③钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为
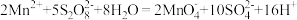 。已知
。已知 的结构如图3所示,上述反应每生成
的结构如图3所示,上述反应每生成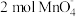 ,
, 层断裂的共价键数目为
层断裂的共价键数目为 。
。
(4)噻吩(
 )广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有
)广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有 键。噻吩的沸点为
键。噻吩的沸点为 ,吡咯(
,吡咯( )的沸点在
)的沸点在 之间,后者沸点较高,其原因
之间,后者沸点较高,其原因
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题:
(1)氟原子激发态的电子排布式有_______ (填标号,后同),其中能量较高的是_______ 。
a. b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为_______ 。
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图_______ (填标号),判断的根据是_______ ;第三电离能的变化图是图_______ (填标号)。

(4)短周期元素X、Y、Z、W的原子序数依次增大。
①元素的电负性:Z_______ (填“大于”“小于”或“等于”)W。
②简单离子半径:W_______ (填“大于”“小于”或“等于”)Y。
③氢化物的稳定性:X_______ (填“大于”“小于”或“等于”)Z。
(1)氟原子激发态的电子排布式有
a.
 b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图

(4)短周期元素X、Y、Z、W的原子序数依次增大。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | 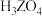 | |||
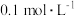 溶液对应的 溶液对应的 | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
名校
解题方法
7 . 下列图示或化学用语表示错误的是
| A | B | C | D |
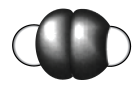 | 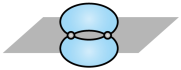 |  | 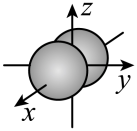 |
| 乙炔的空间填充模型 | 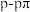 键电子云轮廓图 键电子云轮廓图 |  的结构示意图 的结构示意图 | 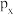 轨道的电子云轮廓图 轨道的电子云轮廓图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 一种可吸附甲醇的材料,其化学式为 ,部分晶体结构如下图所示,其中
,部分晶体结构如下图所示,其中 为平面结构。
为平面结构。
 ,部分晶体结构如下图所示,其中
,部分晶体结构如下图所示,其中 为平面结构。
为平面结构。 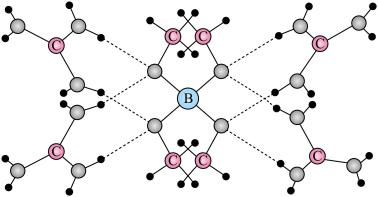
| A.该晶体中存在N-H…O氢键 | B.基态原子的第一电离能: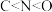 |
C.基态原子未成对电子数: | D.晶体中B、N和O原子轨道的杂化类型相同 |
您最近一年使用:0次
2023-06-10更新
|
14669次组卷
|
24卷引用:云南省宣威市第九中学2023-2024学年高三下学期入学考试理综试题-高中化学
云南省宣威市第九中学2023-2024学年高三下学期入学考试理综试题-高中化学2023年高考新课标理综化学真题(已下线)T9-物质结构(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题06 物质结构与性质(已下线)专题06 物质结构与性质(已下线)专题06 物质结构与性质新疆生产建设兵团第三师图木舒克市第一中学2022-2023学年高二下学期期末考试化学试题黑龙江省哈尔滨师范大学附属中学2022-2023学年高二下学期期末考试化学试题河南省商丘名校联考2022-2023学年高二下学期7月期末考试化学试题(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)(已下线)考点41 原子结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第4讲 空间构型(已下线)考点43 晶体结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)T9-物质结构与性质江苏省南菁高中、常州市第一中学2023-2024学年高二下学期3月月考化学试题湖北省襄阳市第一中学2023-2024学年高二下学期3月月考化学试题山东省枣庄市第八中学三校区2023-2024学年高二下学期联考化学试卷(已下线)FHgkyldyjhx06广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题2024届河南省郑州市第一中学高三下学期考前全真模拟考试理科综合试题-高中化学四川省甘孜藏族自治州某重点中学2023-2024学年高二下学期4月期中考试化学试题四川省达州外国语学校2023-2024学年高二下学期期中考试化学试题
名校
9 . 短周期主族元素X、Y、Z、W的原子序数依次增大,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列说法错误的是
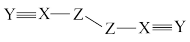
| A.W位于元素周期表的p区 | B.第一电离能:Y>Z>X |
| C.W的原子中有9种运动状态不同的电子 | D.Y、W可形成共价晶体 |
您最近一年使用:0次
2023-06-01更新
|
51次组卷
|
3卷引用:云南省曲靖市会泽县实验高级中学校2022-2023学年高二下学期6月月考化学试题
解题方法
10 . 氮及其化合物在工农业生产和生命活动中起着重要的作用。同时,氮氧化物(NOx)是常见的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。因此,研究氮氧化物(NOx)的无害化处理对治理大气污染、建设生态文明具有重要意义。请按要求回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬在现代工业中发挥着重要的作用。基态铬、氮原子的未成对电子数之比为__________ 。
(2)联氨(又称肼,N2H4,无色液体)也是氮的一种重要的化合物,是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨的第一步电离方程式为___________ 。
(3)研究氮氧化物(NOx)的无害化处理
I.CO还原NO2的反应原理如下:
已知:①NO2(g)+CO(g) CO2(g)+NO(g) ΔH1= -234kJ·mol-1
CO2(g)+NO(g) ΔH1= -234kJ·mol-1
②N2(g)+O2(g) 2NO(g) ΔH2= +179.5 kJ·mol-1
2NO(g) ΔH2= +179.5 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) ΔH3=-112.3 kJ·mol-1
2NO2(g) ΔH3=-112.3 kJ·mol-1
NO2与CO反应生成无污染气体的热化学方程式为__________________________ 。
II.用H2还原NO的反应为2H2(g) + 2NO(g) N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
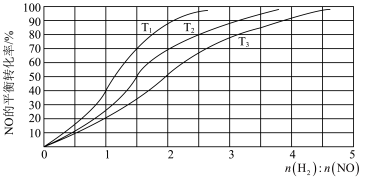
①反应温度T1、T2、T3从高到低的关系为______________________ ;
②T1温度下,充入H2、NO分别为3mol、3mol, 容器内的压强为w Pa,反应进行到10min时达平衡,0~ 10min内N2的平均反应速率为_____________ mol·L-1·s-1,该反应的平衡常数Kp=___________ (写出计算表达式,以分压表示的平衡常数为Kp,某气体分压=总压 ×某气体物质的量分数);
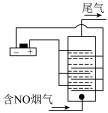
III.以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为___________________________ (用电极反应和离子方程式表示)
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬在现代工业中发挥着重要的作用。基态铬、氮原子的未成对电子数之比为
(2)联氨(又称肼,N2H4,无色液体)也是氮的一种重要的化合物,是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨的第一步电离方程式为
(3)研究氮氧化物(NOx)的无害化处理
I.CO还原NO2的反应原理如下:
已知:①NO2(g)+CO(g)
 CO2(g)+NO(g) ΔH1= -234kJ·mol-1
CO2(g)+NO(g) ΔH1= -234kJ·mol-1②N2(g)+O2(g)
 2NO(g) ΔH2= +179.5 kJ·mol-1
2NO(g) ΔH2= +179.5 kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) ΔH3=-112.3 kJ·mol-1
2NO2(g) ΔH3=-112.3 kJ·mol-1NO2与CO反应生成无污染气体的热化学方程式为
II.用H2还原NO的反应为2H2(g) + 2NO(g)
 N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图: 
①反应温度T1、T2、T3从高到低的关系为
②T1温度下,充入H2、NO分别为3mol、3mol, 容器内的压强为w Pa,反应进行到10min时达平衡,0~ 10min内N2的平均反应速率为
III.以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
您最近一年使用:0次



