解题方法
1 . 一种矿物类饲料添加剂的结构简式如图所示。X、Y、Z、W的原子序数依次增大,Y和W位于第二周期,R 位于元素周期表第四周期ds区,其基态原子无未成对电子。下列说法正确的是


| A.电负性:W>Z>X>Y |
| B.基态R原子的电子在原子核外有30个空间运动状态 |
| C.该配合物中的配体均为中性分子 |
| D.最简单氢化物的键角:Y>Z>W |
您最近一年使用:0次
2 . 锑---钾合金可用作钾离子电池的电极材料,图a为其晶胞结构,图b为晶胞的一部分,下列有关说法正确的是


A.晶胞密度为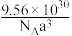 g·cm-3 g·cm-3 |
| B.Sb原子的配位数为6 |
| C.最邻近的Sb原子构成的最小空间结构为正四面体 |
| D.从电子排布推断,K的第一电离能比Sb大 |
您最近一年使用:0次
名校
解题方法
3 . 科学家利用BN和TiO2创造了一种可快速分解世界上最难降解的污染物M的复合光催化剂。M由R、X、Y、Z4种短周期主族元素组成,它们的原子序数依次增大,在暗室中Z的单质能与同温同压下密度最小的气体剧烈反应。M的结构式如图所示。下列叙述错误的是
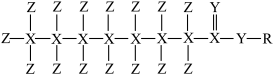
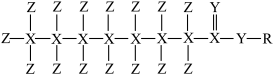
| A.最高正化合价:Z>Y>X>R |
| B.电负性:Z> Y> X |
| C.原子半径:X>Y> Z> R |
| D.M是含极性键和非极性键的共价化合物 |
您最近一年使用:0次
2023-05-23更新
|
223次组卷
|
3卷引用:云南省楚雄彝族自治州2023届高三下学期质量监测理综化学试题
解题方法
4 . X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能与其最高价氧化物对应水化物反应生成盐; Y元素原子的核外电子只有8种运动状态;Z为短周期金属元素,其简单离子的半径在同周期中最小;基态W原子的未成对电子数为6。下列说法错误的是
| A.第一电离能: X>Y> Z |
B.键角 > > |
| C.W为第四周期d区元素 |
| D.X和Y的最简单气态氢化物中,前者更易液化 |
您最近一年使用:0次
5 . 配合物XY(ZW)5的结构如图所示,Y位于第四周期且基态原子中含5个单电子,Z与W位于第二周期的p区,ZW结构与N2相似,Z的电负性小于W。下列说法错误的是
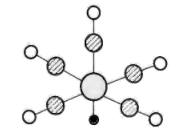

| A.第一电离能: W>Z |
| B.XY(ZW)5中Y的配位数是5 |
| C.W3的熔点低于YW2 |
| D.Z的某种同素异形体具有良好导电性,其中Z原子的杂化方式均为sp2 |
您最近一年使用:0次
解题方法
6 . 氮及其化合物在工农业生产和生命活动中起着重要的作用。同时,氮氧化物(NOx)是常见的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。因此,研究氮氧化物(NOx)的无害化处理对治理大气污染、建设生态文明具有重要意义。请按要求回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬在现代工业中发挥着重要的作用。基态铬、氮原子的未成对电子数之比为__________ 。
(2)联氨(又称肼,N2H4,无色液体)也是氮的一种重要的化合物,是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨的第一步电离方程式为___________ 。
(3)研究氮氧化物(NOx)的无害化处理
I.CO还原NO2的反应原理如下:
已知:①NO2(g)+CO(g) CO2(g)+NO(g) ΔH1= -234kJ·mol-1
CO2(g)+NO(g) ΔH1= -234kJ·mol-1
②N2(g)+O2(g) 2NO(g) ΔH2= +179.5 kJ·mol-1
2NO(g) ΔH2= +179.5 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) ΔH3=-112.3 kJ·mol-1
2NO2(g) ΔH3=-112.3 kJ·mol-1
NO2与CO反应生成无污染气体的热化学方程式为__________________________ 。
II.用H2还原NO的反应为2H2(g) + 2NO(g) N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
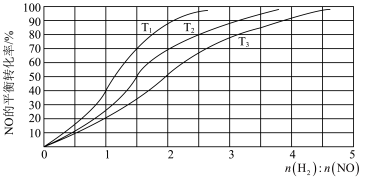
①反应温度T1、T2、T3从高到低的关系为______________________ ;
②T1温度下,充入H2、NO分别为3mol、3mol, 容器内的压强为w Pa,反应进行到10min时达平衡,0~ 10min内N2的平均反应速率为_____________ mol·L-1·s-1,该反应的平衡常数Kp=___________ (写出计算表达式,以分压表示的平衡常数为Kp,某气体分压=总压 ×某气体物质的量分数);
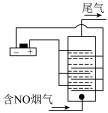
III.以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为___________________________ (用电极反应和离子方程式表示)
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬在现代工业中发挥着重要的作用。基态铬、氮原子的未成对电子数之比为
(2)联氨(又称肼,N2H4,无色液体)也是氮的一种重要的化合物,是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨的第一步电离方程式为
(3)研究氮氧化物(NOx)的无害化处理
I.CO还原NO2的反应原理如下:
已知:①NO2(g)+CO(g)
 CO2(g)+NO(g) ΔH1= -234kJ·mol-1
CO2(g)+NO(g) ΔH1= -234kJ·mol-1②N2(g)+O2(g)
 2NO(g) ΔH2= +179.5 kJ·mol-1
2NO(g) ΔH2= +179.5 kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) ΔH3=-112.3 kJ·mol-1
2NO2(g) ΔH3=-112.3 kJ·mol-1NO2与CO反应生成无污染气体的热化学方程式为
II.用H2还原NO的反应为2H2(g) + 2NO(g)
 N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图: 
①反应温度T1、T2、T3从高到低的关系为
②T1温度下,充入H2、NO分别为3mol、3mol, 容器内的压强为w Pa,反应进行到10min时达平衡,0~ 10min内N2的平均反应速率为
III.以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
您最近一年使用:0次
7 . X、Y、Z、W是同周期主族元素,四种元素均是短周期元素,W元素形成的某种单质具有强氧化性,可用于杀菌消毒。四种元素与锂组成的盐是一种新型锂离子电池的电解质,结构如图所示,下列说法正确的是
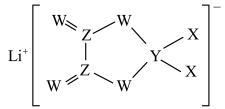

| A.组成这种新型电解质的所有元素均处于元素周期表p区 |
| B.Z元素的含氧酸不可能使酸性高锰酸钾溶液褪色 |
| C.最简单氢化物的沸点: X>W |
| D.同周期中第一电离能比W元素小的有4种元素 |
您最近一年使用:0次
解题方法
8 . 云南省曲靖市物华天宝,资源丰富,煤炭、磷、铅、锌、锑等资源储量位居全省前列,会泽县“斑铜”技艺更是闻名全国。2021年12月,中国有色金属工业协会授予曲靖市“绿色晶硅光伏之都”称号。
(1)晶体硅中Si原子的杂化方式是____ ,基态Zn原子核外电子排布式为____ ,基态Cu原子核外有____ 种能量不同的电子。
(2)磷化亚铜(Cu3P)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化亚铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为____ ;Si、P、S的第一电离能(I1)由大到小的顺序为____ 。
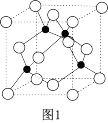
(3)一种铜金合金具有储氢功能。其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为____ 。该储氢材料储氢时,氢分子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与ZnS的结构相似(如图1),该晶体储氢后的化学式为____ 。
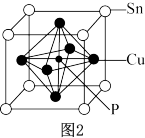
(4)磷青铜晶体的晶胞结构如图2所示,该晶体中P原子位于由铜原子形成的____ 的空隙中。若晶体密度为ag·cm-3,P与最近的Cu原子的核间距为____ nm(用含NA的代数式表示)。
(1)晶体硅中Si原子的杂化方式是
(2)磷化亚铜(Cu3P)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化亚铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为
(3)一种铜金合金具有储氢功能。其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为

(4)磷青铜晶体的晶胞结构如图2所示,该晶体中P原子位于由铜原子形成的

您最近一年使用:0次
解题方法
9 . 胆矾化学式为CuSO4·5H2O。实验证明CuSO4·5H2O中有4个水分子为配位水分子,其结构示意图如下:回答下列问题:
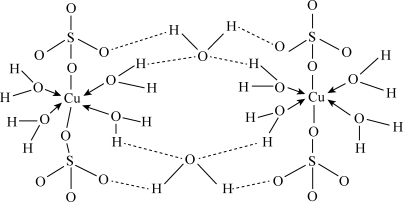
(1)基态铜原子的价层电子排布式为_______ ,位于周期表中第_______ 周期_______ 族。
(2)胆矾中S原子的杂化方式是_______ ,H、O、S中,第一电离能最大的元素是_______ (填元素符号)
(3)胆矾中存在的化学键有配位键、_______ 。
(4)含硫化合物SOCl2的VSEPR模型是_______ ,试分析该分子中键角∠Cl-S-O大于∠Cl-S-Cl的原因是_______ 。
(5)立方铜晶胞中铜原子的配位数为12,则每个晶胞中有_______ 个铜原子,铜原子的半径为rcm,则铜晶体的密度为_______ g·cm-3(阿伏加德罗常数值用NA表示)。

(1)基态铜原子的价层电子排布式为
(2)胆矾中S原子的杂化方式是
(3)胆矾中存在的化学键有配位键、
(4)含硫化合物SOCl2的VSEPR模型是
(5)立方铜晶胞中铜原子的配位数为12,则每个晶胞中有
您最近一年使用:0次
解题方法
10 . 丙二烯磷酸加氢生成顺丙烯磷酸是磷霉素合成的关键步骤,反应原理是:

回答下列问题:
(1)Pd的原子序数是46,基态Pd原子轨道中不存在单电子,基态Pd原子的价电子排布式是_________ .
(2)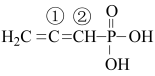 中电负性最大的元素是
中电负性最大的元素是_________ (填元素符号):①号碳原子的杂化方式是_____________ ,②号碳原子的价层电子对数为____________ .
(3)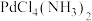 有2种八面体结构:
有2种八面体结构:
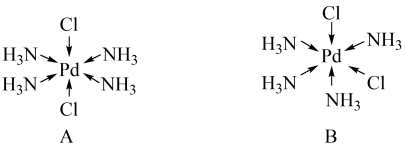
①有极性的结构是________ (填标号).
②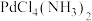 中
中 中
中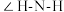 的键角
的键角_________ (填“<”、“>”或“=") 中
中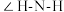 的键角.
的键角.
(4) 能与水混溶,却不溶于
能与水混溶,却不溶于 ,原因是
,原因是______________________ .
(5)Pd的晶胞俯视图如下所示:

已知1个晶胞中含4个Pd原子,其中3个Pd原子的坐标是 ,
, ,
, 则晶胞中每个Pd原子周围距离相等且最近的Pd原子有
则晶胞中每个Pd原子周围距离相等且最近的Pd原子有__________ 个;某铜钯合金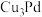 可看作上述Pd晶胞中
可看作上述Pd晶胞中_______ 位置的Pd原子被Cu原子替代.

回答下列问题:
(1)Pd的原子序数是46,基态Pd原子轨道中不存在单电子,基态Pd原子的价电子排布式是
(2)
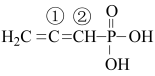 中电负性最大的元素是
中电负性最大的元素是(3)
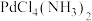 有2种八面体结构:
有2种八面体结构: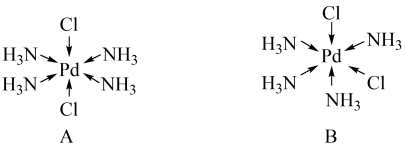
①有极性的结构是
②
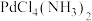 中
中 中
中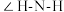 的键角
的键角 中
中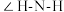 的键角.
的键角.(4)
 能与水混溶,却不溶于
能与水混溶,却不溶于 ,原因是
,原因是(5)Pd的晶胞俯视图如下所示:

已知1个晶胞中含4个Pd原子,其中3个Pd原子的坐标是
 ,
, ,
, 则晶胞中每个Pd原子周围距离相等且最近的Pd原子有
则晶胞中每个Pd原子周围距离相等且最近的Pd原子有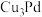 可看作上述Pd晶胞中
可看作上述Pd晶胞中
您最近一年使用:0次



