名校
1 . 氢化镁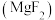 晶体广泛应用在光学、冶金、国防、医疗等领域。
晶体广泛应用在光学、冶金、国防、医疗等领域。
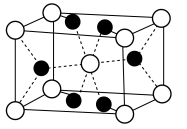
I.氟化镁晶胞是长方体,其结构如图所示:_______ 区(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(2) 晶胞示意图中:离子半径:
晶胞示意图中:离子半径: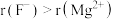 ,结合离子结构示意图解释原因:
,结合离子结构示意图解释原因:_____ 。
II.一种由 制备
制备 的工艺流程如图
的工艺流程如图
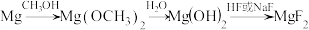
已知:ⅰ. 易溶于甲醇;
易溶于甲醇;
ⅱ.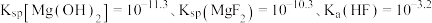
(3)上述流程中,可循环利用的物质是_______ 。
(4)比较相同条件下化学反应速率的大小:① 与
与 ;②
;② 与
与 。
。
 小组同学预测化学反应速率:①
小组同学预测化学反应速率:① ②,理由是甲基为
②,理由是甲基为_______ 基团,导致 键极性:
键极性: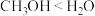 。
。
 实验表明化学反应速率:①
实验表明化学反应速率:① ②,分析其原因可能是
②,分析其原因可能是_______ 。
(5)上述流程中 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: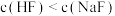 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:_______ 。
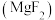 晶体广泛应用在光学、冶金、国防、医疗等领域。
晶体广泛应用在光学、冶金、国防、医疗等领域。I.氟化镁晶胞是长方体,其结构如图所示:
 ”“
”“ ”或“
”或“ ”)。
”)。(2)
 晶胞示意图中:离子半径:
晶胞示意图中:离子半径: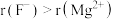 ,结合离子结构示意图解释原因:
,结合离子结构示意图解释原因:II.一种由
 制备
制备 的工艺流程如图
的工艺流程如图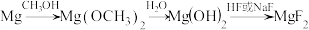
已知:ⅰ.
 易溶于甲醇;
易溶于甲醇;ⅱ.
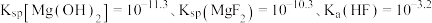
(3)上述流程中,可循环利用的物质是
(4)比较相同条件下化学反应速率的大小:①
 与
与 ;②
;② 与
与 。
。 小组同学预测化学反应速率:①
小组同学预测化学反应速率:① ②,理由是甲基为
②,理由是甲基为 键极性:
键极性: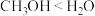 。
。 实验表明化学反应速率:①
实验表明化学反应速率:① ②,分析其原因可能是
②,分析其原因可能是(5)上述流程中
 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: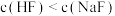 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:
您最近一年使用:0次
名校
2 . 按下列要求填空
(1)基态某原子的最外层电子排布式是 ,推断该元素位于第
,推断该元素位于第_____ 周期第____ 族,在元素周期表中属于____ 区。
(2)基态某原子的价层电子排布式为 ,在元素周期表中属于
,在元素周期表中属于_______ 区。
(3) 杂化类型为
杂化类型为_______ ,VSEPR模型为_______ ,离子空间构型为_______ 。
(1)基态某原子的最外层电子排布式是
 ,推断该元素位于第
,推断该元素位于第(2)基态某原子的价层电子排布式为
 ,在元素周期表中属于
,在元素周期表中属于(3)
 杂化类型为
杂化类型为
您最近一年使用:0次
3 . 回答下列问题
(1)金属钼(Mo)常用于工业、军事等领域,已被多个国家列为战略金属,我国的钼储量居世界第二。已知钼在元素周期表中呈现的信息如下,回答下列问题:
钼在元素周期表中的位置是________ ,基态Mo原子核外有________ 种不同运动状态的电子,其中核外电子占据最高电子层的符号是________ 。
(2)氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知: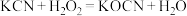 ,回答下列问题:
,回答下列问题:
 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为________ (用元素符号表示,下同),电负性从大到小的顺序为________ ,基态氮原子外围电子排布式为________ 。
(1)金属钼(Mo)常用于工业、军事等领域,已被多个国家列为战略金属,我国的钼储量居世界第二。已知钼在元素周期表中呈现的信息如下,回答下列问题:
钼在元素周期表中的位置是
(2)氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知:
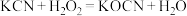 ,回答下列问题:
,回答下列问题: 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为
您最近一年使用:0次
名校
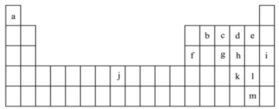
4 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:________ (用元素符号填空,下同)。
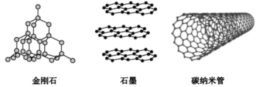
(2)下图为b元素的三种单质,它们互为________ 。________ 。
(4)c的一种氢化物因极易溶于水的性质,可用作喷泉实验,请从物质结构的角度解释溶解度大的原因________ 。
(5)由b、c、h构成的一种阴离子,常用于检验补血剂是否变质,此阴离子的结构可能与________ (请填“ ”、“
”、“ ”或“
”或“ ”)相同。
”)相同。
(6)k常用作光敏材料,基态k原子价层电子占据的最高能级符号为________ ;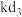 的空间构型为
的空间构型为________ ;熔沸点大小比较: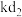
________ 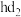 (填“>”、“<”获“=”)。
(填“>”、“<”获“=”)。
(2)下图为b元素的三种单质,它们互为
(4)c的一种氢化物因极易溶于水的性质,可用作喷泉实验,请从物质结构的角度解释溶解度大的原因
(5)由b、c、h构成的一种阴离子,常用于检验补血剂是否变质,此阴离子的结构可能与
 ”、“
”、“ ”或“
”或“ ”)相同。
”)相同。(6)k常用作光敏材料,基态k原子价层电子占据的最高能级符号为
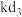 的空间构型为
的空间构型为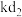
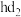 (填“>”、“<”获“=”)。
(填“>”、“<”获“=”)。
您最近一年使用:0次
名校
5 . Ⅰ、已知电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
(1)估计O元素的电负性数值范围________ <X<________
(2)下列物质属于离子化合物的是________ ,属于共价化合物的有________ 。
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
Ⅱ、下表列出了①~⑨九种元素在周期表中的位置:
(3)基态②原子的核外电子有___________ 种空间运动状态。
(4)元素⑦的基态原子价层电子轨道表示式为___________________________ 。
(5)按气态氢化物的稳定性由弱到强的顺序排列,④⑥⑦的简单氢化物稳定性:________ (写氢化物的化学式)。
(6)写出元素⑤形成的单质在氧气中燃烧的化学方程式:___________________ 。
(7)③的简单氢化物与其最高价氧化物的水化物反应的离子方程式:___________________________________ 。
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | X | 2.1 | 2.5 | 1.8 |
(2)下列物质属于离子化合物的是
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
Ⅱ、下表列出了①~⑨九种元素在周期表中的位置:
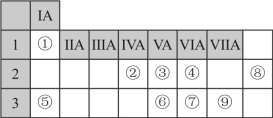
(3)基态②原子的核外电子有
(4)元素⑦的基态原子价层电子轨道表示式为
(5)按气态氢化物的稳定性由弱到强的顺序排列,④⑥⑦的简单氢化物稳定性:
(6)写出元素⑤形成的单质在氧气中燃烧的化学方程式:
(7)③的简单氢化物与其最高价氧化物的水化物反应的离子方程式:
您最近一年使用:0次
6 . Ⅰ.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的________ 区元素,其价电子排布式是________ 。
(2)基态Fe原子核外电子排布式为________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的________ 区(用符号填空),原子序数最大的在周期表位置________ 。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为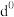 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
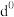 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
您最近一年使用:0次
7 . 写出基态Ti原子的下列表示方法。
(1)电子排布式___________ 。
(2)简化电子排布式___________ 。
(3)价层电子排布式___________ 。
(4)价层电子轨道表示式___________ 。
(5)周期表中的位置(周期、族、区)___________ 。
(1)电子排布式
(2)简化电子排布式
(3)价层电子排布式
(4)价层电子轨道表示式
(5)周期表中的位置(周期、族、区)
您最近一年使用:0次
解题方法
8 . 下表为长式元素周期表的主要部分。①~⑬代表13种元素,⑭表示元素周期表中某一区域。
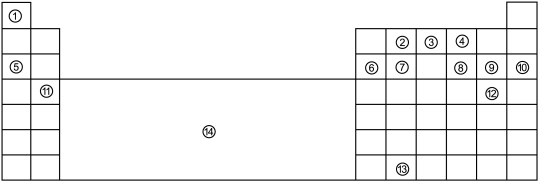
请回答:
(1)①、②、④的原子半径从大到小排列的顺序是______ 。(填化学式)
(2)①与③组成的含10个电子的阳离子的化学式是______ 。
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做______ 元素。
(4)⑩的元素符号是______ 。
(5)⑪的元素名称是______ 。
(6)⑫的原子结构示意图是______ 。
(7)⑬在元素周期表中的位置是______ 。
(8)下列说法不正确 的是______ 。
A. ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数
B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与 溶液反应的化学方程式是
溶液反应的化学方程式是______ 。

请回答:
(1)①、②、④的原子半径从大到小排列的顺序是
(2)①与③组成的含10个电子的阳离子的化学式是
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做
(4)⑩的元素符号是
(5)⑪的元素名称是
(6)⑫的原子结构示意图是
(7)⑬在元素周期表中的位置是
(8)下列说法
A.
 ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与
 溶液反应的化学方程式是
溶液反应的化学方程式是
您最近一年使用:0次
9 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
(3)Ti原子最高能层电子的电子云轮廓形状为___________ ,Ti原子位于元素周期表中的___________ 区,与Ti同周期的过渡元素中,未成对电子数最多的的基态原子的外围电子的轨道表示式___________ 。
(4)N元素基态原子核外电子有___________ 种不同的空间运动状态,能量最高的电子所在原子轨道在空间有___________ 个伸展方向。
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
 b.
b. c.
c. d.
d.
(3)Ti原子最高能层电子的电子云轮廓形状为
(4)N元素基态原子核外电子有
您最近一年使用:0次
23-24高二下·全国·课后作业
10 . 1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:
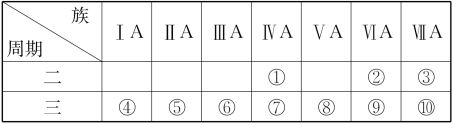
(1)元素③的名称是___________ ,金属性最强的元素是___________ (填元素符号)。
(2)①②⑤三种元素原子半径由大到小的顺序为___________ (填序号)。
(3)元素⑦的单质的一种用途是___________ (填写“制造玻璃”或“制造计算机芯片”)。
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是___________ (填化学式)。

(1)元素③的名称是
(2)①②⑤三种元素原子半径由大到小的顺序为
(3)元素⑦的单质的一种用途是
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是
您最近一年使用:0次



