名校
解题方法
1 . 据媒体报道,法国一家公司Tiamat日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从2020年开始实现工业生产。该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。回答下列问题:
(1)Co 属于元素周期表中___________ 区元素,其基态原子的价电子排布式为___________ 。
(2)基态Na原子中,核外电子占据的原子轨道总数为___________ ,最高能层电子云轮廓图形状为___________
(3)结合题中信息判断:C、O、Cl的电负性由小到大的顺序为___________ (用元素符号表示)。
(4) 的几何构型为
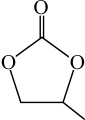
的几何构型为___________ ;碳酸丙烯酯的结构简式如图所示,则其中碳原子的杂化轨道类型为___________ ,1mol碳酸丙烯酯中 键的数目为
键的数目为___________ 。
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是___________ ,该配离子包含的作用力为___________ (填选项字母)。
A.离子键 B.金属键 C.配位键 D.氢键 E.极性键
(1)Co 属于元素周期表中
(2)基态Na原子中,核外电子占据的原子轨道总数为
(3)结合题中信息判断:C、O、Cl的电负性由小到大的顺序为
(4)
 的几何构型为
的几何构型为 键的数目为
键的数目为
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是
A.离子键 B.金属键 C.配位键 D.氢键 E.极性键
您最近一年使用:0次
名校
解题方法
2 . 已知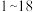 号元素的离子
号元素的离子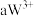 、
、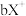 、
、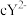 、
、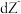 都具有相同电子层结构,下列关系正确的是
都具有相同电子层结构,下列关系正确的是
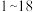 号元素的离子
号元素的离子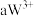 、
、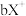 、
、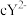 、
、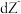 都具有相同电子层结构,下列关系正确的是
都具有相同电子层结构,下列关系正确的是A.质子数: ,离子的还原性: ,离子的还原性: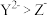 |
B.电负性: |
C.氢化物的稳定性: |
D.原子半径: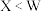 ,第一电离能: ,第一电离能: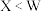 |
您最近一年使用:0次
2022-12-02更新
|
1101次组卷
|
34卷引用:福建省厦门市思明区厦门外国语学校2019-2020学年高二上学期周末练习10——化学试题
福建省厦门市思明区厦门外国语学校2019-2020学年高二上学期周末练习10——化学试题2015-2016学年贵州省思南中学高二下第一次月考化学试卷2015-2016学年山西大学附属中学高二下3月月考化学试卷2015-2016学年吉林省汪清六中高二3月月考化学试卷2015-2016学年山西大学附中高二下3月月考化学试卷2016-2017学年河北省衡水中学高二上学期五调考试化学试卷2016-2017学年河南省洛阳市第一高级中学高二(平行班)3月月考化学试卷2016-2017学年山西省大同市第一中学高二3月月考化学试卷福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题贵州省思南中学2016-2017学年高二下学期期中考试化学试题人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质1河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题【全国百强校】甘肃省嘉峪关市酒钢三中2017-2018学年高二下学期期中考试化学试题【全国百强校】宁夏吴忠中学2017-2018学年高二6月月考化学试题2020届高三化学二轮物质结构题型专攻——元素性质的递变规律【选择提升专练】河南省林州市林虑中学2019-2020学年高二3月线上考试化学试题河北省石家庄市启明中学2019-2020学年高二四月月考化学试题吉林省白山市第七中学2019-2020学年高二下学期3月份月考化学试题鲁科版(新)必修第二册第一章检测题辽宁省六校协作体2019-2020学年高二下学期期中考试化学试卷(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质(人教版2019)选择性必修2第一章 原子结构与性质 第二节 原子结构与元素的性质 第3课时 元素的电负性及其变化规律鲁科版2019选择性必修2第1章 原子结构与元素性质 第3节 元素性质及其变化规律 第2课时 元素的电负性及其变化规律(已下线)模块同步卷03 第一章综合检测-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)专题强化练2 电离能和电负性的应用吉林省辉南县第六中学2022-2023学年高二上学期期中考试化学试题湖南省长沙市周南中学2022-2023学年高二上学期期末考试化学试题安徽省池州市第一中学2022-2023学年高二下学期第一次月考化学试题北京市第三十五中学2021-2022学年高三上学期期中考试化学试题四川省内江市资中县第二中学2023-2024学年高二下学期3月月考化学试题黑龙江省黑河市第一中学2023-2024学年高二下学期4月月考化学试题内蒙古自治区赤峰第四中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
3 . 某种锂盐的结构如图所示,其阴离子由W、X、Y、Z四种同周期主族元素构成,X原子的最外层电子数是W原子的次外层电子数的3倍,化合物中除Li+外其它原子均满足8电子稳定结构。下列说法正确的是
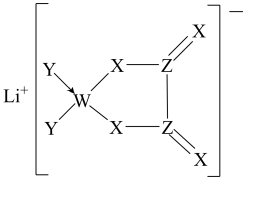

| A.W位于第2周期IVA族 | B.原子半径:Z>X>Y |
| C.元素电负性:Y>Z>X | D.最高化合价:Y>Z>W |
您最近一年使用:0次
2022-05-07更新
|
441次组卷
|
6卷引用:福建省厦门市湖滨中学2023-2024学年高三上学期期中考试化学试题
解题方法
4 . 前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上未成对的电子数最多;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)E元素在周期表中位置为_______ ,E3+价电子轨道表示式为_______ 。
(2)B、C、F三种元素电负性由大到小的顺序为_______ (用元素符号表示),第一电离能D_______ (填“>”、“<”或“=”)Al,其原因是_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)F元素可能的性质_______ (填标号)。
 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。(1)E元素在周期表中位置为
(2)B、C、F三种元素电负性由大到小的顺序为
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)F元素可能的性质
| A.其单质可作半导体材料 |
| B.存在-3、+3、+5等多种化合价 |
| C.最高价氧化物对应的水化物是强酸 |
| D.单质还原性弱于磷单质 |
您最近一年使用:0次
2022-04-16更新
|
305次组卷
|
3卷引用:福建省厦门英才学校中学部2021-2022学年高二下学期半期考化学试题
名校
解题方法
5 . 我国科学家团队采用自激发缺陷诱导的方法获得白光,合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料Ba2[Sn(OH)6][B(OH)4]2。
(1)基态50Sn原子的价电子排布式为______ 。Ba、Sn、O三种元素的电负性由大到小的顺序为______ 。
(2)Na2[B4O5(OH)4]·8H2O(硼砂)的阴离子的结构式如图所示。则硼原子的杂化方式为______ ;硼砂中存在的作用力有______ (填标号)。
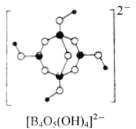
a.氢键 b.离子键 c.共价键 d.配位键
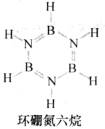
(3)环硼氮六烷(结构如图)在热水中比冷水中溶解度显著增大的主要原因是______ 。
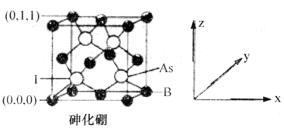
(4)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如图所示,则1号砷原子的坐标为______ 。已知阿伏加德罗常数的值为NA,若晶胞中As原子到B原子最近距离为a pm,则该晶体的密度为______ g·cm-3。(列出含a、NA的计算式即可)。
(1)基态50Sn原子的价电子排布式为
(2)Na2[B4O5(OH)4]·8H2O(硼砂)的阴离子的结构式如图所示。则硼原子的杂化方式为

a.氢键 b.离子键 c.共价键 d.配位键
(3)环硼氮六烷(结构如图)在热水中比冷水中溶解度显著增大的主要原因是

(4)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如图所示,则1号砷原子的坐标为

您最近一年使用:0次
2021-02-04更新
|
280次组卷
|
2卷引用:福建省厦门双十中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
6 . 常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Ga 基态原子核外电子排布式为_______ ,As 基态原子核外有_______ 个未成对电子。
(2)Ga、As、Se 的电负性由大到小的顺序是__________ 。
(3)GaCl3和AsF3的立体构型分别是____________ ,__________ 。
(4)比较下列镓的卤化物的熔点和沸点,分析其变化的原因:____________ 。
GaF3的熔点超过1000 ℃,可能的原因是_____ 。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。[B(OH)4]-中B原子的杂化类型为______ 。
(6)若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅,若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是__________ (用化学式表示);
(1)Ga 基态原子核外电子排布式为
(2)Ga、As、Se 的电负性由大到小的顺序是
(3)GaCl3和AsF3的立体构型分别是
(4)比较下列镓的卤化物的熔点和沸点,分析其变化的原因:
| 镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
| 熔点/℃ | 77.75 | 122.3 | 211.5 |
| 沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000 ℃,可能的原因是
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。[B(OH)4]-中B原子的杂化类型为
(6)若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅,若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是
您最近一年使用:0次
名校
7 . 下列说法正确的是( )
| A.Na、Mg、Al的第一电离能逐渐增大 |
| B.V、Cr、Mn的最外层电子数逐渐增大 |
| C.S2﹣、Cl﹣、K+的半径逐渐减小 |
| D.O、F、Ne的电负性逐渐增大 |
您最近一年使用:0次
2016-06-01更新
|
247次组卷
|
10卷引用:2015-2016学年福建省厦门市高二上学期期末质检化学试卷
2015-2016学年福建省厦门市高二上学期期末质检化学试卷【全国百强校】福建省厦门市外国语学校2018-2019学年高二(理)上学期期中考试化学试题福建省厦门外国语学校2018-2019学年高二下学期期中考试化学试题2015-2016学年吉林省扶余一中高二下学期期中考试化学试卷2017届河南信阳高考化学暑假自学自测专练:原子结构与性质广东省实验中学2016-2017学年高二下学期期中考试化学试题四川省邻水实验学校2019-2020学年高二下学期阶段检测化学试卷云南省玉溪市新平彝族傣自治县第一中学2020-2021学年高三上学期开学考试化学试题湖北省南漳县第二中学2021-2022学年高二下学期3月月考化学试题安徽省 淮北师范大学附属实验中学2022-2023学年高二下学期第一次月考化学试题



