名校
解题方法
1 . 过渡元素在现代工农业生产和科技发展方面具有重要的用途。回答下列问题:
(1)已知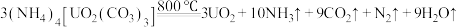 。
。
①基态U原子的外围电子排布式为 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________ (填标号)。
A. B.
B. 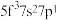 C.
C. 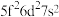 D.
D. 
②反应中断裂的化学键有___________ (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是___________ (填化学式,下同);氢化物中更易与 形成配离子的是
形成配离子的是___________ 。向 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式___________ 。
(2)一个配体中有两个配位原子的配体叫双齿配体,C2O 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为___________
(3)四羰基镍 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是___________ 。
(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为___________ (保留三位小数)。

(1)已知
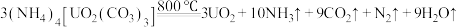 。
。①基态U原子的外围电子排布式为
 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是A.
 B.
B. 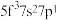 C.
C. 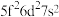 D.
D. 
②反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式(2)一个配体中有两个配位原子的配体叫双齿配体,C2O
 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为(3)四羰基镍
 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为

您最近半年使用:0次
2024-04-03更新
|
255次组卷
|
2卷引用:山东省济宁市第一中学2023-2024学年高三下学期3月月考化学试题
名校
解题方法
2 . 物质的光学性质在科研中有重要的用途。回答下列问题:
Ⅰ.一种比率光声探针M与Cu2+配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:___________ ,M中键角F-B-F___________  中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为___________ 。
(2)均为平面结构的吡咯(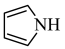 )和吡啶(
)和吡啶(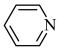 )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为___________ ,原因是___________ 。
Ⅱ.铪(Hf)的卤化物八面体离子是构建卤化物钙钛矿的基本发光单元,其构建的某晶胞结构如图所示。 的配位数为
的配位数为___________ ,阴离子形成的八面体空隙有___________ 个。
(4)该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Hf-Hf最近距离为
,则Hf-Hf最近距离为___________ nm。
Ⅰ.一种比率光声探针M与Cu2+配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
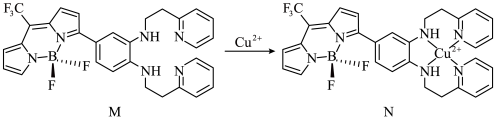
 中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为(2)均为平面结构的吡咯(
 )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为Ⅱ.铪(Hf)的卤化物八面体离子是构建卤化物钙钛矿的基本发光单元,其构建的某晶胞结构如图所示。
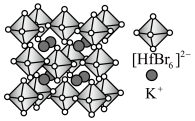
 的配位数为
的配位数为(4)该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Hf-Hf最近距离为
,则Hf-Hf最近距离为
您最近半年使用:0次
2024-03-14更新
|
1049次组卷
|
4卷引用:山东省烟台市2024届高三一模化学试题
山东省烟台市2024届高三一模化学试题2024届山东省高三下学期第一次练兵考试一模化学试题山东省德州市2023-2024学年高三下学期一模考试化学试题(已下线)化学(山东卷03)-2024年高考押题预测卷
3 . 原子是肉眼和一般仪器都看不到的微粒,科学家们是根据可观察、可测量的宏观实验事实,经过分析和推理,揭示了原子结构的奥秘。
(1)下列说法中正确的个数是__________。
①同一原子中,s电子的能量总是低于p电子的能量
②任何s轨道形状均是球形,只是能层不同,球的半径大小不同而己
③2p、3p、4p能级的轨道数依次增多
④原子核外电子排布,先排满K层再排L层,排满M层再排N层
⑤基态碳原子的轨道表示式: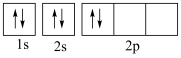
⑥ⅢB族到ⅡB族的10个纵列的元素都是金属元素
⑦用电子式表示 的形成过程:
的形成过程: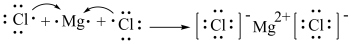
⑧基态钒原子的结构示意图为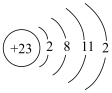
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为__________ 、__________ 。
A.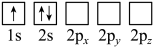 B.
B.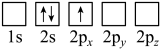
C.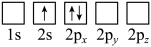 D.
D.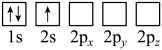
(3)研究发现,正离子的颜色与未成对电子数有关,例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是__________ (从微粒结构的角度进行描述)。
(4)钠在火焰上灼烧产生的黄光是一种原子__________ 光谱(选填“发射”或“吸收”)。
(5)第四周期的元素形成的化合物在生产生活中有着重要的用途。
①镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为__________ ,按照电子排布式,镍元素在周期表中位于__________ 区。
②“玉兔二号”月球车通过砷化镓 太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为
太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为__________ 形。砷的电负性比镓__________ (填“大”或“小”)。
(6)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。表中列出了第三周期的几种元素的部分性质:
①预测x值的区间:______ ~______ 。
②表中五种元素的第一电离能由大到小的顺序是__________ (写元素符号)。
(1)下列说法中正确的个数是__________。
①同一原子中,s电子的能量总是低于p电子的能量
②任何s轨道形状均是球形,只是能层不同,球的半径大小不同而己
③2p、3p、4p能级的轨道数依次增多
④原子核外电子排布,先排满K层再排L层,排满M层再排N层
⑤基态碳原子的轨道表示式:

⑥ⅢB族到ⅡB族的10个纵列的元素都是金属元素
⑦用电子式表示
 的形成过程:
的形成过程:
⑧基态钒原子的结构示意图为

| A.2 | B.3 | C.4 | D.5 |
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(3)研究发现,正离子的颜色与未成对电子数有关,例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是(4)钠在火焰上灼烧产生的黄光是一种原子
(5)第四周期的元素形成的化合物在生产生活中有着重要的用途。
①镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为
②“玉兔二号”月球车通过砷化镓
 太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为
太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为(6)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。表中列出了第三周期的几种元素的部分性质:
元素编号 | a | b | c | d | e |
电负性 | 3.0 | 2.5 | x | 1.5 | 0.9 |
主要化合价 |
|
|
|
|
|
②表中五种元素的第一电离能由大到小的顺序是
您最近半年使用:0次
2024-03-08更新
|
271次组卷
|
2卷引用:山东省青岛市莱西市2023-2024学年高二上学期1月期末考试化学试题
解题方法
4 . 第四周期中的18种元素具有重要的用途。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为_______ 。
(2)第四周期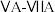 族的元素中,电负性由大到小的顺序为(用元素符号表示)
族的元素中,电负性由大到小的顺序为(用元素符号表示)_______ 。
(3)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则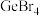 晶体类型为
晶体类型为_______ ,中心原子的杂化类型为_______ 。
(4) 的结构如图所示。
的结构如图所示。
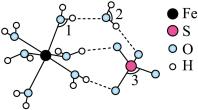
 中
中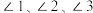 由大到小的顺序是
由大到小的顺序是_______ 。(用“1”“2”“3”表示)
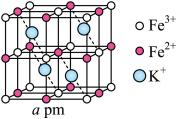
(5)普鲁士蓝晶体属立方晶系,晶胞棱长为 。铁氰骨架组成晶胞中的8个小立方体,
。铁氰骨架组成晶胞中的8个小立方体, 粒子在小立方体顶点,
粒子在小立方体顶点, 在小立方体的棱上,两端均与
在小立方体的棱上,两端均与 相连,小立方体中心空隙可容纳
相连,小立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)
在图中省略)
①普鲁士蓝中 与
与 个数之比为
个数之比为_______ ;
②若所有铁粒子为等径小球,则 与
与 之间最近距离为
之间最近距离为_______  。
。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为
(2)第四周期
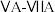 族的元素中,电负性由大到小的顺序为(用元素符号表示)
族的元素中,电负性由大到小的顺序为(用元素符号表示)(3)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则
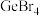 晶体类型为
晶体类型为(4)
 的结构如图所示。
的结构如图所示。
 中
中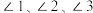 由大到小的顺序是
由大到小的顺序是(5)普鲁士蓝晶体属立方晶系,晶胞棱长为
 。铁氰骨架组成晶胞中的8个小立方体,
。铁氰骨架组成晶胞中的8个小立方体, 粒子在小立方体顶点,
粒子在小立方体顶点, 在小立方体的棱上,两端均与
在小立方体的棱上,两端均与 相连,小立方体中心空隙可容纳
相连,小立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)
在图中省略)
①普鲁士蓝中
 与
与 个数之比为
个数之比为②若所有铁粒子为等径小球,则
 与
与 之间最近距离为
之间最近距离为 。
。
您最近半年使用:0次
解题方法
5 . Fe为重要的元素,与C、N、O等组成的化合物有广泛的用途。回答下列问题:
(1)甘氨酸亚铁络合物[ ]是一种新型的铁营养强化剂。
]是一种新型的铁营养强化剂。
① 中含有的第二周期元素的第一电离能由大到小的顺序为
中含有的第二周期元素的第一电离能由大到小的顺序为___________ 。
②甘氨酸( )的沸点比相近相对分子质量的烷烃高很多,原因是
)的沸点比相近相对分子质量的烷烃高很多,原因是___________ 。
II.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池等,回答下列问题:
(2)基态Ga原子的核外电子排布式为[Ar]___________ 。
(3)根据元素周期律,元素的电负性Ga___________ (填“大于”或“小于”)As。
(4)杀虫剂Na3AsO4中As原子采取___________ 杂化。
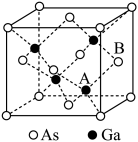
(5)共价晶体GaAs的晶胞参数a=xpm,它的晶胞结构如图所示,该晶体的密度为___________ (列出计算式,阿伏加德罗常数的值用NA表示) 。
。
(1)甘氨酸亚铁络合物[
 ]是一种新型的铁营养强化剂。
]是一种新型的铁营养强化剂。①
 中含有的第二周期元素的第一电离能由大到小的顺序为
中含有的第二周期元素的第一电离能由大到小的顺序为②甘氨酸(
 )的沸点比相近相对分子质量的烷烃高很多,原因是
)的沸点比相近相对分子质量的烷烃高很多,原因是II.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池等,回答下列问题:
(2)基态Ga原子的核外电子排布式为[Ar]
(3)根据元素周期律,元素的电负性Ga
(4)杀虫剂Na3AsO4中As原子采取
(5)共价晶体GaAs的晶胞参数a=xpm,它的晶胞结构如图所示,该晶体的密度为
 。
。
您最近半年使用:0次
名校
解题方法
6 . 卤族元素及其化合物种类繁多,有着非常重要的用途,回答下列问题:
(1)基态Br原子的电子排布式为[Ar]____ 。
(2)HF分子的极性____ (填“大于”“等于”或“小于”,以下同)HCl,同一条件下,HF在水中的溶解度____ HCl,HF的沸点____ HCl。SOCl2中心S原子VSEPR模型为____ 。1mol氟硼酸铵NH4BF4中含有____ mol配位键。
(3)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为apm、apm和2apm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影,标记为n的原子分数坐标为( ,
, ,
, ),则m的原子分数坐标为
),则m的原子分数坐标为____ ,距离Hg最近的Ag有____ 个。设NA为阿伏加德罗常数的值,Ag2HgI4的摩尔质量为Mg•mol-1,该晶体的密度为____ g•cm-3(用代数式表示)。

(1)基态Br原子的电子排布式为[Ar]
(2)HF分子的极性
(3)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为apm、apm和2apm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影,标记为n的原子分数坐标为(
 ,
, ,
, ),则m的原子分数坐标为
),则m的原子分数坐标为
您最近半年使用:0次
2022-03-22更新
|
1239次组卷
|
3卷引用:山东省济南市2022届高三3月高考模拟考试(一模)化学试题
解题方法
7 . ⅤA族元素及其化合物在材料等方面有重要用途。根据所学知识回答下列问题:
(1)基态砷原子处于最高能级的电子云轮廓图为_______ 形。
(2) 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是_______ 。
(3)叠氮化钠( )用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(
)用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸( ),叠氮酸中3个氮原子的杂化类型分别为
),叠氮酸中3个氮原子的杂化类型分别为_______ (不分先后)。
(4)N原子之间可以形成π键,而 原子之间较难形成π键。从原子结构角度分析,其原因为
原子之间较难形成π键。从原子结构角度分析,其原因为_______ 。
(5)往硫酸铜溶液中加入过量氨水,可生成配离子 。已知
。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是_______ 。
(6)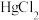 和不同浓度
和不同浓度 反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个
反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个 原子均处于小立方体的面心)
原子均处于小立方体的面心)
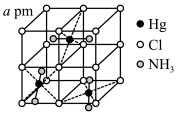
写出该含汞化合物的化学式:_______ 。则该晶体的密度
_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
(1)基态砷原子处于最高能级的电子云轮廓图为
(2)
 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是(3)叠氮化钠(
 )用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(
)用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸( ),叠氮酸中3个氮原子的杂化类型分别为
),叠氮酸中3个氮原子的杂化类型分别为(4)N原子之间可以形成π键,而
 原子之间较难形成π键。从原子结构角度分析,其原因为
原子之间较难形成π键。从原子结构角度分析,其原因为(5)往硫酸铜溶液中加入过量氨水,可生成配离子
 。已知
。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是(6)
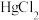 和不同浓度
和不同浓度 反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个
反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个 原子均处于小立方体的面心)
原子均处于小立方体的面心)
写出该含汞化合物的化学式:

 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
2021·全国·模拟预测
名校
解题方法
8 . 氮(N)、磷(P)、砷(As)等第VA族元素的单质和化合物在科研与生产中有许多重要用途。回答下列问题:
(1)基态砷原子的价电子排布图为_______ ,电负性:As_______ S(填“>”“=”或“<”)。
(2)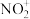 中N原子的杂化方式是
中N原子的杂化方式是_______ 杂化。
(3)LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图所示(图中阴离子未画出)。

①从化学键角度看,Li+迁移过程发生_______ (填“物理”或“化学”)变化。
②相同条件,电池材料_______ (填“LiPF6”或“LiAsF6”)中的Li+迁移较快,原因是_______ 。
(4)通常认为Cu3N是离子晶体,其晶格能可通过Born−Haber循环计算得到。
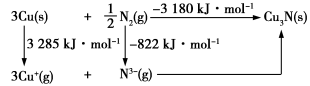
通过图中数据_______ (填“能”或“不能”)计算出Cu原子的第一电离能,Cu3N晶格能为_______ kJ·mol−1。
(5)PCl5能形成离子型晶体,该晶体的晶胞如图所示:
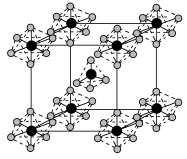
其阴离子中P的配位数为_______ ;若立方体的晶胞边长为apm,NA为阿伏加德罗常数的值,则该晶体的密度为_______ g·cm−3。
(1)基态砷原子的价电子排布图为
(2)
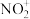 中N原子的杂化方式是
中N原子的杂化方式是(3)LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图所示(图中阴离子未画出)。

①从化学键角度看,Li+迁移过程发生
②相同条件,电池材料
(4)通常认为Cu3N是离子晶体,其晶格能可通过Born−Haber循环计算得到。
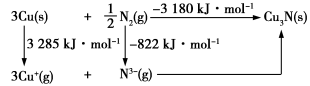
通过图中数据
(5)PCl5能形成离子型晶体,该晶体的晶胞如图所示:

其阴离子中P的配位数为
您最近半年使用:0次
解题方法
9 . 铁及其化合物在国民生产、生活中用途广泛。
(1)向FeCl3溶液加入少量的KSCN溶液,生成红色的[Fe(SCN)(H2O)5]2+。N、C、H元素的第一电离能由大到小的顺序为___________ ,O、N、C、H四种元素电负性最大的是___________ (填元素符号) 。
(2)FeCl3 与K4[Fe(CN)6]溶液混合生成Fe4[Fe(CN)6]3沉淀。配体CN-中C原子的杂化方式为___________ ,CH2=CHCH2CN分子中σ键与π键的数目比n(σ)∶n(π)=___________ 。
(3)用邻二氮菲(phen,如图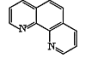 )与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
①[Fe(phen)3]2+中,存在的化学键有___________ (填序号)。
a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定Fe2+浓度时应控制pH为2~9的适宜范围,请解释原因___________ 。
(4)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。
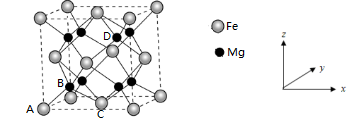
晶体中每个铁原子周围距离最近的镁原子有___________ 个,原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),B为( ),C为(
),C为(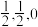 ),则D点坐标参数为
),则D点坐标参数为___________ 。
(1)向FeCl3溶液加入少量的KSCN溶液,生成红色的[Fe(SCN)(H2O)5]2+。N、C、H元素的第一电离能由大到小的顺序为
(2)FeCl3 与K4[Fe(CN)6]溶液混合生成Fe4[Fe(CN)6]3沉淀。配体CN-中C原子的杂化方式为
(3)用邻二氮菲(phen,如图
 )与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。①[Fe(phen)3]2+中,存在的化学键有
a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定Fe2+浓度时应控制pH为2~9的适宜范围,请解释原因
(4)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。

晶体中每个铁原子周围距离最近的镁原子有
 ),C为(
),C为(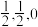 ),则D点坐标参数为
),则D点坐标参数为
您最近半年使用:0次
2021-01-29更新
|
298次组卷
|
2卷引用:山东省烟台市2020-2021学年高二上学期期末考试化学试题
解题方法
10 . 铂(Pt)及其化合物用途广泛。
(1)在元素周期表中,铂元素与铁元素同族,则铂元素位于______ 。
A.s区 B.p区 C.d区 D.ds区 E.f区
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,反式分子和顺式分子一样具有抗癌活性。
①Cl-的最外层电子排布式为______ 。
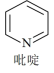
②吡啶分子是大体积平面配体,其结构简式如图所示,该配体的配位原子是___ 。吡啶分子中,碳、氮原子的轨道杂化方式分别是____ 、_____ ,各元素的电负性由大到小的顺序为____ 。
③二氯二吡啶合铂分子中存在的微粒间作用力有___  填序号
填序号 。
。
a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键
④反式二氯二吡啶合铂分子结构如图所示,该分子是___ 分子 选填“极性”、“非极性”
选填“极性”、“非极性” 。
。

(3)已知金属铂的密度为d g/cm3,NA代表阿伏加德罗常数的值,金属铂的相对原子质量为 M。如图分别表示金属铂原子的堆积方式、晶胞特征,则金属铂的堆积方式为____ , 晶胞参数a =_____ nm (列出计算式即可)。

(1)在元素周期表中,铂元素与铁元素同族,则铂元素位于
A.s区 B.p区 C.d区 D.ds区 E.f区
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,反式分子和顺式分子一样具有抗癌活性。
①Cl-的最外层电子排布式为
②吡啶分子是大体积平面配体,其结构简式如图所示,该配体的配位原子是

③二氯二吡啶合铂分子中存在的微粒间作用力有
 填序号
填序号 。
。a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键
④反式二氯二吡啶合铂分子结构如图所示,该分子是
 选填“极性”、“非极性”
选填“极性”、“非极性” 。
。
(3)已知金属铂的密度为d g/cm3,NA代表阿伏加德罗常数的值,金属铂的相对原子质量为 M。如图分别表示金属铂原子的堆积方式、晶胞特征,则金属铂的堆积方式为

您最近半年使用:0次
2020-11-15更新
|
327次组卷
|
2卷引用:山东省济南市平阴县第一中学2021届高三下学期3月月考化学试题

 ,
,
 ,
,
 ,
,




