真题
解题方法
1 . 三氯甲硅烷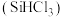 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,熔点为 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
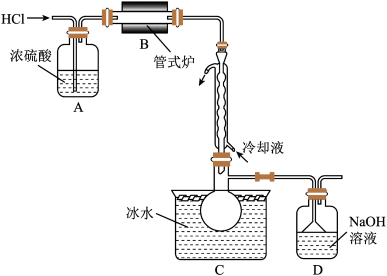
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为_____ ;判断制备反应结束的实验现象是_____ 。图示装置存在的两处缺陷是_____ 。
(2)已知电负性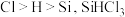 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为_____ 。
(3)采用如下方法测定溶有少量 的
的 纯度。
纯度。
 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____ ,②_____ (填操作名称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为_____ (填标号)。测得样品纯度为_____ (用含 、
、 的代数式表示)。
的代数式表示)。

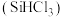 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,熔点为 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
(1)制备
 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为(2)已知电负性
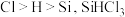 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为(3)采用如下方法测定溶有少量
 的
的 纯度。
纯度。 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2023-06-19更新
|
10715次组卷
|
16卷引用:2024届河北省实验中学高三年级上学期第一次月考化学试题
2024届河北省实验中学高三年级上学期第一次月考化学试题2023年高考山东卷化学真题(已下线)2023年高考山东卷化学真题变式题(实验综合题)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点12 硅及其无机非金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第10讲 硅及其化合物(已下线)T26-工业流程题(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点13 硅及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点46 定量分析实验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
解题方法
2 . 卤族元素及其化合物种类繁多,有着非常重要的用途,回答下列问题:
(1)基态Br原子的电子排布式为[Ar]____ 。
(2)HF分子的极性____ (填“大于”“等于”或“小于”,以下同)HCl,同一条件下,HF在水中的溶解度____ HCl,HF的沸点____ HCl。SOCl2中心S原子VSEPR模型为____ 。1mol氟硼酸铵NH4BF4中含有____ mol配位键。
(3)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为apm、apm和2apm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影,标记为n的原子分数坐标为( ,
, ,
, ),则m的原子分数坐标为
),则m的原子分数坐标为____ ,距离Hg最近的Ag有____ 个。设NA为阿伏加德罗常数的值,Ag2HgI4的摩尔质量为Mg•mol-1,该晶体的密度为____ g•cm-3(用代数式表示)。

(1)基态Br原子的电子排布式为[Ar]
(2)HF分子的极性
(3)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为apm、apm和2apm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影,标记为n的原子分数坐标为(
 ,
, ,
, ),则m的原子分数坐标为
),则m的原子分数坐标为
您最近一年使用:0次
2022-03-22更新
|
1241次组卷
|
3卷引用:河北省衡水中学2023届高三上学期三调考试化学试题
名校
3 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是___________ ,能量最低的是___________ (填序号)。
a. b.
b.
c. d.
d.
(3)Ti原子位于元素周期表中的___________ 区,最高能层电子的电子云轮廓形状为___________ ,其价电子排布式为___________ 。与Ti同周期的过渡元素中,未成对电子数最多的的基态原子的外围电子的轨道表示式___________ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+___________ Fe2+(填“大于”或“小于”)
(5)下列各组多电子原子的能级能量比较不正确的是___________
①2p=3p ②4s>2s ③4p>4f ④4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
 b.
b.
c.
 d.
d.
(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是___________
①2p=3p ②4s>2s ③4p>4f ④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次
2022-02-18更新
|
1337次组卷
|
7卷引用:河北省邯郸市大名县第一中学2021-2022学年高二上学期第二次月考化学试题
2022·山东聊城·一模
4 . 石墨烯、高温氯化钠、砷化镉等超导材料应用广泛。回答下列问题:
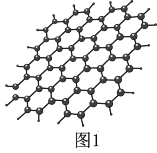
(1)石墨烯结构如图1所示,则碳原子的杂化方式为_______ ,12 g石墨烯中含有六元环个数与σ键个数之比为_______ 。
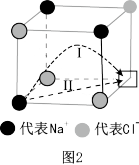
(2)温度升高时,NaCl晶体出现缺陷,如图2方格处填入Na+时,恰好构成氯化钠晶胞的 ,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径_______ (填图中序号)迁移到空位处。
(3)石墨烯限域单原子铁催化剂使CH4在室温条件下被H2O2直接氧化为HCHO、HCOOH,比较HCHO、HCOOH的沸点高低并说明理由_______ 。
(4)镉(Cd)与Zn同族且相邻,则基态Cd原子的价电子排布式为_______ ;与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3强于PH3,原因是_______ 。
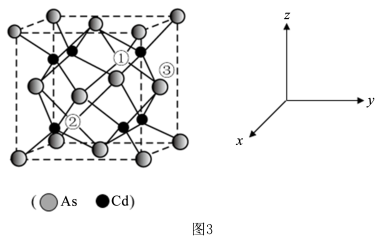
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构为正方体如图3, 占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为_______ 。晶胞的密度为 ,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为_______ pm(列计算式即可)。
(1)石墨烯结构如图1所示,则碳原子的杂化方式为

(2)温度升高时,NaCl晶体出现缺陷,如图2方格处填入Na+时,恰好构成氯化钠晶胞的
 ,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
(3)石墨烯限域单原子铁催化剂使CH4在室温条件下被H2O2直接氧化为HCHO、HCOOH,比较HCHO、HCOOH的沸点高低并说明理由
(4)镉(Cd)与Zn同族且相邻,则基态Cd原子的价电子排布式为
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构为正方体如图3,
 占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为 ,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
您最近一年使用:0次
2022-03-29更新
|
699次组卷
|
4卷引用:必刷卷05-2022年高考化学考前信息必刷卷(河北专用)
(已下线)必刷卷05-2022年高考化学考前信息必刷卷(河北专用)河北省石家庄市第二中学2022届高三2.5模化学试题山东省聊城市2021-2022学年下学期高三一模化学试题(已下线)必刷卷02-2022年高考化学考前信息必刷卷(山东专用)
2022·陕西咸阳·一模
5 . 中国科学家在国际上首次实现了CO2到淀粉的合成,不依赖植物光合作用,原料只需CO2、H2和电,相关成果发表在《科学》上。回答下列问题:
(1)CO2的空间结构为_______ 。
(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是_______ (用离子方程式表示)。
(3)淀粉在一定条件下可水解成葡萄糖(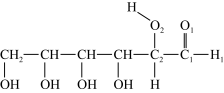 ),葡萄糖分子中键角∠H1C1O1
),葡萄糖分子中键角∠H1C1O1_______ ∠C1C2O2 (填“>”、“<”或“=”)。
(4)(CH3NH3)PbI3的晶胞结构如图所示,其中B代表Pb2+。
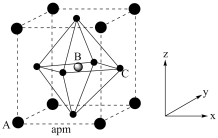
①Pb位于第六周期第IVA族,其基态原子的价电子排布图为_______ ,基态I原子核外电子占据最高能级的电子云轮廓图为_______ 。
②(CH3NH3)PbI3中涉及的短周期元素的电负性由大到小的顺序为_______ (用元素符号表示)。
③有机阳离子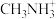 可通过CH3NH2制备,CH3NH2中C和N的杂化类型分别是
可通过CH3NH2制备,CH3NH2中C和N的杂化类型分别是_______ 、_______ 。
④_______ (填“A”或“C”)代表I-,原子分数坐标A为(0,0,0),B为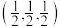 ,则C的原子分数坐标为
,则C的原子分数坐标为_______ 。NA为阿伏加德罗常数的值,则(CH3NH3)PbI3晶体的密度为_______ g∙cm-3。
(1)CO2的空间结构为
(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是
(3)淀粉在一定条件下可水解成葡萄糖(
 ),葡萄糖分子中键角∠H1C1O1
),葡萄糖分子中键角∠H1C1O1(4)(CH3NH3)PbI3的晶胞结构如图所示,其中B代表Pb2+。

①Pb位于第六周期第IVA族,其基态原子的价电子排布图为
②(CH3NH3)PbI3中涉及的短周期元素的电负性由大到小的顺序为
③有机阳离子
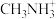 可通过CH3NH2制备,CH3NH2中C和N的杂化类型分别是
可通过CH3NH2制备,CH3NH2中C和N的杂化类型分别是④
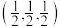 ,则C的原子分数坐标为
,则C的原子分数坐标为
您最近一年使用:0次
名校
6 . 回答下列问题:
(1)Pt的电子排布式为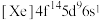 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是_______ ,处于_______ 区。
(2) 中阴离子的立体构型名称是
中阴离子的立体构型名称是_______ ,B、N、H的电负性由大到小的顺序为_______ 。
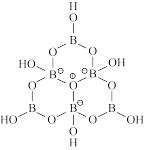
(3)科学家合成了一种含硼阴离子[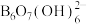 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。

①该晶体的化学式为_______ 。
②金属M原子与硼原子间最短距离为_______ pm。
③金属M的相对原子质量为_______ (列出表达式)。
(1)Pt的电子排布式为
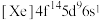 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是(2)
 中阴离子的立体构型名称是
中阴离子的立体构型名称是(3)科学家合成了一种含硼阴离子[
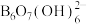 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
①该晶体的化学式为
②金属M原子与硼原子间最短距离为
③金属M的相对原子质量为
您最近一年使用:0次
2022-04-01更新
|
492次组卷
|
5卷引用:河北省石家庄市第二中学2022届高三下学期5月模拟考试化学试题
22-23高三上·辽宁沈阳·阶段练习
名校
解题方法
7 . 铜及其化合物在科学研究和工业生产中具有许多用途,请回答下列问题:
(1)写出基态Cu原子的价电子排布式_______ 。
(2)已知高温下 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因_______ 。
(3)配合物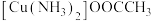 中碳原子的杂化类型是
中碳原子的杂化类型是_______ ,配体的空间构型为_______ 。配合物所含元素的电负性由大到小的顺序是_______ (用元素符号表示)。
(4)M原子的价电子排布式为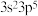 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
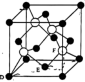
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为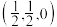 ,则F原子的坐标参数为
,则F原子的坐标参数为_______ 。
②已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为_______ pm(写出计算式)。
(1)写出基态Cu原子的价电子排布式
(2)已知高温下
 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因(3)配合物
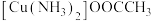 中碳原子的杂化类型是
中碳原子的杂化类型是(4)M原子的价电子排布式为
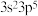 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为
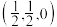 ,则F原子的坐标参数为
,则F原子的坐标参数为②已知该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为
您最近一年使用:0次
2022-10-12更新
|
459次组卷
|
4卷引用:2022年河北省高考真题变式题(14-18)
8 . 为回收利用废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等),科研人员研制了一种回收镍和硫酸铜晶体的新工艺。工艺流程如图所示:
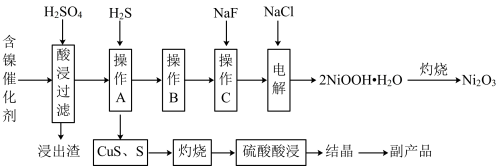
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
请回答下列问题:
(1)加快酸浸速率的常用措施有___________ (任写一条即可)。
(2)“浸出渣”主要成分为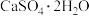 和
和___________ 两种物质。
(3)“操作B”的过程是:先在40~50℃温度下加入 ,其作用是
,其作用是___________ (用离子方程式表示);再调pH至___________ (填pH范围),操作B可除去溶液中的___________ 元素(填元素名称)。
(4)在碱性条件下,电解产生 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到 沉淀的离子方程式
沉淀的离子方程式___________ 。
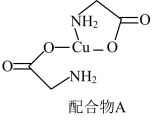
(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(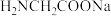 )即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
)即可得到它,配合物A中的配位原子的电负性由大到小的顺序是___________ 。

已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
请回答下列问题:
(1)加快酸浸速率的常用措施有
(2)“浸出渣”主要成分为
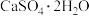 和
和(3)“操作B”的过程是:先在40~50℃温度下加入
 ,其作用是
,其作用是(4)在碱性条件下,电解产生
 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到 沉淀的离子方程式
沉淀的离子方程式(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(
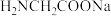 )即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
)即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
您最近一年使用:0次
2022-08-25更新
|
415次组卷
|
2卷引用:河北省石家庄市第九中学2022-2023高三上学期10月月考化学试题
名校
解题方法
9 . 硫氰酸甲基铵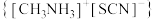 用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(
用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(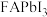 )和一种新型光电材料铯铜卤化物
)和一种新型光电材料铯铜卤化物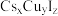 。请回答下列问题:
。请回答下列问题:
(1)基态Cu原子的电子排布式为_______ 。基态I原子的价电子排布图为_______ 。
(2)硫氰酸甲基铵所含元素中第一电离能最大的是_______ (填元素符号)。
(3)Cs、Cu、I的电负性由大到小的顺序是_______ 。
(4)甲脒( )与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是
)与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是_______ 。甲脒中碳原子的杂化方式为_______ 。
(5)水中铅的测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(结构如图)。
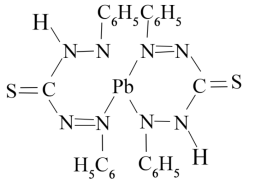
①该络合物可溶于四氯化碳,其晶体类型为_______ 。
②该络合物分子内不存在的微粒间作用力有_______ (填标号)。
a. 键 b.
键 b. 键 c.非极性键 d.离子键 e.配位键
键 c.非极性键 d.离子键 e.配位键
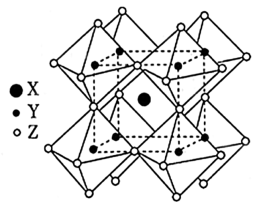
(6) 的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为
的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为_______ 。
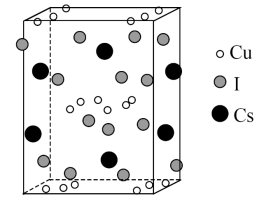
(7)某铯铜碘化物的晶胞如图所示,其晶胞参数为a nm,b nm和c nm,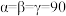 °,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为
°,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为_______  。
。
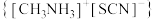 用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(
用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(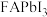 )和一种新型光电材料铯铜卤化物
)和一种新型光电材料铯铜卤化物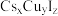 。请回答下列问题:
。请回答下列问题:(1)基态Cu原子的电子排布式为
(2)硫氰酸甲基铵所含元素中第一电离能最大的是
(3)Cs、Cu、I的电负性由大到小的顺序是
(4)甲脒(
 )与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是
)与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是(5)水中铅的测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(结构如图)。

①该络合物可溶于四氯化碳,其晶体类型为
②该络合物分子内不存在的微粒间作用力有
a.
 键 b.
键 b. 键 c.非极性键 d.离子键 e.配位键
键 c.非极性键 d.离子键 e.配位键(6)
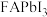 的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为
的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为
(7)某铯铜碘化物的晶胞如图所示,其晶胞参数为a nm,b nm和c nm,
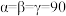 °,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为
°,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为 。
。
您最近一年使用:0次
2022-03-08更新
|
410次组卷
|
2卷引用:河北省部分名校2021-2022学年高三下学期3月份联考考试化学试题
名校
解题方法
10 .  及其化合物在生产和生活中用途广泛,回答下列问题。
及其化合物在生产和生活中用途广泛,回答下列问题。
(1) 的基态原子共有
的基态原子共有_____________ 种不同能级的电子。
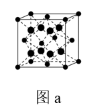
(2) 为只含有离子键的离子化合物,其晶胞结构如图a,距一个
为只含有离子键的离子化合物,其晶胞结构如图a,距一个 最近的所有
最近的所有 为顶点构成的几何形状为
为顶点构成的几何形状为_____________ 。
(3)二茂铁是最重要的金属茂基配合物,结构为一个铁原子处在两个平行的环戊二烯基环之间,结构如图b所示,已知二茂铁的一氯代物只有一种。

①二茂铁的分子式为_____________ 。
②穆斯堡尔谱学数据显示,二茂铁中学铁原子的氧化态为+2,每个茂环带有一个单位负电荷,因此每个环含有_____________ 个 电子。
电子。
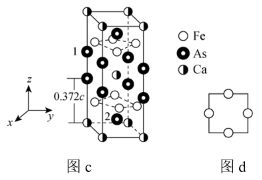
(4)一种铁基超导材料( ,相对分子质量为
,相对分子质量为 )晶胞如图c所示,图d为铁原子沿轴方向的投影图。
)晶胞如图c所示,图d为铁原子沿轴方向的投影图。
① 与
与 位于同一周期、且最外层电子数相等,但
位于同一周期、且最外层电子数相等,但 的熔点、沸点均比
的熔点、沸点均比 高,原因是
高,原因是_____________ 。
② 分子与
分子与 形成配合物后
形成配合物后 键角
键角_____________ (填“变大”“变小”或“不变”)。
③ 、
、 、
、 电负性由大到小的顺序为
电负性由大到小的顺序为_____________ 。
④ 的沸点(319℃,易升华)高于
的沸点(319℃,易升华)高于 的沸点(130.2℃),原因是
的沸点(130.2℃),原因是_____________ 。
⑤已知处于体心与顶点的 原子有着相同的化学环境,晶胞中
原子有着相同的化学环境,晶胞中 原子1的原子坐标为(0,0,0.628),则
原子1的原子坐标为(0,0,0.628),则 原子2的原子坐标为
原子2的原子坐标为_____________ 。
 及其化合物在生产和生活中用途广泛,回答下列问题。
及其化合物在生产和生活中用途广泛,回答下列问题。(1)
 的基态原子共有
的基态原子共有(2)
 为只含有离子键的离子化合物,其晶胞结构如图a,距一个
为只含有离子键的离子化合物,其晶胞结构如图a,距一个 最近的所有
最近的所有 为顶点构成的几何形状为
为顶点构成的几何形状为
(3)二茂铁是最重要的金属茂基配合物,结构为一个铁原子处在两个平行的环戊二烯基环之间,结构如图b所示,已知二茂铁的一氯代物只有一种。

①二茂铁的分子式为
②穆斯堡尔谱学数据显示,二茂铁中学铁原子的氧化态为+2,每个茂环带有一个单位负电荷,因此每个环含有
 电子。
电子。(4)一种铁基超导材料(
 ,相对分子质量为
,相对分子质量为 )晶胞如图c所示,图d为铁原子沿轴方向的投影图。
)晶胞如图c所示,图d为铁原子沿轴方向的投影图。
①
 与
与 位于同一周期、且最外层电子数相等,但
位于同一周期、且最外层电子数相等,但 的熔点、沸点均比
的熔点、沸点均比 高,原因是
高,原因是②
 分子与
分子与 形成配合物后
形成配合物后 键角
键角③
 、
、 、
、 电负性由大到小的顺序为
电负性由大到小的顺序为④
 的沸点(319℃,易升华)高于
的沸点(319℃,易升华)高于 的沸点(130.2℃),原因是
的沸点(130.2℃),原因是⑤已知处于体心与顶点的
 原子有着相同的化学环境,晶胞中
原子有着相同的化学环境,晶胞中 原子1的原子坐标为(0,0,0.628),则
原子1的原子坐标为(0,0,0.628),则 原子2的原子坐标为
原子2的原子坐标为
您最近一年使用:0次



