名校
1 . 物质世界缤纷多彩,物质的性质与分子的结构紧密关联。回答下列问题:
I.非金属氟化物在生产、生活和科研中应用广泛。
(1)基态F原子核外电子的空间运动状态有____________ 种。
(2)O、F、Cl电负性由大到小的顺序为______________ ;OF2的熔、沸点___________ (填“高于”或“低于”)Cl2O,原因是__________ 。
Ⅱ、过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应。
(3)对于基态Cr原子,下列叙述正确的是_________ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d44s2
B.从空间角度看,4s轨道比3s轨道大,其空间包含了3s轨道
C.电负性比钾高,原子对键合电子的吸引力比钾大
(4)三价铬离子能形成多种配位化合物。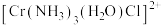 中提供孤电子对形成配位键的原子是
中提供孤电子对形成配位键的原子是___________ ,中心离子的配位数为___________ 。
(5)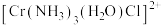 中配体分子NH3、H2O
中配体分子NH3、H2O
①键角:NH3___________ H2O(填“>”或“<”)。
②NH3极易溶于水,原因是____________ 。
(6)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是____________ 原子。设Cr和Al原子半径分别为 和
和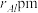 ,晶胞参数如图所示,已知:空间占有率=晶胞中原子总体积/晶胞体积,则金属原子空间占有率为
,晶胞参数如图所示,已知:空间占有率=晶胞中原子总体积/晶胞体积,则金属原子空间占有率为________ %(列出计算表达式)。
I.非金属氟化物在生产、生活和科研中应用广泛。
(1)基态F原子核外电子的空间运动状态有
(2)O、F、Cl电负性由大到小的顺序为
Ⅱ、过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应。
(3)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d44s2
B.从空间角度看,4s轨道比3s轨道大,其空间包含了3s轨道
C.电负性比钾高,原子对键合电子的吸引力比钾大
(4)三价铬离子能形成多种配位化合物。
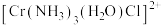 中提供孤电子对形成配位键的原子是
中提供孤电子对形成配位键的原子是(5)
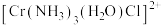 中配体分子NH3、H2O
中配体分子NH3、H2O①键角:NH3
②NH3极易溶于水,原因是
(6)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是
 和
和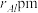 ,晶胞参数如图所示,已知:空间占有率=晶胞中原子总体积/晶胞体积,则金属原子空间占有率为
,晶胞参数如图所示,已知:空间占有率=晶胞中原子总体积/晶胞体积,则金属原子空间占有率为
您最近一年使用:0次
名校
2 . 下列实验操作及现象与对应结论匹配的是
| 选项 | 实验操作及现象 | 结论 |
| A | 将 固体粉末加入过量NaOH溶液中,充分搅拌,溶解得到无色溶液 固体粉末加入过量NaOH溶液中,充分搅拌,溶解得到无色溶液 |  既体现碱性又体现酸性 既体现碱性又体现酸性 |
| B | 向硫酸铜溶液中滴加氨水至过量,溶液由蓝色变为深蓝色 |  转化为 转化为 |
| C | 相同温度下,分别测定NaNO2和CH3COONa溶液的pH,NaNO2溶液的pH约为8,CH3COONa溶液的pH约为9 | 相同温度下,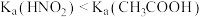 |
| D | 向5mL0.1mol/LNaOH稀溶液中滴加5滴0.1mol/L的MgCl2溶液,出现白色沉淀,再滴加5滴0.1mol/L的CuSO4溶液,出现蓝色沉淀 | 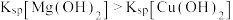 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 二氯化二硫(S2Cl2)可用于橡胶的低温硫化剂和黏接剂。其分子结构与H2O2相似,室温下稳定,100℃时分解为相应单质,与氯气反应能生成SO2。下列说法错误的是
| A.H2O2是含有极性键和非极性键的非极性分子 | B.Cl2中Cl-Cl是p-pσ键 |
| C.SO2中硫原子的杂化方式为sp2 | D.酸性:H2SO4<HClO4 |
您最近一年使用:0次
名校
解题方法
4 . 前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E的元素名称为___________ 。
(2)元素A、B、C中,电负性最大的是___________ (填元素符号 ) 。
(3)BC 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为___________ ,BC 的空间结构为
的空间结构为___________ 。
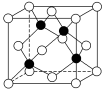
(4)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为___________ g·cm-3(用NA表示阿伏加德罗常数的值)。
(1)E的元素名称为
(2)元素A、B、C中,电负性最大的是
(3)BC
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 的空间结构为
的空间结构为(4)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为
您最近一年使用:0次
名校
解题方法
5 . 下列各种说法中错误的是
| A.形成配位键的条件是一方有空轨道,一方有孤电子对 |
| B.配位键是一种特殊的共价键 |
| C.配位化合物中的配体可以是分子也可以是阴离子 |
| D.配位键具有饱和性,没有方向性 |
您最近一年使用:0次
6 .  晶体的立方晶胞如下图所示,晶胞参数为apm,若A点原子坐标为
晶体的立方晶胞如下图所示,晶胞参数为apm,若A点原子坐标为 ,B点原子坐标为
,B点原子坐标为 ,已知阿伏加德罗常数的值为
,已知阿伏加德罗常数的值为 ,
, 的摩尔质量为232g/mol。下列说法不正确的是
的摩尔质量为232g/mol。下列说法不正确的是
 晶体的立方晶胞如下图所示,晶胞参数为apm,若A点原子坐标为
晶体的立方晶胞如下图所示,晶胞参数为apm,若A点原子坐标为 ,B点原子坐标为
,B点原子坐标为 ,已知阿伏加德罗常数的值为
,已知阿伏加德罗常数的值为 ,
, 的摩尔质量为232g/mol。下列说法不正确的是
的摩尔质量为232g/mol。下列说法不正确的是
A.该晶体中与 等距且紧邻的 等距且紧邻的 有8个 有8个 |
B.C点原子坐标为 |
C.该晶体的密度为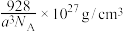 |
| D.该晶体属于离子晶体 |
您最近一年使用:0次
7 . 一种具有聚集诱导发光性能的分子结构如图所示。下列说法错误的是
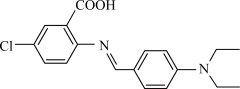
| A.分子中C原子有sp2、sp3两种杂化方式 |
| B.分子中没有手性碳原子 |
| C.1mol该物质最多可与7molH2发生加成反应 |
| D.苯环上的C-Cl键可通过苯环与氯气在光照条件下生成 |
您最近一年使用:0次
8 . 氢氟酸可以溶蚀石英玻璃,反应方程式为: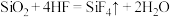 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
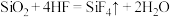 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.每60gSiO2含NA个SiO2分子 | B.标准状况下,1molHF体积为22.4L |
| C.1molH2O含有孤对电子数为2NA | D.0.1mol/L的氢氟酸中含H+数小于0.1NA |
您最近一年使用:0次
名校
9 . 超氧化钾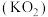 与
与 反应会生成
反应会生成 并放出
并放出 ,下列说法错误的是
,下列说法错误的是
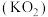 与
与 反应会生成
反应会生成 并放出
并放出 ,下列说法错误的是
,下列说法错误的是A. 的原子结构示意图为 的原子结构示意图为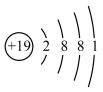 | B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 的电子式为 的电子式为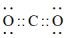 | D.核内有10个中子的氧原子表示为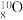 |
您最近一年使用:0次
名校
解题方法
10 . 某科研人员提出HCHO与 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
A.HAP降低了该反应的焓变( ) ) |
| B.反应过程中,发生了非极性键的断裂和生成 |
C.HCHO在反应过程中,无 键发生断裂 键发生断裂 |
D. 和 和 的中心原子上所含孤电子对数不同 的中心原子上所含孤电子对数不同 |
您最近一年使用:0次
2024-04-26更新
|
382次组卷
|
5卷引用:重庆市渝西中学2023-2024学年高二下学期4月月考化学试题



