名校
解题方法
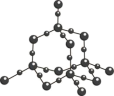
1 . 氨硼烷(NH3BH3)在一定条件下与水反应: ,
, 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是
 ,
, 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是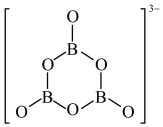
| A.NH3BH3分子中存在配位键,B原子提供孤电子对 |
| B.1molNH3BH3发生反应时转移3mole- |
| C.反应产物中只含有离子键、配位键和非极性共价键 |
| D.反应过程中B原子的杂化方式由sp2变为sp3 |
您最近一年使用:0次
2024-04-26更新
|
151次组卷
|
2卷引用:重庆市渝西中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
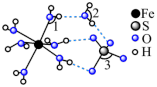
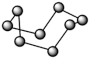
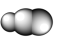
2 . 观察下列模型并结合信息,判断有关说法错误的是
| 石英 | FeSO4·7H2O | S8分子 | HCN |
|
|
|
|
| A.石英属于共价晶体,且两原子个数比为2:1 |
| B.FeSO4·7H2O结构中键角1、2、3由大到小的顺序:3>1>2 |
| C.固态硫S8中S原子为sp2杂化 |
D.HCN的结构式为 |
您最近一年使用:0次
名校
解题方法
3 . X、Y、Z、W是4种原子序数依次增大的短周期主族元素。其中Y和Z的价层电子数相同,Y原子的s能级与p能级填充的电子数相等。四种元素形成如图所示两种化合物,它们均能水解生成对应的酸和氧化物。下列说法错误的是
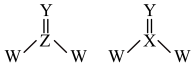
A.X的核外电子排布式为 |
B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C.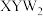 的中心原子采取 的中心原子采取 杂化 杂化 |
D.2种化合物水解得到氧化物分别为 和 和 |
您最近一年使用:0次
4 . 氮、磷、砷等元素的单质及其化合物在生产生活中应用广泛。回答下列问题:
(1) 是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用,
是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用, 分子的空间构型为
分子的空间构型为________ .
(2)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与_______ 个氮原子相连,氮化铝晶体属于__________ 晶体。
(3)M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。 键,则虚线框中氮元素采用杂化方式为
键,则虚线框中氮元素采用杂化方式为_______ ,M中存在的微粒间作用力有_______ (填标号)。
A.共价键 B.离子键 C.氢键 D.配位键
(4) 是一种重要的半导体材料,晶胞结构如图1;将
是一种重要的半导体材料,晶胞结构如图1;将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料,如图2。
的晶体中得到稀磁性半导体材料,如图2。 ,则B原子的分数坐标为
,则B原子的分数坐标为_______ ;若 晶体密度为
晶体密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞中两个
为阿伏加德罗常数的值,则晶胞中两个 原子间的最小距离为
原子间的最小距离为_________  (列出计算式即可);稀磁性半导体材料中
(列出计算式即可);稀磁性半导体材料中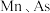 的原子个数比为
的原子个数比为_________ 。
(1)
 是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用,
是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用, 分子的空间构型为
分子的空间构型为(2)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与
(3)M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。
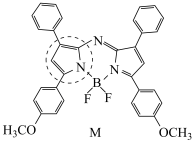
 键,则虚线框中氮元素采用杂化方式为
键,则虚线框中氮元素采用杂化方式为A.共价键 B.离子键 C.氢键 D.配位键
(4)
 是一种重要的半导体材料,晶胞结构如图1;将
是一种重要的半导体材料,晶胞结构如图1;将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料,如图2。
的晶体中得到稀磁性半导体材料,如图2。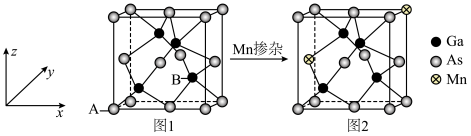
 ,则B原子的分数坐标为
,则B原子的分数坐标为 晶体密度为
晶体密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞中两个
为阿伏加德罗常数的值,则晶胞中两个 原子间的最小距离为
原子间的最小距离为 (列出计算式即可);稀磁性半导体材料中
(列出计算式即可);稀磁性半导体材料中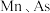 的原子个数比为
的原子个数比为
您最近一年使用:0次
名校
5 . 柠檬烯的结构式如图所示,下列说法正确的是
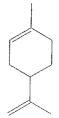
A.柠檬烯的分子式为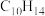 |
B. 柠檬烯最多能与 柠檬烯最多能与 发生加成反应 发生加成反应 |
C.柠檬烯分子中碳原子的杂化方式有 、 、 、 、 |
| D.柠檬烯分子的所有碳原子都可以位于同一平面内 |
您最近一年使用:0次
名校
解题方法
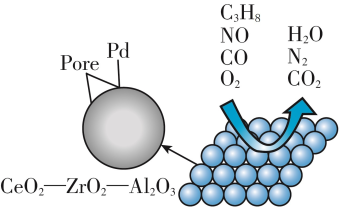
6 . 为解决汽车尾气达标排放,催化剂及其载体的选择和改良是关键。目前我国研制的稀土催化剂具有很好的催化转化效果,催化过程图如下。__________ 。
(2)CO、NO均能够与血红蛋白(Hb)中Fe2+形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。
已知:CO进入血液后有如下平衡:CO+Hb·O2 O2+Hb·CO
O2+Hb·CO
①C、N、O三种元素,第一电离能由大到小的顺序为________ ,简单氢化物的沸点由大到小的顺序为_____ (用氢化物化学式表示)。
②在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是:_______________ 。
③高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:____________ 。
(3)为节省贵金属并降低成本,常用某些复合型物质作催化剂。一种复合型物质的晶胞结构如图所示。________ 。
②已知阿伏加德罗常数的值为NA,该晶体的密度为ρg/cm3。其晶胞为立方体结构,则晶胞的边长为________ cm。
(2)CO、NO均能够与血红蛋白(Hb)中Fe2+形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。
已知:CO进入血液后有如下平衡:CO+Hb·O2
 O2+Hb·CO
O2+Hb·CO①C、N、O三种元素,第一电离能由大到小的顺序为
②在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是:
③高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:
(3)为节省贵金属并降低成本,常用某些复合型物质作催化剂。一种复合型物质的晶胞结构如图所示。

②已知阿伏加德罗常数的值为NA,该晶体的密度为ρg/cm3。其晶胞为立方体结构,则晶胞的边长为
您最近一年使用:0次
7 . 碳中和的目标是减少含碳气体的排放。CH4与CO2都能引起温室效应,将二者联合处理不仅可以减缓温室气体排放,还可以转化为CH3OH、CH3COOH、H2等高附加值产品。
(1)CH4与CO2在一定条件下能发生如下两个反应:
Ⅰ.CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1=+247kJ/mol
2CO(g)+2H2(g) ΔH1=+247kJ/mol
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ/mol
CO(g)+H2O(g) ΔH2=+41kJ/mol
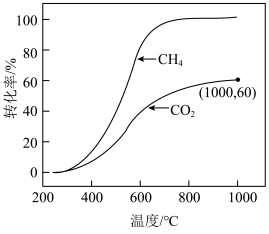
若CH4与CO2按物质的量之比1∶3投料在某恒容密闭容器中发生上述反应,一定时间内CH4与CO2的转化率随温度的变化如图所示,其中CO2在1000℃时的平衡转化率为60%,CH4在1000℃时的平衡转化率几乎为100%。_______ 下能自发进行(填“高温”或“低温”)。
②温度高于700℃ 时,随温度升高,平衡产物中H2O的体积分数_______ (填“增大”“减小”或“不变”)。
③1000℃时反应Ⅱ 的平衡常数K=_______ (保留3位有效数字,下同),平衡时CO的体积分数为_______ 。
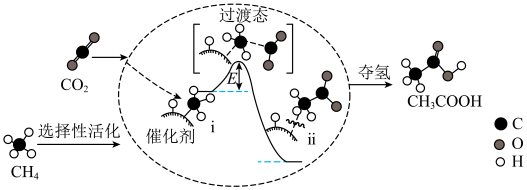
(2)CH4与CO2在催化剂作用下反应可生成CH3COOH,其反应机理如图所示。_______ 。
②转化过程中经历了i→ii的变化,该变化过程_______ (填“吸热”或“放热”)。产物CH3COOH中碳原子的杂化方式为_______ 。
③甲醇(CH3OH)与氧气形成的燃料电池是新能源汽车等领域常用的电池。通常以石墨为电极,KOH溶液为电解质溶液,该电池放电时,负极反应式为_______ 。
(1)CH4与CO2在一定条件下能发生如下两个反应:
Ⅰ.CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1=+247kJ/mol
2CO(g)+2H2(g) ΔH1=+247kJ/molⅡ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ/mol
CO(g)+H2O(g) ΔH2=+41kJ/mol若CH4与CO2按物质的量之比1∶3投料在某恒容密闭容器中发生上述反应,一定时间内CH4与CO2的转化率随温度的变化如图所示,其中CO2在1000℃时的平衡转化率为60%,CH4在1000℃时的平衡转化率几乎为100%。
②温度高于700℃ 时,随温度升高,平衡产物中H2O的体积分数
③1000℃时反应Ⅱ 的平衡常数K=
(2)CH4与CO2在催化剂作用下反应可生成CH3COOH,其反应机理如图所示。
②转化过程中经历了i→ii的变化,该变化过程
③甲醇(CH3OH)与氧气形成的燃料电池是新能源汽车等领域常用的电池。通常以石墨为电极,KOH溶液为电解质溶液,该电池放电时,负极反应式为
您最近一年使用:0次
名校
解题方法
8 . 氟元素可形成多种有工业价值和科研价值的化合物,如OF2、(CF)x、XeF2、HF、NH4BF4、CaF2等。
(1)基态F原子核外电子有______ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填序号)。
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p2 D.1s22s22p33p2
(2)F2通入稀NaOH溶液中可生成OF2,其中氧原子的杂化方式为_________ 。
(3)AlF3的熔点为1090℃,远高于AlCl3的熔点(192℃),其原因是___________ 。
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,(CF)x的导电性________ (填“增强”或“减弱”),(CF)x中C-C键的键长比石墨中C-C键的_______ (填“长”或“短”)。

(5)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂HF、NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为________ ,1mol氟硼酸铵(NH4BF4)中含有_______ mol配位键。
(1)基态F原子核外电子有
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p2 D.1s22s22p33p2
(2)F2通入稀NaOH溶液中可生成OF2,其中氧原子的杂化方式为
(3)AlF3的熔点为1090℃,远高于AlCl3的熔点(192℃),其原因是
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,(CF)x的导电性

(5)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂HF、NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为
您最近一年使用:0次
名校
9 . 配合物在许多方面有着广泛的应用。下列叙述不正确的是
| A.以Mg2+为中心的大环配合物叶绿素能催化光合作用 |
| B.魔术表演中常用一种含硫氰化铁配离子的溶液来代替血液 |
| C.[Ag(NH3)2]+是化学镀银试剂的有效成分 |
| D.向溶液中逐滴加入氨水,可除去硫酸锌溶液中的Cu2+ |
您最近一年使用:0次
名校
解题方法
10 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)元素F简单离子的价电子排布式为___________ ;写出元素G在周期表中的位置___________ 。
(2)B与氢元素形成的简单气态氢化物的空间构型为___________ ,C与氢元素形成的简单气态氢化物的VSEPR模型为___________ 。
(3)C、D、E三种元素的简单离子半径由大到小的顺序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为___________ 。
(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”);M的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为___________ 。
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: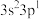 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)B与氢元素形成的简单气态氢化物的空间构型为
(3)C、D、E三种元素的简单离子半径由大到小的顺序为
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO
 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次