1 .  是周期表中
是周期表中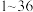 号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.
号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.
(1) 的电子式为
的电子式为______________ , 中含有的化学键类型为
中含有的化学键类型为______________ .
(2)B、C两种元素的第三电离能由大到小的顺序为______________ (填元素符号)
(3)E在元素周期表中位置为______________ ,位于元素周期表的______________ 区.
(4)比较:①键角大小:
______________  ;②在水中的溶解性大小
;②在水中的溶解性大小
______________  ;
;
 是周期表中
是周期表中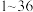 号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.
号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.(1)
 的电子式为
的电子式为 中含有的化学键类型为
中含有的化学键类型为(2)B、C两种元素的第三电离能由大到小的顺序为
(3)E在元素周期表中位置为
(4)比较:①键角大小:

 ;②在水中的溶解性大小
;②在水中的溶解性大小
 ;
;
您最近一年使用:0次
解题方法
2 . 过渡金属( 等)在工业生产中有重要的作用,是化学工作者研究的对象。
等)在工业生产中有重要的作用,是化学工作者研究的对象。
(1) 的结构示意图如图-1所示。
的结构示意图如图-1所示。

①基态 的核外电子排布式为
的核外电子排布式为___________ 。
②图中 与
与 之间形成的化学键称为
之间形成的化学键称为___________ 。
③ 能与
能与 结合成
结合成 ,
, 中的键角
中的键角_______  中的键角(填“>”、“<”或“=”)
中的键角(填“>”、“<”或“=”)
(2)锰元素能形成很多重要的化合物。
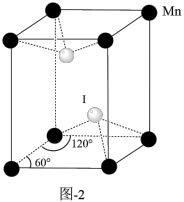
①锰与碘形成的某种化合物的晶胞结构如图-2所示,该化合物的化学式为___________ 。
② 能形成配合物
能形成配合物 ,其配离子的结构如图-3所示(配体位于顶点)。若
,其配离子的结构如图-3所示(配体位于顶点)。若 该配合物与足量
该配合物与足量 反应生成
反应生成 沉淀,则化学式中的n为
沉淀,则化学式中的n为___________ 。

③三醋酸锰由硝酸锰晶体和乙酸酐反应制得。乙酸酐[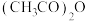 ]可由
]可由 在一定条件下脱水形成,其结构如图-4所示,
在一定条件下脱水形成,其结构如图-4所示, 乙酸酐中所含的
乙酸酐中所含的 键数目为
键数目为___________ 。已知羧酸是一大类含羧基( )的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释
)的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释 的酸性大于
的酸性大于 的原因:
的原因:___________ 。

 等)在工业生产中有重要的作用,是化学工作者研究的对象。
等)在工业生产中有重要的作用,是化学工作者研究的对象。(1)
 的结构示意图如图-1所示。
的结构示意图如图-1所示。
①基态
 的核外电子排布式为
的核外电子排布式为②图中
 与
与 之间形成的化学键称为
之间形成的化学键称为③
 能与
能与 结合成
结合成 ,
, 中的键角
中的键角 中的键角(填“>”、“<”或“=”)
中的键角(填“>”、“<”或“=”)(2)锰元素能形成很多重要的化合物。
①锰与碘形成的某种化合物的晶胞结构如图-2所示,该化合物的化学式为

②
 能形成配合物
能形成配合物 ,其配离子的结构如图-3所示(配体位于顶点)。若
,其配离子的结构如图-3所示(配体位于顶点)。若 该配合物与足量
该配合物与足量 反应生成
反应生成 沉淀,则化学式中的n为
沉淀,则化学式中的n为
③三醋酸锰由硝酸锰晶体和乙酸酐反应制得。乙酸酐[
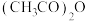 ]可由
]可由 在一定条件下脱水形成,其结构如图-4所示,
在一定条件下脱水形成,其结构如图-4所示, 乙酸酐中所含的
乙酸酐中所含的 键数目为
键数目为 )的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释
)的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释 的酸性大于
的酸性大于 的原因:
的原因:
您最近一年使用:0次
名校
解题方法
3 . 铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)Cu在周期表中位于___________ 区,Cu2+价电子排布式为___________ 。
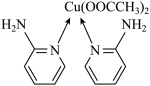
(2)邻氨基吡啶( )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为___________ ;1mol 中σ键的数目为
中σ键的数目为___________ 。邻氨基吡啶的铜配合物结构简式如下图所示,C原子轨道杂化类型为___________ 。
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是___________ 。
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是___________ 。
(1)Cu在周期表中位于
(2)邻氨基吡啶(
 )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为 中σ键的数目为
中σ键的数目为
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是
您最近一年使用:0次
2023-07-05更新
|
151次组卷
|
2卷引用:江苏省泰州中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
4 . N、P、Sb原子的最外层电子数都是5,与卤素原子形成的化合物有广泛用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌,
可用于面粉的漂白和杀菌, 广泛应用于农药、杀虫剂的制造,
广泛应用于农药、杀虫剂的制造, 常用于有机反应催化剂。
常用于有机反应催化剂。
(1)几种化学键的键能如下表所示:
由两种单质化合形成1mol  ,焓变
,焓变
___________  。
。
(2)已知: 常温常压下为无色气体,熔点-129℃,沸点-207℃;
常温常压下为无色气体,熔点-129℃,沸点-207℃; 为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
① 热稳定性高于
热稳定性高于 :
:___________ 。
② 熔、沸点高于
熔、沸点高于 :
:___________ 。
(3) 在水中溶解度不大,而
在水中溶解度不大,而 在水中溶解度较大,由此判断是
在水中溶解度较大,由此判断是
___________ 分子, 是
是___________ 分子。(填“极性”或“非极性”)
 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌,
可用于面粉的漂白和杀菌, 广泛应用于农药、杀虫剂的制造,
广泛应用于农药、杀虫剂的制造, 常用于有机反应催化剂。
常用于有机反应催化剂。(1)几种化学键的键能如下表所示:
| 化学键 |  |  |  |
键能/ | 941.6 | 154.8 | 283.0 |
 ,焓变
,焓变
 。
。(2)已知:
 常温常压下为无色气体,熔点-129℃,沸点-207℃;
常温常压下为无色气体,熔点-129℃,沸点-207℃; 为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:①
 热稳定性高于
热稳定性高于 :
:②
 熔、沸点高于
熔、沸点高于 :
:(3)
 在水中溶解度不大,而
在水中溶解度不大,而 在水中溶解度较大,由此判断是
在水中溶解度较大,由此判断是
 是
是
您最近一年使用:0次
2023-06-20更新
|
205次组卷
|
3卷引用:上海交通大学附属中学2022-2023学年高一下学期期末考试(等级考)化学试题
上海交通大学附属中学2022-2023学年高一下学期期末考试(等级考)化学试题上海交通大学附属中学2022-2023学年高一下学期期末考试(等级考)化学试题(已下线)专题02 反应热的测量和计算-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
名校
5 . 依据相关知识回答下列问题:
Ⅰ.键能是指在25 ℃、101 kPa,将1 mol理想气体分子AB拆开为中性气态原子A和B时所需要的能量。显然键能越大,化学键越牢固,含有该键的分子越稳定。
(1)已知键能:H-H键为436 kJ•mol-1;H-F键为565 kJ•mol-1;H-Cl键为431 kJ•mol-1;H-Br键为366 kJ•mol-1。则下列分子受热时最稳定的是_______。
(2)能用键能大小解释的是_______。
(3)已知:H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成lmol NH3过程中放出46kJ的热量。则N≡N的键能为_______ kJ/mol。
Ⅱ.CO与H2反应可制备CH3OH,由CH3OH和O2构成的质子交换膜燃料电池的结构示意图如下。
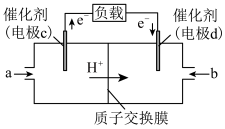
(4)电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是_______ (填“正极”或“负极”),c电极的电极反应式为_______ 。若外电路中转移2 mol电子,则上述燃料电池所消耗的O2在标准状况下的体积为_______ L。
(5)下列反应中,属于吸热反应的是_______ (填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败 ⑥Ba(OH)2•8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
Ⅰ.键能是指在25 ℃、101 kPa,将1 mol理想气体分子AB拆开为中性气态原子A和B时所需要的能量。显然键能越大,化学键越牢固,含有该键的分子越稳定。
(1)已知键能:H-H键为436 kJ•mol-1;H-F键为565 kJ•mol-1;H-Cl键为431 kJ•mol-1;H-Br键为366 kJ•mol-1。则下列分子受热时最稳定的是_______。
| A.HF | B.HCl | C.HBr | D.H2 |
| A.氮气的化学性质比氧气稳定 | B.常温常压下溴呈液态,碘呈固态 |
| C.稀有气体一般很难发生化学反应 | D.硝酸易挥发而硫酸难挥发 |
Ⅱ.CO与H2反应可制备CH3OH,由CH3OH和O2构成的质子交换膜燃料电池的结构示意图如下。

(4)电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是
(5)下列反应中,属于吸热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败 ⑥Ba(OH)2•8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
您最近一年使用:0次
解题方法
6 . 半导体材料的发展带动了科技的进步,如传统半导体Si、Ge,新型半导体GaAs、AlN、GaN等。回答下列问题:
(1)基态Ge原子的价电子排布式为______ ,与其同周期的IIIB族元素属于______ 区。
(2)根据元素周期律可判知:原子半径Al______ N(填“>”或“<”,下同),还原性As3—______ Br—。
(3)Ga、Ge、As的第一电离能由大到小的顺序为______ ;Ge、As的常见化合物有GeCl4、AsH3、AsCl5,其中呈正四面体结构的是______ 。
(4)AlN结构中只存在N-Al键,每个原子周围都满足8e—结构,AlN中______ (填“存在”或“不存在”)配位键。
(5)Si与C是同主族相邻元素,C原子之间可以形成双键、三键,但Si原子之间难以形成双键或三键,从原子结构角度分析其原因______ 。
(1)基态Ge原子的价电子排布式为
(2)根据元素周期律可判知:原子半径Al
(3)Ga、Ge、As的第一电离能由大到小的顺序为
(4)AlN结构中只存在N-Al键,每个原子周围都满足8e—结构,AlN中
(5)Si与C是同主族相邻元素,C原子之间可以形成双键、三键,但Si原子之间难以形成双键或三键,从原子结构角度分析其原因
您最近一年使用:0次
解题方法
7 . 回答下列问题:
(1) 与
与 同族且相邻,写出基态
同族且相邻,写出基态 原子的价层电子排布图:
原子的价层电子排布图:___________ 。
(2)O和S处于同一主族,第一电离能较大的是___________ 。 和
和 分子中的键角较大的是
分子中的键角较大的是___________ ,键长较短的是___________ 。单质硫与热的 浓溶液反应的产物之一为
浓溶液反应的产物之一为 ,
,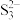 的空间构型为
的空间构型为___________ 。
(3)Cu2+能与吡咯( )的阴离子(
)的阴离子( )形成双吡咯铜。已知吡咯分子中的大π键可用符号
)形成双吡咯铜。已知吡咯分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则吡咯分子中的大π键应表示为
),则吡咯分子中的大π键应表示为___________ 。吡咯分子中N原子的杂化类型为___________ , 吡咯分子中含有
吡咯分子中含有___________  键,
键,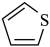 噻吩的沸点为
噻吩的沸点为 ,吡咯(
,吡咯(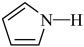 )的沸点在
)的沸点在 之间,吡咯沸点较高,其原因是
之间,吡咯沸点较高,其原因是___________ 。
(4)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度: ,则下列物质酸性由强到弱的顺序是
,则下列物质酸性由强到弱的顺序是___________ 。
(1)
 与
与 同族且相邻,写出基态
同族且相邻,写出基态 原子的价层电子排布图:
原子的价层电子排布图:(2)O和S处于同一主族,第一电离能较大的是
 和
和 分子中的键角较大的是
分子中的键角较大的是 浓溶液反应的产物之一为
浓溶液反应的产物之一为 ,
,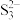 的空间构型为
的空间构型为(3)Cu2+能与吡咯(
 )的阴离子(
)的阴离子( )形成双吡咯铜。已知吡咯分子中的大π键可用符号
)形成双吡咯铜。已知吡咯分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则吡咯分子中的大π键应表示为
),则吡咯分子中的大π键应表示为 吡咯分子中含有
吡咯分子中含有 键,
键, 噻吩的沸点为
噻吩的沸点为 ,吡咯(
,吡咯( )的沸点在
)的沸点在 之间,吡咯沸点较高,其原因是
之间,吡咯沸点较高,其原因是(4)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:
 ,则下列物质酸性由强到弱的顺序是
,则下列物质酸性由强到弱的顺序是A. | B. |
C. | D. |
您最近一年使用:0次
名校
解题方法
8 . Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的阴离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物中Q的杂化类型为___ ,分子中含有____ 个σ键,____ 个π键。
(2)R的氢化物分子的立体构型是____ ,R与X形成的化合物可作为一种重要的陶瓷材料,其化学式是____ 。
(3)X的常见氢化物的立体构型是____ ;键角___ ;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是____ 。
(4)Q分别与Y、Z形成的共价化合物的化学式是____ 和____ ;
(1)Q的最高价氧化物中Q的杂化类型为
(2)R的氢化物分子的立体构型是
(3)X的常见氢化物的立体构型是
(4)Q分别与Y、Z形成的共价化合物的化学式是
您最近一年使用:0次



