1 .  、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有___________ 种;O、S、Cl电负性由大到小的顺序是___________ 。
(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是___________ (填化学式);键长 最长的是
最长的是___________ (填化学式)。已知:配离子的颜色与 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
___________  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为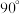 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为___________ 。若阿伏加德罗常数的值为 ,化合物
,化合物 的密度
的密度
___________  (用含
(用含 的代数式表示)。
的代数式表示)。
 、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: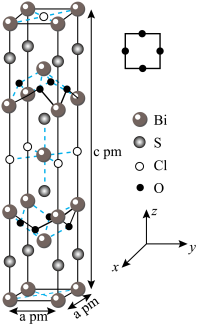
 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是
 最长的是
最长的是 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
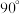 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为 ,化合物
,化合物 的密度
的密度
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
2 .  汽车尾气处理系统的原理是利用
汽车尾气处理系统的原理是利用 脱除
脱除 并转化为
并转化为 。
。
(1)已知在25℃, 时:
时:
反应ⅰ:

反应ⅱ: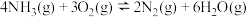
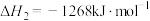
反应ⅲ:

________ 
(2)当 与
与 的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为
的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为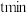 ,
, 的脱除率随温度变化的曲线如下图所示:
的脱除率随温度变化的曲线如下图所示: 与
与 的物质的量之比为
的物质的量之比为________ 。
②若曲线a中 的起始浓度为
的起始浓度为 ,则在900℃时
,则在900℃时 的脱除速率为
的脱除速率为________  。
。
③在800℃~1100℃时,催化剂活性较稳定。则 脱除的最佳温度为
脱除的最佳温度为________ ℃, 的脱除率在最佳温度之前逐渐增大的原因是
的脱除率在最佳温度之前逐渐增大的原因是________ 。
④940℃时,反应ⅲ的平衡常数
________ (用物质的量分数代替浓度,列计算式)。
⑤若其它条件不变,提高催化剂的活性,940℃时 的脱除率
的脱除率________ (选填“增大”“减小”或“不变”)。
(3)一定比例的 和
和 也能很好的脱除
也能很好的脱除 ,某催化反应机理如下图所示:
,某催化反应机理如下图所示: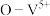 表示V化合价为
表示V化合价为 价,其它相似)
价,其它相似)
①该反应的催化剂为________ 。
② 转化为
转化为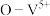 过程中
过程中 与
与 的物质的量比为
的物质的量比为________ 。
③ 转化为
转化为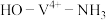 ,
, 键角增大的原因是
键角增大的原因是________ 。
 汽车尾气处理系统的原理是利用
汽车尾气处理系统的原理是利用 脱除
脱除 并转化为
并转化为 。
。(1)已知在25℃,
 时:
时:反应ⅰ:


反应ⅱ:
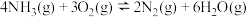
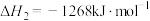
反应ⅲ:



(2)当
 与
与 的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为
的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为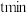 ,
, 的脱除率随温度变化的曲线如下图所示:
的脱除率随温度变化的曲线如下图所示:
 与
与 的物质的量之比为
的物质的量之比为②若曲线a中
 的起始浓度为
的起始浓度为 ,则在900℃时
,则在900℃时 的脱除速率为
的脱除速率为 。
。③在800℃~1100℃时,催化剂活性较稳定。则
 脱除的最佳温度为
脱除的最佳温度为 的脱除率在最佳温度之前逐渐增大的原因是
的脱除率在最佳温度之前逐渐增大的原因是④940℃时,反应ⅲ的平衡常数

⑤若其它条件不变,提高催化剂的活性,940℃时
 的脱除率
的脱除率(3)一定比例的
 和
和 也能很好的脱除
也能很好的脱除 ,某催化反应机理如下图所示:
,某催化反应机理如下图所示:
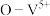 表示V化合价为
表示V化合价为 价,其它相似)
价,其它相似)①该反应的催化剂为
②
 转化为
转化为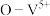 过程中
过程中 与
与 的物质的量比为
的物质的量比为③
 转化为
转化为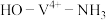 ,
, 键角增大的原因是
键角增大的原因是
您最近一年使用:0次
解题方法
3 . 乙醚是一种极易挥发的无色透明液体。乙醚长时间与空气接触时,逐渐生成过氧化乙醚( )。
)。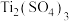 、
、 、
、 可除去过氧化乙醚。回答下列问题:
可除去过氧化乙醚。回答下列问题:
(1)基态 、O、
、O、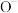 的第一电离能
的第一电离能 按由大到小排序为
按由大到小排序为___________ 。
(2)基态 还原过氧化乙醚时失去的是
还原过氧化乙醚时失去的是___________ 轨道电子,从电负性角度判断 中H的化合价为
中H的化合价为___________ 。 中
中 键的化学键类型为
键的化学键类型为___________ ,中心原子的杂化轨道类型为___________ 。
(3)一个过氧化乙醚分子中,价层电子对数目为4的原子有___________ 个。过氧化乙醚分子中的键能如下:
造成 键键能小于
键键能小于 键键能的可能原因是
键键能的可能原因是___________ 。
(4)乙醚沸点35.6℃,丙酸( )沸点为141℃,两者沸点差异较大的主要原因是
)沸点为141℃,两者沸点差异较大的主要原因是___________ 。
(5)硫酸亚铁的正交晶胞参数为 、
、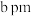 、
、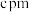 ,
, ,晶胞沿c轴、a轴的投影图见下,假设阿伏加德罗常数的值为
,晶胞沿c轴、a轴的投影图见下,假设阿伏加德罗常数的值为 。
。___________  ,晶体密度为
,晶体密度为___________  (列出算式)。
(列出算式)。
 )。
)。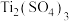 、
、 、
、 可除去过氧化乙醚。回答下列问题:
可除去过氧化乙醚。回答下列问题:(1)基态
 、O、
、O、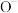 的第一电离能
的第一电离能 按由大到小排序为
按由大到小排序为(2)基态
 还原过氧化乙醚时失去的是
还原过氧化乙醚时失去的是 中H的化合价为
中H的化合价为 中
中 键的化学键类型为
键的化学键类型为(3)一个过氧化乙醚分子中,价层电子对数目为4的原子有
| 单键 |  |  |  |  |  |
键能/( ) ) | 346 | 411 | 358 | 207 | 459 |
 键键能小于
键键能小于 键键能的可能原因是
键键能的可能原因是(4)乙醚沸点35.6℃,丙酸(
 )沸点为141℃,两者沸点差异较大的主要原因是
)沸点为141℃,两者沸点差异较大的主要原因是(5)硫酸亚铁的正交晶胞参数为
 、
、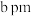 、
、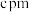 ,
, ,晶胞沿c轴、a轴的投影图见下,假设阿伏加德罗常数的值为
,晶胞沿c轴、a轴的投影图见下,假设阿伏加德罗常数的值为 。
。
 ,晶体密度为
,晶体密度为 (列出算式)。
(列出算式)。
您最近一年使用:0次
4 . 硼族元素可形成许多结构和性质特殊的化合物,回答下列问题:
(1)过硼酸钠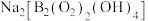 被用于洗衣粉中作增白剂,其阴离子结构如图所示
被用于洗衣粉中作增白剂,其阴离子结构如图所示 ,该阴离子组成元素中第一电离能最大的元素是
,该阴离子组成元素中第一电离能最大的元素是______ ,该物质可用于增白的原因是______ 。
(2)硼酸三甲酯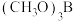 由硼酸
由硼酸 和甲醇互相反应而制得。熔沸点
和甲醇互相反应而制得。熔沸点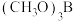
______  (填“>”或“<”或“=”),原因是
(填“>”或“<”或“=”),原因是______ 。比较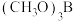 和
和 中
中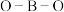 键角的大小顺序是
键角的大小顺序是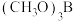
______  (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
(3)氮化硼晶体有多种结构,六方相氮化硼结构与石墨相似,但不具有导电性。六方氮化硼中与B距离最近且相等的B有______ 个。
(4)科学家利用 和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为
和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为______ ,晶胞参数: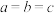 (单位nm),
(单位nm), 。若
。若 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为______  。
。
(1)过硼酸钠
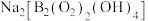 被用于洗衣粉中作增白剂,其阴离子结构如图所示
被用于洗衣粉中作增白剂,其阴离子结构如图所示 ,该阴离子组成元素中第一电离能最大的元素是
,该阴离子组成元素中第一电离能最大的元素是(2)硼酸三甲酯
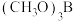 由硼酸
由硼酸 和甲醇互相反应而制得。熔沸点
和甲醇互相反应而制得。熔沸点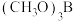
 (填“>”或“<”或“=”),原因是
(填“>”或“<”或“=”),原因是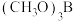 和
和 中
中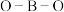 键角的大小顺序是
键角的大小顺序是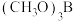
 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。(3)氮化硼晶体有多种结构,六方相氮化硼结构与石墨相似,但不具有导电性。六方氮化硼中与B距离最近且相等的B有
(4)科学家利用
 和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为
和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为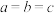 (单位nm),
(单位nm), 。若
。若 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
5 . 铁、钴、镍位于元素周期表中第四周期第Ⅷ族,它们的单质及其化合物在化工生产中用途广泛.回答下列问题:
(1)基态铁原子价电子排布图为________________ ;第四周期元素中基态原子未成对电子数与钴相同的还有________ (填元素符号);
(2)向含 的溶液中加入过量氨水,最终会得到黄色的
的溶液中加入过量氨水,最终会得到黄色的 ,在空气中易被氧化为橙黄色的
,在空气中易被氧化为橙黄色的 ;
;
①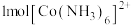 中含有
中含有 键的物质的量为
键的物质的量为________ ; 中存在
中存在________ (填选项字母);
A. 键 B.离子键 C.配位键 D.金属键
键 B.离子键 C.配位键 D.金属键
②与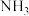 相比,
相比, 中的
中的
________ (填“较大”或“较小”),原因为________________ ;
③ 被氧化为
被氧化为 的离子方程式为
的离子方程式为________________ ;
(3)由钾、镍、氟三种元素组成的某晶体常应用于光化学领域,其四方晶胞结构及晶胞参数如图.该晶体中镍的配位数为________ ;设 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为________ 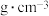 (列出计算式即可);
(列出计算式即可);
(1)基态铁原子价电子排布图为
(2)向含
 的溶液中加入过量氨水,最终会得到黄色的
的溶液中加入过量氨水,最终会得到黄色的 ,在空气中易被氧化为橙黄色的
,在空气中易被氧化为橙黄色的 ;
;①
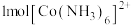 中含有
中含有 键的物质的量为
键的物质的量为 中存在
中存在A.
 键 B.离子键 C.配位键 D.金属键
键 B.离子键 C.配位键 D.金属键②与
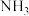 相比,
相比, 中的
中的
③
 被氧化为
被氧化为 的离子方程式为
的离子方程式为(3)由钾、镍、氟三种元素组成的某晶体常应用于光化学领域,其四方晶胞结构及晶胞参数如图.该晶体中镍的配位数为
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为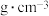 (列出计算式即可);
(列出计算式即可);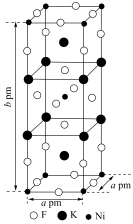
您最近一年使用:0次
解题方法
6 . 卤族元素是形成化合物的常见元素。请回答:
(1)含Na、Cl、Al三种元素的某化合物,其晶体部分结构如图所示。其化学式是___________ ,晶体类型是___________ 。错误 的是___________。
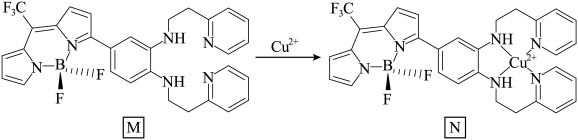
(3)一种比率光生探针M与铜离子配位,可用于小鼠脑内Cu(Ⅱ)的高时空分辨率动态成像。反应如下所示:___________ 。
②M中键角∠F-B-F___________ BF3中键角∠F-B-F(填“>”、“<”、“=”),请说明理由___________ 。
(4)在水中,氟化氢是一种弱酸,但氟化氢却是酸性很强的溶剂,其酸度与无水硫酸相当,能够给予氟化氢质子的化合物是很少的。如HNO3在HF溶剂中存在如下反应: 。则HNO3在HF溶剂中呈
。则HNO3在HF溶剂中呈___________ (填“酸性”、“中性”、“碱性”)
(1)含Na、Cl、Al三种元素的某化合物,其晶体部分结构如图所示。其化学式是

A.电负性: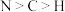 | B.第一电离能: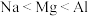 |
C.离子半径: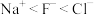 | D. 的简化电子排布式: 的简化电子排布式: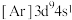 |
(3)一种比率光生探针M与铜离子配位,可用于小鼠脑内Cu(Ⅱ)的高时空分辨率动态成像。反应如下所示:
②M中键角∠F-B-F
(4)在水中,氟化氢是一种弱酸,但氟化氢却是酸性很强的溶剂,其酸度与无水硫酸相当,能够给予氟化氢质子的化合物是很少的。如HNO3在HF溶剂中存在如下反应:
 。则HNO3在HF溶剂中呈
。则HNO3在HF溶剂中呈
您最近一年使用:0次
名校
解题方法
7 . 氮族元素可以形成多种多样的化合物,回答下列问题:
(1)基态As原子的价电子的轨道表示式是______ 。
(2)叠氮酸(HN3)常用于引爆剂,可用联氨( )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
______ 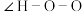 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: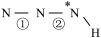 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①______ ②。
(3)乙胺( )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是______ 。
(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是______ 。

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是______ ,n原子的分数坐标是______ ,若阿伏加德罗常数值为 ,该晶体密度是
,该晶体密度是______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态As原子的价电子的轨道表示式是
(2)叠氮酸(HN3)常用于引爆剂,可用联氨(
 )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
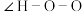 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: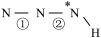 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①(3)乙胺(
 )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为
 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是 ,该晶体密度是
,该晶体密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-05-21更新
|
507次组卷
|
2卷引用:山东省潍坊市2024届高三下学期二模化学试题
8 . 硫元素化合物非常丰富,应用广泛。
请回答:
(1)由钾、镍、硫三种元素组成的某电极材料的晶胞如图,已知钾离子位于晶胞顶点及体心,其化学式是___________ ,与钾离子直接相邻的元素是___________ (填元素符号)。
(3)①硫酰卤( ):
):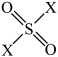 ,分子中S原子的杂化方式为:
,分子中S原子的杂化方式为:___________ ;比较键角
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
请回答:
(1)由钾、镍、硫三种元素组成的某电极材料的晶胞如图,已知钾离子位于晶胞顶点及体心,其化学式是
A.基态S原子的价层电子排布图: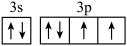 |
B.第一电离能: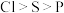 |
| C.K、Ni同为第四周期金属元素,都处于元素周期表d区 |
D.离子半径: |
(3)①硫酰卤(
 ):
): ,分子中S原子的杂化方式为:
,分子中S原子的杂化方式为:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②氟磺酸(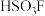 )属于超酸,可看作
)属于超酸,可看作 部分水解形成的产物。氟磺酸酸性比硫酸强。请从分子结构上说明氟磺酸酸性强的原因:
部分水解形成的产物。氟磺酸酸性比硫酸强。请从分子结构上说明氟磺酸酸性强的原因: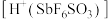 ,由
,由 (
(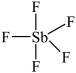 )与
)与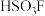 等物质的量化合生成。写出其中阴离子的结构式:
等物质的量化合生成。写出其中阴离子的结构式:
您最近一年使用:0次
解题方法
9 .  固体发生如下转化。
固体发生如下转化。
(1) 固体中所含的化学键为
固体中所含的化学键为_______ ,写出加“过量氯水”后的溶液中的所有阴离子_______ 。
(2)下列说法不正确的是_______。
(3)请依据非氧化还原反应,设计实验验证“固体混合物”中含硫元素的微粒__________ 。
(4)写出 与足量炭黑反应的化学方程式
与足量炭黑反应的化学方程式_______ 。
 固体发生如下转化。
固体发生如下转化。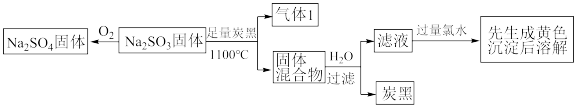
(1)
 固体中所含的化学键为
固体中所含的化学键为(2)下列说法不正确的是_______。
A. 的键角比 的键角比 的键角大 的键角大 |
B.只用稀硝酸不能验证 是否全部氧化为 是否全部氧化为 |
| C.气体1可用作高温炼铁的原料气 |
| D.过滤时,滤纸要对折两次后打开成圆锥形,放入漏斗且紧贴内壁 |
(3)请依据非氧化还原反应,设计实验验证“固体混合物”中含硫元素的微粒
(4)写出
 与足量炭黑反应的化学方程式
与足量炭黑反应的化学方程式
您最近一年使用:0次
名校
10 . I.金属催化剂M(Co、Ni)催化硼氢化钠( )水解释放
)水解释放 机理如下图所示:
机理如下图所示:

(1)过程Ⅱ中形成化学键的类型有________(填序号)。
(2) 最终会转化为
最终会转化为 ,1个
,1个 中存在
中存在________ 个配位键。
(3) 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为________ 。
Ⅱ.过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为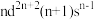 ,中子数为31,
,中子数为31,
(4)Q原子符号为________ ;基态Q原子核外成对电子数和未成对电子数之比为________ 。
Ⅲ. 、
、 是新型磁性材料的成分。依据其中有关元素回答问题:
是新型磁性材料的成分。依据其中有关元素回答问题:
(5)钕(Nd)属于镧系元素,则其在元素周期表中处于________ 区,Co元素在元素周期表中的位置________ 。
Ⅳ.分子式为 的化合物的结构如图,
的化合物的结构如图,
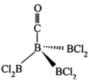
(6)其中B原子的杂化类型是________ ,B-B-B键的键角________ Cl-B-Cl的键角(填“ ”“
”“ ”或“
”或“ ”)。
”)。
 )水解释放
)水解释放 机理如下图所示:
机理如下图所示:
(1)过程Ⅱ中形成化学键的类型有________(填序号)。
| A.离子键 | B.金属键 | C.极性键 | D.非极性键 |
(2)
 最终会转化为
最终会转化为 ,1个
,1个 中存在
中存在(3)
 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为Ⅱ.过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为
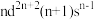 ,中子数为31,
,中子数为31,(4)Q原子符号为
Ⅲ.
 、
、 是新型磁性材料的成分。依据其中有关元素回答问题:
是新型磁性材料的成分。依据其中有关元素回答问题:(5)钕(Nd)属于镧系元素,则其在元素周期表中处于
Ⅳ.分子式为
 的化合物的结构如图,
的化合物的结构如图,
(6)其中B原子的杂化类型是
 ”“
”“ ”或“
”或“ ”)。
”)。
您最近一年使用:0次



