名校
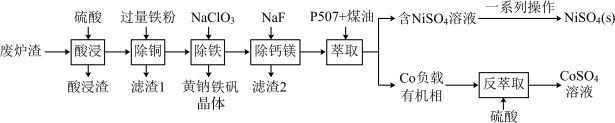
1 . 镍、钴是重要的战略物资,但资源匮乏。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如下:
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)Co2+ 的价电子排布式________ , 空间构型为
空间构型为________
(2)提高“酸浸”速率的方法有_________ 。(任写一条)
(3)“滤渣1”的主要成分是_________ 。(写化学式)
(4)黄钠铁矾的化学式为Na2 Fe 6(SO4)4(OH)12,“除铁”的离子方程式为___________ 。
(5)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是________ (结合平衡理论解释)。Ca2+和Mg2+沉淀完全时,溶液中F-的浓度c(F- )最小为______ mol·L-1(已知离子浓度≤10-5 mol·L-1时,认为该离子沉淀完全,Ksp(CaF2)=1.0 ×10-10,Ksp(MgF2)=7.5×10-11)。
(6)获得NiSO4(s)的“一系列操作”是________ 。
(7)工艺流程中,可循环利用的物质是___________ 。
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)Co2+ 的价电子排布式
 空间构型为
空间构型为(2)提高“酸浸”速率的方法有
(3)“滤渣1”的主要成分是
(4)黄钠铁矾的化学式为Na2 Fe 6(SO4)4(OH)12,“除铁”的离子方程式为
(5)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(6)获得NiSO4(s)的“一系列操作”是
(7)工艺流程中,可循环利用的物质是
您最近一年使用:0次
解题方法
2 . 锌是一种应用广泛的金属,工业上以菱锌矿(主要成分是 、ZnO,含少量
、ZnO,含少量 和
和 )制备锌单质的流程如下:
)制备锌单质的流程如下:
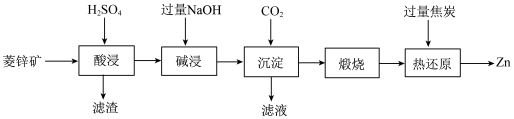
已知:
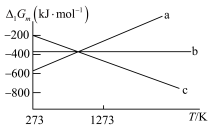
a.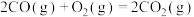

b.
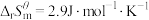
c.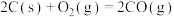
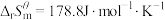
反应a,b,c的自由能变随温度的变化关系如图所示。
下列说法错误的是
 、ZnO,含少量
、ZnO,含少量 和
和 )制备锌单质的流程如下:
)制备锌单质的流程如下:
已知:
a.
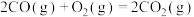

b.

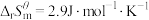
c.
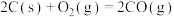
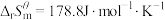
反应a,b,c的自由能变随温度的变化关系如图所示。

下列说法错误的是
| A.硫酸根离子的VSEPR模型为正四面体 |
| B.“酸浸”过程中加入食盐可增加滤渣的量 |
C.“沉淀”过程中,消耗 与 与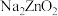 的物质的量之比为1∶1 的物质的量之比为1∶1 |
D.“热还原”过程中,发生主要反应的化学方程式为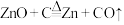 |
您最近一年使用:0次
名校
解题方法
3 . 锰酸锂(LiMn2O4) 可作为某锂离子电池的正极材料,工业上利用软锰矿浆(主要成分为 MnO2,含少量 Fe2O3、FeO、Al2O3、SiO2。等杂质)吸收含硫烟气(主要成分 SO2) 制备锰酸锂,生产流程如图所示:

已知:①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强;
②在此流程中部分金属阳离子生成氢氧化物沉淀的 pH 如下表:
(1)含硫烟气中 SO2的VSEPR模型为___________ 。
(2)含硫烟气在通入软锰矿浆前需要先冷却,冷却的原因是___________ 。
(3)请写出含硫烟气在通入软锰矿浆后与 MnO2发生反应的化学方程式:___________ 。
(4)滤液1中所含金属阳离子除 以外还有
以外还有___________ (填离子符号)。
(5)由“滤液1”得到“滤液2”同时回收 Al(OH)3的实验方案如下:边搅拌边向滤液1中加入___________ ,再加入NaOH溶液调节pH范围为___________ ,过滤得到滤液 2 和滤渣,请设计实验方案由滤渣制得纯净 Al(OH)3[Al(OH)3在 pH≥12时溶解]的实验方案:___________ 。
(6)在实际生产中, Li2CO3与 MnO2按物质的量之比1:4混合均匀在 600℃~750℃制取 LiMn2O4,请写出该反应的化学方程式:___________ 。
(7)为测定锰酸锂的纯度, 取2.00g产品置于锥形瓶中, 向其中加入2.68g Na2C2O4和足量硫酸,充分反应后,用0.100mol/L KMnO4标准溶液滴定未反应完的 H2C2O4,到达滴定终点时消耗标准 KMnO4溶液20.00mL,已知:
 则该产品中锰酸锂的质量分数为
则该产品中锰酸锂的质量分数为___________ 。

已知:①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强;
②在此流程中部分金属阳离子生成氢氧化物沉淀的 pH 如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)含硫烟气中 SO2的VSEPR模型为
(2)含硫烟气在通入软锰矿浆前需要先冷却,冷却的原因是
(3)请写出含硫烟气在通入软锰矿浆后与 MnO2发生反应的化学方程式:
(4)滤液1中所含金属阳离子除
 以外还有
以外还有(5)由“滤液1”得到“滤液2”同时回收 Al(OH)3的实验方案如下:边搅拌边向滤液1中加入
(6)在实际生产中, Li2CO3与 MnO2按物质的量之比1:4混合均匀在 600℃~750℃制取 LiMn2O4,请写出该反应的化学方程式:
(7)为测定锰酸锂的纯度, 取2.00g产品置于锥形瓶中, 向其中加入2.68g Na2C2O4和足量硫酸,充分反应后,用0.100mol/L KMnO4标准溶液滴定未反应完的 H2C2O4,到达滴定终点时消耗标准 KMnO4溶液20.00mL,已知:

 则该产品中锰酸锂的质量分数为
则该产品中锰酸锂的质量分数为
您最近一年使用:0次
名校
4 . 下列说法不正确的是
A.CO 、NO 、NO 、SO 、SO 中心原子都是sp2杂化 中心原子都是sp2杂化 |
| B.NH3、PCl3、H3O+的空间结构都是三角锥 |
| C.CO2、SO3都是由极性键构成的非极性分子 |
| D.CH2=CHCN分子中的σ键和π键的比为2∶1 |
您最近一年使用:0次
解题方法
5 . 下列各组分子或离子的空间结构不相似 的是
| A.CO2和OF2 | B.NH 和CH4 和CH4 | C.H3O+和NH3 | D.SO2和O3 |
您最近一年使用:0次
解题方法
6 . 含硅化合物在生活中的应用非常广泛。请回答下列问题:
(1)祖母绿宝石的主要成分化学式为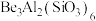 ,
, 与
与 的第一电离能大小关系为:
的第一电离能大小关系为:
___________ 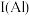 。
。
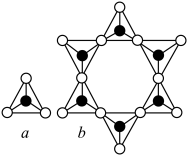
(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是___________ (不能用最简式表示)。
(3)工业制备高纯硅,先用焦炭在电炉中将石英还原为粗硅,再将粗硅与 在300℃反应生成
在300℃反应生成 ,氯原子的价层电子排布式为
,氯原子的价层电子排布式为___________ , 的空间构型为
的空间构型为___________ 。
(4)硅的各种卤化物的沸点如下表,沸点依次升高的原因是___________ 。
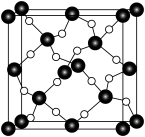
(5)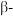 石英是晶质石英(
石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为___________ ,请用价层电子对互斥模型解释图中键角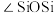 并不是
并不是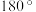 的原因是
的原因是___________ 。
(1)祖母绿宝石的主要成分化学式为
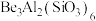 ,
, 与
与 的第一电离能大小关系为:
的第一电离能大小关系为:
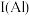 。
。(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为
 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是
(3)工业制备高纯硅,先用焦炭在电炉中将石英还原为粗硅,再将粗硅与
 在300℃反应生成
在300℃反应生成 ,氯原子的价层电子排布式为
,氯原子的价层电子排布式为 的空间构型为
的空间构型为(4)硅的各种卤化物的沸点如下表,沸点依次升高的原因是
 |  | 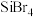 |  | |
| 沸点/K | 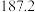 | 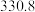 | 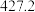 | 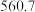 |
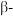 石英是晶质石英(
石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为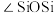 并不是
并不是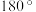 的原因是
的原因是
您最近一年使用:0次
解题方法
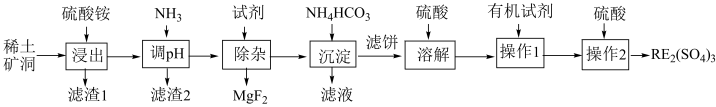
7 . 我国稀土工艺技术水平世界领先。从离子型稀土矿中(含RE、K、Al、Mg、Si、F等多种铝硅酸盐化合物,RE代表稀土元素)通过阳离子交换法提取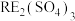 工艺流程如图。
工艺流程如图。
已知:①稀土矿中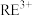 、
、 、
、 等主要吸附于铝硅酸盐中,稀土元素离子
等主要吸附于铝硅酸盐中,稀土元素离子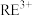
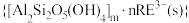 和杂质离子
和杂质离子 在矿洞中可与加入的盐溶液发生阳离子交换,将
在矿洞中可与加入的盐溶液发生阳离子交换,将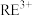 与
与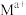 从铝硅酸盐中交换出来。
从铝硅酸盐中交换出来。
②常温下部分难溶物的溶度积如表:
③pH对稀土和铝浸出率的影响如图:

回答下列问题:
(1)“滤渣1”中存在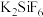 ,其阴离子的空间构型为
,其阴离子的空间构型为___________ 。“浸出”时最佳 为4.5,大于4.5稀土浸出率降低,解释原因
为4.5,大于4.5稀土浸出率降低,解释原因___________ 。
(2)矿洞中“浸出”时发生复杂反应,写出稀土离子交换的离子方程式___________ (注明物质状态)。
(3)“沉淀”稀土离子的离子方程式为___________ 。
(4)回收利用“滤液”的操作单元是___________ 。
(5)“操作2”的名称为___________ ,实验室进行该步操作需要用到的玻璃仪器有___________ 。
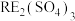 工艺流程如图。
工艺流程如图。
已知:①稀土矿中
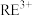 、
、 、
、 等主要吸附于铝硅酸盐中,稀土元素离子
等主要吸附于铝硅酸盐中,稀土元素离子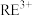
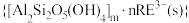 和杂质离子
和杂质离子 在矿洞中可与加入的盐溶液发生阳离子交换,将
在矿洞中可与加入的盐溶液发生阳离子交换,将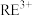 与
与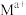 从铝硅酸盐中交换出来。
从铝硅酸盐中交换出来。②常温下部分难溶物的溶度积如表:
| 物质 |  |  | 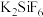 |
 | 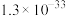 |  |  |

回答下列问题:
(1)“滤渣1”中存在
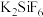 ,其阴离子的空间构型为
,其阴离子的空间构型为 为4.5,大于4.5稀土浸出率降低,解释原因
为4.5,大于4.5稀土浸出率降低,解释原因(2)矿洞中“浸出”时发生复杂反应,写出稀土离子交换的离子方程式
(3)“沉淀”稀土离子的离子方程式为
(4)回收利用“滤液”的操作单元是
(5)“操作2”的名称为
您最近一年使用:0次
22-23高二下·全国·期中
解题方法
8 . 氯吡苯脲是一种常用的膨大剂,其结构简式为 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为___________ 。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型有___________ ,羰基碳原子的杂化轨道类型为___________ 。
(3)已知,可用异氰酸苯酯与2-氯-4-氨基吡啶反应生成氯吡苯脲: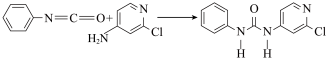 ,反应过程中,每生成
,反应过程中,每生成 氯吡苯脲,断裂
氯吡苯脲,断裂___________  键,断裂
键,断裂___________ 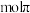 键。
键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有 、
、 、
、 等。
等。
①请用共价键的相关知识解释 分子比
分子比 分子稳定的原因:
分子稳定的原因:___________ 。
② 分子的空间结构是
分子的空间结构是___________ ,中心原子的杂化类型是___________ 。
 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。(1)氯元素基态原子核外电子的未成对电子数为
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型有
(3)已知,可用异氰酸苯酯与2-氯-4-氨基吡啶反应生成氯吡苯脲:
 ,反应过程中,每生成
,反应过程中,每生成 氯吡苯脲,断裂
氯吡苯脲,断裂 键,断裂
键,断裂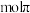 键。
键。(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有
 、
、 、
、 等。
等。①请用共价键的相关知识解释
 分子比
分子比 分子稳定的原因:
分子稳定的原因:②
 分子的空间结构是
分子的空间结构是
您最近一年使用:0次
名校
解题方法
9 . I.工业中可利用生产钛白的副产物FeSO4·7H2O和硫铁矿(FeS2)联合制备铁精粉(FexOy)和硫酸,实现能源及资源的有效利用。
(1)FeSO4·7H2O结构示意图如图:
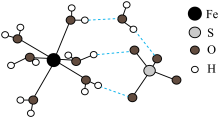
①Fe2+的价层电子排布式为_____ 。
②H2O中O和SO 中S均为sp3杂化,比较H2O中H-O-H键角和SO
中S均为sp3杂化,比较H2O中H-O-H键角和SO 中O-S-O键角的大小并解释原因
中O-S-O键角的大小并解释原因____ 。
③FeSO4·7H2O中H2O与Fe2+、H2O与SO 的作用力类型分别是
的作用力类型分别是_____ 。
(2)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图:
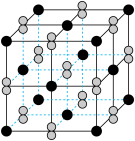
①Fe2+的配位数_____ 个。
②FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数为NA,晶体的密度为_____ g•cm-3。(1nm=10—9m)
Ⅱ.四氟肼(N2F4)可作高能燃料的氧化剂,可用Fe3+与二氟胺(HNF2)反应制得,发生的反应是2HNF2+2Fe3+=N2F4↑+2Fe2++2H+,请回答有关问题:
(3)F原子最外层电子排布式_____ ;N原子核外不同运动状态的电子有_____ 种;N2的电子式_____ ;F元素的非金属性比N强,用原子结构的知识说明理由:_____ 。
(4)HNF2中N元素的化合价是_____ ;反应中氧化剂与还原剂的物质的量之比为_____ ;若生成0.1molN2F4,电子转移数是____ 。
(1)FeSO4·7H2O结构示意图如图:

①Fe2+的价层电子排布式为
②H2O中O和SO
 中S均为sp3杂化,比较H2O中H-O-H键角和SO
中S均为sp3杂化,比较H2O中H-O-H键角和SO 中O-S-O键角的大小并解释原因
中O-S-O键角的大小并解释原因③FeSO4·7H2O中H2O与Fe2+、H2O与SO
 的作用力类型分别是
的作用力类型分别是(2)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图:

①Fe2+的配位数
②FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数为NA,晶体的密度为
Ⅱ.四氟肼(N2F4)可作高能燃料的氧化剂,可用Fe3+与二氟胺(HNF2)反应制得,发生的反应是2HNF2+2Fe3+=N2F4↑+2Fe2++2H+,请回答有关问题:
(3)F原子最外层电子排布式
(4)HNF2中N元素的化合价是
您最近一年使用:0次
解题方法
10 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布“嫦娥五号”最新科学成果:中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”。“嫦娥石”是一种新的磷酸盐矿物,属于陨磷钠镁钙石(Merrillite)族,颗粒约2~30微米,伴生矿物有钛铁矿等。回答下列问题:
(1)基态钛原子价电子排布式为_______ 。
(2)Fe的配合物有多种。 、
、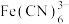 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是_______ (写元素符号,下同);第一电离能由大到小的顺序为_______ 。
(3)磷酸为磷的最高价含氧酸,其空间结构如图:
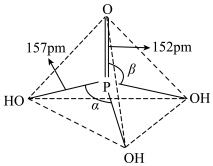
①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是_______ 。
② 的立体构型为
的立体构型为_______ ,中心原子的杂化类型是_______ 。
(4)反型钙钛矿电池无须使用具有光催化活性的 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
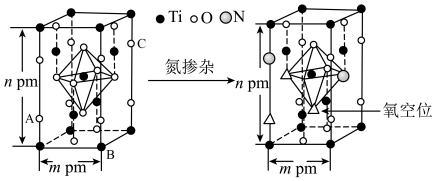
 晶体中
晶体中
_______ ;已知原子A、B的分数坐标分别为 和
和 ,则原子C的坐标为
,则原子C的坐标为_______ ,设阿伏加德罗常数的值为 ,
, 的密度为
的密度为_______ g·cm 。
。
(1)基态钛原子价电子排布式为
(2)Fe的配合物有多种。
 、
、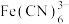 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是(3)磷酸为磷的最高价含氧酸,其空间结构如图:

①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
②
 的立体构型为
的立体构型为(4)反型钙钛矿电池无须使用具有光催化活性的
 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
 晶体中
晶体中
 和
和 ,则原子C的坐标为
,则原子C的坐标为 ,
, 的密度为
的密度为 。
。
您最近一年使用:0次
2023-01-02更新
|
391次组卷
|
3卷引用:吉林省部分学校2022-2023学年高三上学期12月联考化学试题



