解题方法
1 . X、Z、Q、R、T为前四周期元素,且原子序数依次增大。X和Q属同族元素,X和R可形成化合物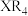 ;
; 为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;
为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;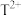 的3d轨道中有5个电子。请回答下列问题。
的3d轨道中有5个电子。请回答下列问题。
(1)Z基态原子的电子排布式是___________ ;
(2)利用价层电子对互斥模型判断 的空间结构是
的空间结构是___________ ;
(3)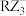 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为___________ 。
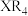 ;
; 为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;
为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;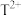 的3d轨道中有5个电子。请回答下列问题。
的3d轨道中有5个电子。请回答下列问题。(1)Z基态原子的电子排布式是
(2)利用价层电子对互斥模型判断
 的空间结构是
的空间结构是(3)
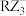 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为
您最近一年使用:0次
名校
解题方法
2 . 中国早在周朝已能冶炼铸铁了。目前,铁及其化合物广泛地应用到各个领域。请回答下列问题:
(1)基态铁原子的电子排布式为_______ 。
(2)我国菱铁矿FeCO3储量较为丰富。其中CO 的空间结构为
的空间结构为_______ 。
(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是_______ 。
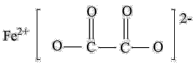
(4)Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20℃、103.6℃左右。因此可知Fe(CO)5属于_______ 晶体。
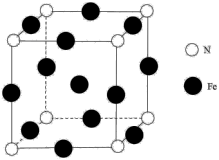
(5)铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是_______ 。若该晶体的密度是dg·cm-3,则两个最近的Fe间的距离为_______ cm(设NA为阿伏加德罗常数的值)。
(1)基态铁原子的电子排布式为
(2)我国菱铁矿FeCO3储量较为丰富。其中CO
 的空间结构为
的空间结构为(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是
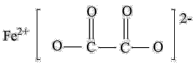
(4)Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20℃、103.6℃左右。因此可知Fe(CO)5属于
(5)铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是

您最近一年使用:0次
名校
解题方法
3 . 请回答下列问题:
(1)铱(Ir)与钴为同族元素,其核外电子占据最高能层的符号为 p,则基态 Ir 原子的价电子排布式为_______ 。
(2)下列状态的钙中,电离最外层一个电子所需能量最大的是_______(填标号);
(3)N、P、O、S 的简单氢化物性质的比较:
①热稳定性:NH3>PH3,其原因是_______ ,
②在乙醇中的溶解度:H2O>H2S,其原因是_______ ;
(4)H3O+离子和 SeO3分子的空间构型分别是_______ 、_______ ,O、F、S 电负性由大到小的顺序为_______ ;
(1)铱(Ir)与钴为同族元素,其核外电子占据最高能层的符号为 p,则基态 Ir 原子的价电子排布式为
(2)下列状态的钙中,电离最外层一个电子所需能量最大的是_______(填标号);
A.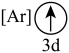 | B.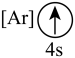 | C.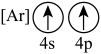 | D.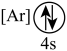 |
①热稳定性:NH3>PH3,其原因是
②在乙醇中的溶解度:H2O>H2S,其原因是
(4)H3O+离子和 SeO3分子的空间构型分别是
您最近一年使用:0次
名校
解题方法
4 .  为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A.0.5 mol 中氙的价层电子对数为 中氙的价层电子对数为 |
B.23 g 中 中 杂化的原子数为 杂化的原子数为 |
| C.氢键(X-H…Y)中三原子在一条直线上时,作用力最强 |
D.标准状况下,11.2 L CO和 的混合气体中分子数为 的混合气体中分子数为 |
您最近一年使用:0次
名校
解题方法
5 . 下列化学用语或图示表达正确的是
A.基态氮原子价电子的轨道表示式: |
B. 的电子式: 的电子式: |
C. 的VSEPR模型: 的VSEPR模型: |
D.2-丁烯的反式结构: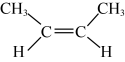 |
您最近一年使用:0次
名校
6 . 下列关于杂化轨道的叙述中,不正确的是( )
| A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 |
| B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| C.NH3和CH4两个分子中中心原子N和C都是通过sp3杂化轨道成键 |
D.ClO 的立体构型为平面三角形 的立体构型为平面三角形 |
您最近一年使用:0次
2023-06-08更新
|
76次组卷
|
2卷引用:广东省梅州市兴宁市齐昌中学2022-2023学年高三上学期第二次质检考试化学试题
解题方法
7 . 我国科研团队揭示利用氢化钡进行固氮加氢产氨的过程如图所示,下列说法正确的是
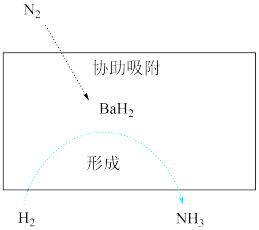

A.1molN2中约含有 个质子 个质子 |
B.根据该固氮反应,22.4LN2被还原生成2mol |
C. 的立体构型为三角锥形 的立体构型为三角锥形 |
| D.氢化钡中含有离子键和共价键 |
您最近一年使用:0次
名校
解题方法
8 . SiH4与NH3制备氮化硅(熔点1900℃)的反应为 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是| A.熔点:单晶硅>氮化硅 | B.未成对电子数:Si<N |
| C.键角:SiH4>NH3 | D.NH3是由极性键构成的三角锥形分子 |
您最近一年使用:0次
名校
解题方法
9 .  能吸收有害紫外线,保护人类赖以生存的空间。
能吸收有害紫外线,保护人类赖以生存的空间。 的分子结构如图,呈V形,两个键的夹角为116.5°,三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这些电子。
的分子结构如图,呈V形,两个键的夹角为116.5°,三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这些电子。 ,新生状态的“O”具有极强氧化性,请回答:
,新生状态的“O”具有极强氧化性,请回答:

(1)下列分子与 分子的结构最相似的是___________。
分子的结构最相似的是___________。
(2)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那么 分子有
分子有___________ 对孤对电子。
(3) 中“特殊的化学键”是
中“特殊的化学键”是___________ 键(填“ ”或“
”或“ ”)。中心原子的杂化方式为
”)。中心原子的杂化方式为___________ 。
(4)配平反应___________ :_______PbS+_______ _______
_______ _______
_______
 能吸收有害紫外线,保护人类赖以生存的空间。
能吸收有害紫外线,保护人类赖以生存的空间。 的分子结构如图,呈V形,两个键的夹角为116.5°,三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这些电子。
的分子结构如图,呈V形,两个键的夹角为116.5°,三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这些电子。 ,新生状态的“O”具有极强氧化性,请回答:
,新生状态的“O”具有极强氧化性,请回答:
(1)下列分子与
 分子的结构最相似的是___________。
分子的结构最相似的是___________。A. | B. | C. | D. |
 分子有
分子有(3)
 中“特殊的化学键”是
中“特殊的化学键”是 ”或“
”或“ ”)。中心原子的杂化方式为
”)。中心原子的杂化方式为(4)配平反应
 _______
_______ _______
_______
您最近一年使用:0次
名校
解题方法
10 . 将少量硫酸铜溶液滴入氨基乙酸钠溶液(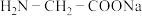 )中即可得到结构如图所示的产物。下列叙述错误的是
)中即可得到结构如图所示的产物。下列叙述错误的是
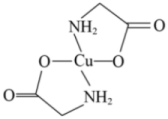
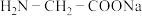 )中即可得到结构如图所示的产物。下列叙述错误的是
)中即可得到结构如图所示的产物。下列叙述错误的是
A.氨基乙酸钠中的氮原子采取 杂化 杂化 |
B.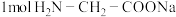 中含有 中含有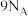 个 个 键 键 |
C.产物中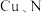 原子VSEPR模型均为四面体形结构 原子VSEPR模型均为四面体形结构 |
| D.该反应产物为配合物,只有内界而无外界 |
您最近一年使用:0次



