名校
解题方法
1 . 铂钴合金在磁控、仪表等领域有重要用途。回答下列问题:
(1)基态Co原子价层电子的轨道表达式为___________ ;Co与Ca处于同一周期,且核外最外层电子构型相同,但金属Co的熔点比金属Ca的高,原因为________________ 。
(2)Pt与Cl、吡啶( )能形成如图所示两种分子。
)能形成如图所示两种分子。
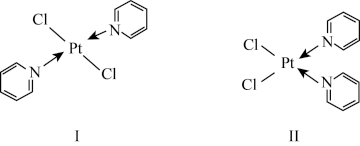
①吡啶中所含同周期元素的第一电离能由小到大的顺序为________________ 。
②1mol化合物Ⅰ中含有 键的数目为
键的数目为__________________ 。
③相同条件下,两种化合物中在水中溶解度更大的为__ (填“Ⅰ”或“Ⅱ”),原因为____ 。
(3)某Pt-Co合金的晶体堆积模型为面心立方堆积,其中Co原子处于顶角位置、Pt原子处于面心位置,则该合金的化学式为_______ 。
(4)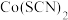 可用于检验可卡因。其中阴离子的立体构型为
可用于检验可卡因。其中阴离子的立体构型为 __ ,碳原子的杂化形式为____ 。
(5)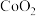 是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。
是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。
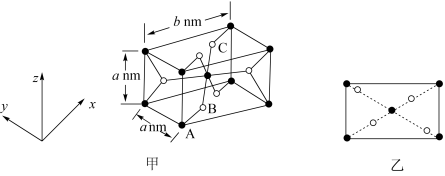
①原子坐标参数:A为(0,0,0);B为(0.31,0.31,0)。则C原子的坐标参数为__ 。
②若阿伏加 德罗常数的值为 ,则晶体密度为
,则晶体密度为___  (列出计算表达式)。
(列出计算表达式)。
(1)基态Co原子价层电子的轨道表达式为
(2)Pt与Cl、吡啶(
 )能形成如图所示两种分子。
)能形成如图所示两种分子。
①吡啶中所含同周期元素的第一电离能由小到大的顺序为
②1mol化合物Ⅰ中含有
 键的数目为
键的数目为③相同条件下,两种化合物中在水中溶解度更大的为
(3)某Pt-Co合金的晶体堆积模型为面心立方堆积,其中Co原子处于顶角位置、Pt原子处于面心位置,则该合金的化学式为
(4)
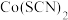 可用于检验可卡因。其中阴离子的立体构型为
可用于检验可卡因。其中阴离子的立体构型为 (5)
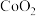 是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。
是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。
①原子坐标参数:A为(0,0,0);B为(0.31,0.31,0)。则C原子的坐标参数为
②若阿伏加 德罗常数的值为
 ,则晶体密度为
,则晶体密度为 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
名校
2 . 氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过______ 方法区分晶体准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为______ 。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______ ,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是______ (各举一例)。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是______ ;氟化铵中存在______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图(a)计算相关键能。则F-F键的键能为______ kJ•mol-1,S-F键的键能为______ kJ•mol-1。
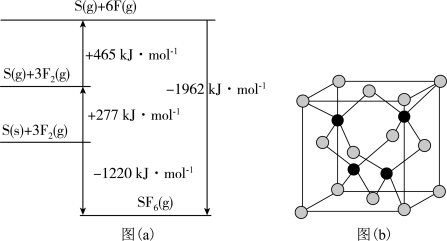
(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是______
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=______ nm(列出计算式)。
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态F原子的价层电子排布图(轨道表达式)为
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是
A.离子键 B.σ键 C.π键 D.氢键
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图(a)计算相关键能。则F-F键的键能为

(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=
您最近一年使用:0次
2019-10-28更新
|
351次组卷
|
2卷引用:西藏自治区拉萨中学2020届高三上学期第四次月考理综化学试题
3 . 碳、铜、锡及其化合物有许多用途。回答下列问题
(1)在元素周期表里,锡和碳同族,锡在第五周期。基态锡原子的价电子排布式为__________ ,据此推测,锡的常见正价是__________ 。
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为__________ ;P、S的第一电离能(I1)的大小为I1(P) __________ I1(S)(填“>”“<”或“=”)
(3)CO32-中C原子的杂化轨道类型为__________ ;乙烯分子中σ键与π键数目之比为__________ 。
(4)NH3的沸点__________ (填“高于”或“低于”)PH3的沸点,原因是____________________ 。
(5)磷青铜晶体的晶胞结构如图所示,该晶体中P原子位于由铜原子形成的__________ 的空隙中。若晶体密度为ag·cm-3,P与最近的Cu原子的核间距为__________ nm(用含NA的代数式表示)。

(1)在元素周期表里,锡和碳同族,锡在第五周期。基态锡原子的价电子排布式为
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为
(3)CO32-中C原子的杂化轨道类型为
(4)NH3的沸点
(5)磷青铜晶体的晶胞结构如图所示,该晶体中P原子位于由铜原子形成的

您最近一年使用:0次
4 . 钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________ ;K、F、Zn的电负性从大到小的顺序为___________ 。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________ 。
(3)OF2分子的几何构型为___________ ,中心原子的杂化类型为___________ 。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在___________ ;与O3-互为等电子体的分子为___________ (任 写一种 )。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。
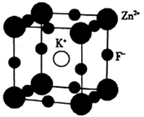
①晶胞中Zn2+的配位数为___________ 个。
②晶胞中紧邻的两个F-间的距离为_______________________ (列出算式即可)nm。
③该晶体的密度为___________ (列出算式即可,用NA表示阿伏伽德罗常数的数值)g·cm-3。
(1)基态锌原子的价电子排布式为
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是
(3)OF2分子的几何构型为
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为
②晶胞中紧邻的两个F-间的距离为
③该晶体的密度为
您最近一年使用:0次
2018-01-07更新
|
409次组卷
|
6卷引用:西藏拉萨市拉萨中学2022届高三上学期第一次月考理综化学试题



