名校
解题方法
1 . ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_____ ;

原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为_____ ;
Se原子序数为_____ ,其核外M层电子的排布式为_____ ;
 离子的立体构型为
离子的立体构型为_____ ;
ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为_____ g·cm-3(列式并计算)。
(2)
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为
Se原子序数为
 离子的立体构型为
离子的立体构型为ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为
(2)

您最近一年使用:0次
名校
解题方法
2 . 氮及其化合物在工、农业生产中用途广泛。
(1)基态氮原子的核外电子排布式为_______ ;与N同周期的主族元素中,电负性大于N的有 _______ 种。
(2)NaN3在强烈撞击的情况下快速分解并产生大量氮气,可用于汽车安全气囊的制造。写出一种与N 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:_______ ,N 的空间构型为
的空间构型为 _______ 。
(3)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是_______ 。
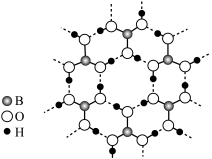
(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。

①分子中的大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),已知N
),已知N 为平面结构且含有大π键,则N
为平面结构且含有大π键,则N 中的大π键应表示为
中的大π键应表示为 _______ 。
②图中虚线代表氢键,其表示式为(NH )N﹣H•••Cl、
)N﹣H•••Cl、_______ 、_______ 。
(5)氮化硼(BN)和碳一样可以形成像石墨那样的平面六角形的层状结构,如图1所示,其中B原子的杂化方式为_______ 。该氮化硼晶体具有良好的润滑性,其原因是 _______ 。
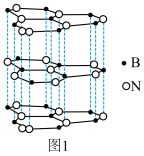
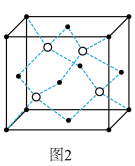
(6)一定条件下,层型BN可转变为立方氮化硼,其晶胞结构如图2所示。一个晶胞中所含B原子的数目为_______ ;已知晶体的密度为dg•cm﹣3,NA为阿伏加德罗常数的值,则晶胞边长为 _______ pm(用含d、NA的代数式表示)。
(1)基态氮原子的核外电子排布式为
(2)NaN3在强烈撞击的情况下快速分解并产生大量氮气,可用于汽车安全气囊的制造。写出一种与N
 互为等电子体的分子的化学式:
互为等电子体的分子的化学式: 的空间构型为
的空间构型为 (3)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是
(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。

①分子中的大π键可用符号Π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),已知N
),已知N 为平面结构且含有大π键,则N
为平面结构且含有大π键,则N 中的大π键应表示为
中的大π键应表示为 ②图中虚线代表氢键,其表示式为(NH
 )N﹣H•••Cl、
)N﹣H•••Cl、(5)氮化硼(BN)和碳一样可以形成像石墨那样的平面六角形的层状结构,如图1所示,其中B原子的杂化方式为

(6)一定条件下,层型BN可转变为立方氮化硼,其晶胞结构如图2所示。一个晶胞中所含B原子的数目为

您最近一年使用:0次
3 . 硼及其化合物在新材料、工农业生产等方面用途、广泛。
(1)写出基态B原子的轨道表达式___________ 。
(2)已知:硼酸的电离方程式可表示为H3BO3+H2O⇌[B(OH)4]-+H+。
①根据以上信息,下列说法正确的是_________ 。(填序号)
a.硼酸是一元酸
b.硼酸在电离的过程中,B原子的杂化类型发生了变化
c.硼酸与过量NaOH反应,能观察到白色沉淀逐渐消失
②从化学键的角度表述由H3BO3,形成[B(OH)4]-的过程__________ 。
(3)B与N可以形成不同类型的晶体,如六方氮化硼、立方氮化硼等,其结构如图。
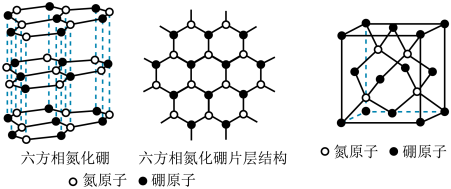
①六方氮化硼的晶体结构类似石墨,每一个B或N的杂化类型是__________ 。
②立方氮化硼因其硬度高、耐磨性好,在机械加工行业广泛用作切削工具。立方氮化硼可在高温高压的条件下由六方氮化硼转化而成。如图,立方氮化硼的晶体类型为___________ ,立方氮化硼的密度为dg⋅cm-3,阿伏加德罗常数为NA,B与N的相对原子质量分别为m和n,则立方晶胞边长a=______________ cm。

(1)写出基态B原子的轨道表达式
(2)已知:硼酸的电离方程式可表示为H3BO3+H2O⇌[B(OH)4]-+H+。
①根据以上信息,下列说法正确的是
a.硼酸是一元酸
b.硼酸在电离的过程中,B原子的杂化类型发生了变化
c.硼酸与过量NaOH反应,能观察到白色沉淀逐渐消失
②从化学键的角度表述由H3BO3,形成[B(OH)4]-的过程
(3)B与N可以形成不同类型的晶体,如六方氮化硼、立方氮化硼等,其结构如图。

①六方氮化硼的晶体结构类似石墨,每一个B或N的杂化类型是
②立方氮化硼因其硬度高、耐磨性好,在机械加工行业广泛用作切削工具。立方氮化硼可在高温高压的条件下由六方氮化硼转化而成。如图,立方氮化硼的晶体类型为
您最近一年使用:0次
4 . 钛和锆为同族的元素,它们形成的化合物用途广泛。
(1)锆为第五周期元素,基态原子的价层电子排布式为_______ 。
(2)钛与EDTA(乙二胺四乙酸根离子,结构如图1)形成的配位离子如图2所示。
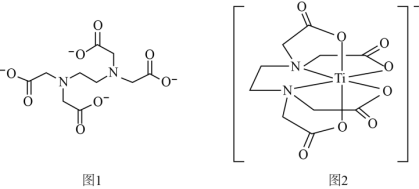
①EDTA中所含元素的电负性从大到小的顺序为_______ ;
②EDTA中键角∠NCC_______ (填“>”、“<”或“=”)∠CNC;
③钛与EDTA形成的配位离子中配位数为_______ 。
(3)常温下TiCl4为液体,ZrCl4为易升华的固体。两者熔点不同的原因是_______ 。
(4)ZrO2是制作全瓷牙的主要原料。ZrO2的晶体有立方晶相(如图3)、单斜晶相(如图4,微粒未画出,微粒分布与立方晶相相似,晶胞参数α=γ=900≠β,apm、bpm、cpm)等。
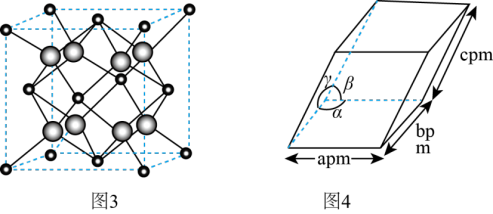
①ZrO2立方晶相中,与Zr等距离且最近的O围成的几何图形是_______ 。
②设阿伏加德罗常数的值为NA,则单斜晶相ZrO2的密度为_______ g·cm-3(列出含字母的计算表达式)。
(1)锆为第五周期元素,基态原子的价层电子排布式为
(2)钛与EDTA(乙二胺四乙酸根离子,结构如图1)形成的配位离子如图2所示。

①EDTA中所含元素的电负性从大到小的顺序为
②EDTA中键角∠NCC
③钛与EDTA形成的配位离子中配位数为
(3)常温下TiCl4为液体,ZrCl4为易升华的固体。两者熔点不同的原因是
(4)ZrO2是制作全瓷牙的主要原料。ZrO2的晶体有立方晶相(如图3)、单斜晶相(如图4,微粒未画出,微粒分布与立方晶相相似,晶胞参数α=γ=900≠β,apm、bpm、cpm)等。

①ZrO2立方晶相中,与Zr等距离且最近的O围成的几何图形是
②设阿伏加德罗常数的值为NA,则单斜晶相ZrO2的密度为
您最近一年使用:0次
名校
解题方法
5 . 铜及其化合物在科学研究和工业生产中具有许多用途,请回答下列问题:
(1)写出基态Cu原子的价电子排布式_______ 。
(2)已知高温下 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因_______ 。
(3)配合物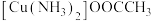 中碳原子的杂化类型是
中碳原子的杂化类型是_______ ,配体的空间构型为_______ 。配合物所含元素的电负性由大到小的顺序是_______ (用元素符号表示)。
(4)M原子的价电子排布式为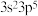 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
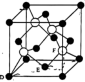
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为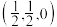 ,则F原子的坐标参数为
,则F原子的坐标参数为_______ 。
②已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为_______ pm(写出计算式)。
(1)写出基态Cu原子的价电子排布式
(2)已知高温下
 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因(3)配合物
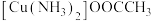 中碳原子的杂化类型是
中碳原子的杂化类型是(4)M原子的价电子排布式为
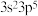 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为
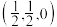 ,则F原子的坐标参数为
,则F原子的坐标参数为②已知该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为
您最近一年使用:0次
2022-10-12更新
|
459次组卷
|
4卷引用:辽宁省沈阳市皇姑屯区实验中学2022-2023学年高三上学期第一阶段检测化学试题
名校
解题方法
6 . 物质的结构决定性质,依据性质在我们日常生活中才会有形形色色的用途。
I.磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷的化合物在药物生产和农药制造等方面用途非常广泛。请回答下列有关问题:
(1)画出基态P原子的核外电子排布图_____ 。
(2)NH3比PH3易液化的原因是_____ 。
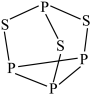
(3)P4S3可用于制造火柴,其结构如图所示。
①P4S3中硫原子的杂化轨道类型为_____ 。
②电负性:磷_____ 硫(填“>”或“<”);第一电离能磷大于硫的原因是_____ 。
(4)NH4BF4是合成氮化硼纳米管的原料之一,1molNH4BF4中含有_____ mol配位键。
Ⅱ.
(5)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为acm,则r(N3-)为_____ cm。该氮化钛的密度为_____ g·cm-3(NA为阿伏加德罗常数的值,只列计算式)。

I.磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷的化合物在药物生产和农药制造等方面用途非常广泛。请回答下列有关问题:

(1)画出基态P原子的核外电子排布图
(2)NH3比PH3易液化的原因是
(3)P4S3可用于制造火柴,其结构如图所示。
①P4S3中硫原子的杂化轨道类型为
②电负性:磷
(4)NH4BF4是合成氮化硼纳米管的原料之一,1molNH4BF4中含有
Ⅱ.
(5)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为acm,则r(N3-)为

您最近一年使用:0次
7 . 科学研究表明,物质含有许多种聚集状态,下列关于物质聚集状态的描述错误的是
| A.等离子体的用途之一是可以制造等离子体显示器 |
| B.超分子具有分子识别与自组装的特征 |
| C.液晶和液态是物质的同一种聚集状态 |
| D.同一种金属元素构成的纳米材料的某些性质具有很大的差异 |
您最近一年使用:0次
2023-06-24更新
|
105次组卷
|
3卷引用:广东省广州市第六中学2021-2022学年高二下学期期中测试化学试题
名校
解题方法
8 . 氨、磷、铁、钴等元素的化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)N2H4是一种良好的火箭发射燃料,熔点、沸点分别为1.4℃、113.5℃。N2H4中氮原子的杂化轨道类型为___ ,N2H4沸点较高的主要原因是___ 。
(2) 的一种结构如图1所示,氢原子只有一种化学环境,氨原子有两种化学环境,其中的大π键可表示为
的一种结构如图1所示,氢原子只有一种化学环境,氨原子有两种化学环境,其中的大π键可表示为___ (已知苯中的大Π键可表示为Π )。
)。

(3)磷原子在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态磷原子的核外电子排布式____ 。
(4)铁、钴与CN-、CO,NH3易形成配合物Fe(CO)5、Fe(CN) 、Co(CN)
、Co(CN) 和[Co(NH3)4]3+等。铁、钴位于周期表的
和[Co(NH3)4]3+等。铁、钴位于周期表的___ 区,CN-的电子式为___ ,N、C、O的第一电离能由大到小的顺序为___ ,已知[Co(NH3)6]3+的几何构型为正八面体形,推测[CoCl2(NH3)4]+的空间结构有___ 种。
(5)Co可以形成六方晶系的CoO(OH),晶胞结构如图2所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标.已知晶胞含对称中心,其中1号O原子的坐标为(0.6667,0.3333,0.1077),则2号O原子的坐标为____ 。设NA为阿伏加德罗常数的值,该晶体的密度为____ g/cm3(用代数式表示)。

(1)N2H4是一种良好的火箭发射燃料,熔点、沸点分别为1.4℃、113.5℃。N2H4中氮原子的杂化轨道类型为
(2)
 的一种结构如图1所示,氢原子只有一种化学环境,氨原子有两种化学环境,其中的大π键可表示为
的一种结构如图1所示,氢原子只有一种化学环境,氨原子有两种化学环境,其中的大π键可表示为 )。
)。
(3)磷原子在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态磷原子的核外电子排布式
(4)铁、钴与CN-、CO,NH3易形成配合物Fe(CO)5、Fe(CN)
 、Co(CN)
、Co(CN) 和[Co(NH3)4]3+等。铁、钴位于周期表的
和[Co(NH3)4]3+等。铁、钴位于周期表的(5)Co可以形成六方晶系的CoO(OH),晶胞结构如图2所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标.已知晶胞含对称中心,其中1号O原子的坐标为(0.6667,0.3333,0.1077),则2号O原子的坐标为

您最近一年使用:0次
2022-03-20更新
|
386次组卷
|
4卷引用:湖南省湘潭市湘乡市东山学校2022学年高三下学期期中考试化学试题
湖南省湘潭市湘乡市东山学校2022学年高三下学期期中考试化学试题重庆市2022届高三第七次质量检测化学试题(已下线)专题18 物质结构与性质(综合题)-三年(2020-2022)高考真题分项汇编湖南省常德市石门县第一中学2022届高三下学期月考化学试题
9 . 回答下列问题:
(1)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为_______ 。

(2)S和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的S与Cu的微粒个数比为_______ 。

(3)价电子排布式为3d54s2的原子,其原子结构示意图为_______ 。
(4)CuaSnbSc中Cu元素有+1和+2两种价态,从结构上分析基态Cu+、Cu2+中_______ 更稳定,原因是_______ 。
(5)GaN、GaP、GaAs熔融状态均不导电,据此判断它们是_______ (填“共价”或“离子”)化合物。它们的晶体结构与金刚石相似,其熔点如表所示,试分析GaN、GaP、GaAs熔点依次降低的原因_______ 。
(6)已知配合物的品种超过数百万种,是一个庞大的化合物家族。在配合物[Cd(NH3)4](OH)2中,中心离子是_______ ,提供孤电子对的成键原子是_______ ,配位体是_______ ,配位数是_______ 。
(7)铬、铁、镍、铜等金属及其化合物在工业上有重要用途,基态铬原子的电子排布式为_______ 。
(1)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为

(2)S和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的S与Cu的微粒个数比为

(3)价电子排布式为3d54s2的原子,其原子结构示意图为
(4)CuaSnbSc中Cu元素有+1和+2两种价态,从结构上分析基态Cu+、Cu2+中
(5)GaN、GaP、GaAs熔融状态均不导电,据此判断它们是
| 物质 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
(7)铬、铁、镍、铜等金属及其化合物在工业上有重要用途,基态铬原子的电子排布式为
您最近一年使用:0次
名校
解题方法
10 . 铜及其化合物在人们的日常生活中有着广泛的用途,回答下列问题:
(1)基态铜原子的价电子排布式为___________ 。
(2)在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下: 2CuCl+2CO+2H2O= Cu2Cl2·2CO·2H2O,Cu2Cl2·2CO·2H2O是一种配合物。其结构简式如图1所示。

①H2O中氧原子的杂化轨道类型为___________ 。
②该配合物中,CO作配体时配位原子是C而不是O的原因是___________ 。
(3)氧化亚铜的化学式为Cu2O,为一价铜的氧化物,为鲜红色粉末状固体,常用于催化有机物的合成,其立方晶胞如图2所示:

①晶胞中白球Z表示___________ 原子(填名称)
②与O距离相等且最近的O能构成___________ ( 填空间构型)
③体心Z原子的坐标为( ,
, ,
, )。 则P与M两个位置的R原子的坐标分别是
)。 则P与M两个位置的R原子的坐标分别是_____ 、______ 。
(1)基态铜原子的价电子排布式为
(2)在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下: 2CuCl+2CO+2H2O= Cu2Cl2·2CO·2H2O,Cu2Cl2·2CO·2H2O是一种配合物。其结构简式如图1所示。

①H2O中氧原子的杂化轨道类型为
②该配合物中,CO作配体时配位原子是C而不是O的原因是
(3)氧化亚铜的化学式为Cu2O,为一价铜的氧化物,为鲜红色粉末状固体,常用于催化有机物的合成,其立方晶胞如图2所示:

①晶胞中白球Z表示
②与O距离相等且最近的O能构成
③体心Z原子的坐标为(
 ,
, ,
, )。 则P与M两个位置的R原子的坐标分别是
)。 则P与M两个位置的R原子的坐标分别是
您最近一年使用:0次



