解题方法
1 . SnO2是锡的重要氧化物,现以锡锑渣(主要含塑料及SnO2、Sb4O6、PbO2)为原料,提纯SnO2的工艺流程图如下:
②Na2SnO3可溶于水,难溶于乙醇。
请回答下列问题:
(1)“焙烧”的主要目的是_______ 。
(2)“沉铅”时同时生成S沉淀的化学方程式_______ 。
(3)“还原”时Na3SbO4发生的离子方程式为_______ 。
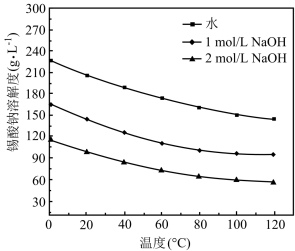
(4)在不同溶剂中Na2SnO3的溶解度随温度变化如图。_______ 。
②由Na2SnO3溶液可获得Na2SnO3晶体,具体操作方法为_______ 、用_______ 洗涤、干燥。
(5)下列冶炼方法与本工艺流程中加入焦炭冶炼锡的方法相似的是_______。
(6)将10kg锡锑渣进行碱浸,“还原”时消耗0. 13kg锡粒,假设其余各步损失不计,干燥后称量锡酸钠质量为4. 0kg,滴定测得锡酸钠中锡的质量分数为53. 5%。锡锑渣中锡元素的质量分数为_______ 。

②Na2SnO3可溶于水,难溶于乙醇。
请回答下列问题:
(1)“焙烧”的主要目的是
(2)“沉铅”时同时生成S沉淀的化学方程式
(3)“还原”时Na3SbO4发生的离子方程式为
(4)在不同溶剂中Na2SnO3的溶解度随温度变化如图。
②由Na2SnO3溶液可获得Na2SnO3晶体,具体操作方法为
(5)下列冶炼方法与本工艺流程中加入焦炭冶炼锡的方法相似的是_______。
| A.工业制粗硅 | B.电解熔融氯化钠制钠 |
| C.氧化汞分解制汞 | D.工业炼铁 |
(6)将10kg锡锑渣进行碱浸,“还原”时消耗0. 13kg锡粒,假设其余各步损失不计,干燥后称量锡酸钠质量为4. 0kg,滴定测得锡酸钠中锡的质量分数为53. 5%。锡锑渣中锡元素的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 肉桂酸广泛应用于香精香料、食品添加剂、医药工业、美容和有机合成等方面。其合成原理及实验室制备方法如下:
i.在50mL仪器a中加入5mL苯甲醛、14mL乙酸酐和12g无水碳酸钾粉末(过量),加热回流45min。
ii.向反应混合物中加入40mL蒸馏水浸泡几分钟,进行水蒸气蒸馏。
iii.将烧瓶冷却后,加入10g碳酸钠,再加入70mL水,加热煮沸,趁热过滤。
iV.待滤液冷却至室温后,在搅拌下小心加入40mL 盐酸,使溶液呈酸性。
盐酸,使溶液呈酸性。
V.冷却结晶,抽滤,用少量试剂b洗涤,80℃烘干,得粗产品4.5g。
回答下列问题:
(1)仪器使用前必须干燥,原因是___________ 。
(2)加热回流装置中仪器a的名称是___________ ,不使用水冷冷凝管而用空气冷凝管是为了___________ 。
(3)整个实验过程中温度不宜超过180℃,原因是___________ 。
(4)水蒸气蒸馏装置中止水夹的主要作用是___________ 。
(5)步骤V中试剂b是___________ 。
(6)本实验肉桂酸的产率最接近___________ (填标号)。若产物不纯,则提纯产物的方法为___________ 。
A.50% B.60% C.70% D.80%
主反应:
温度较高时发生副反应: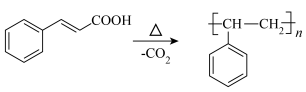
i.在50mL仪器a中加入5mL苯甲醛、14mL乙酸酐和12g无水碳酸钾粉末(过量),加热回流45min。
ii.向反应混合物中加入40mL蒸馏水浸泡几分钟,进行水蒸气蒸馏。
iii.将烧瓶冷却后,加入10g碳酸钠,再加入70mL水,加热煮沸,趁热过滤。
iV.待滤液冷却至室温后,在搅拌下小心加入40mL
 盐酸,使溶液呈酸性。
盐酸,使溶液呈酸性。V.冷却结晶,抽滤,用少量试剂b洗涤,80℃烘干,得粗产品4.5g。

| 名称 | 相对分子质量 | 密度/ | 熔点/℃ | 沸点/℃ | 溶解度:g/100mL | ||
| 水 | 醇 | 醚 | |||||
| 苯甲醛 | 106 | 1.04 | -26 | 178~179 | 0.3 | 互溶 | 互溶 |
| 乙酸酐 | 102 | 1.08 | -79 | 138~140 | 遇水生成乙酸 | 溶 | 不溶 |
| 肉桂 | 148 | 1.24 | 133~134 | 300 | 0.04 | 24 | 溶 |
(1)仪器使用前必须干燥,原因是
(2)加热回流装置中仪器a的名称是
(3)整个实验过程中温度不宜超过180℃,原因是
(4)水蒸气蒸馏装置中止水夹的主要作用是
(5)步骤V中试剂b是
(6)本实验肉桂酸的产率最接近
A.50% B.60% C.70% D.80%
您最近一年使用:0次
名校
3 . 钯(Pd)见一种银白色过渡金属,质软、有良好的延展性和可塑性,可锻造、压延和拉丝。块状金属钯能吸收大量氢气,使体积显著胀大、变脆乃至破裂成碎片。一种从废钯催化剂(杂质主要含有机物、活性炭及少量Fe、Cu、Al等元素)中回收钯和催化剂FeOCl的工艺流程如图所示:
②离子交换树脂的基本工作原理分别为 (
(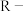 表示树脂的有机成分);
表示树脂的有机成分);
③常温下,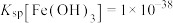 ,
,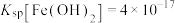 ,
,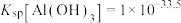 ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;
④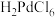 是一种二元强酸,
是一种二元强酸,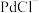 在溶液中存在配位平衡:
在溶液中存在配位平衡: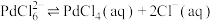
 ;
;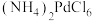 在水中溶解度小。
在水中溶解度小。
回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧的目的是___________ ,再通入甲酸继续焙烧的目的是___________ 。
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为___________ 。
(3)“洗脱”时,加入最佳“试剂Y”的名称是___________ ,“洗脱液”中要加入过量 的目的是
的目的是___________ 。
(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为___________ 。“调pH”步骤中,若铁元素和铝元素浓度均为 ,则调pH的范围为
,则调pH的范围为___________  。
。

②离子交换树脂的基本工作原理分别为
 (
(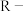 表示树脂的有机成分);
表示树脂的有机成分);③常温下,
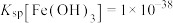 ,
,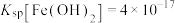 ,
,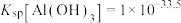 ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;④
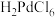 是一种二元强酸,
是一种二元强酸,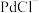 在溶液中存在配位平衡:
在溶液中存在配位平衡: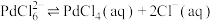
 ;
;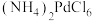 在水中溶解度小。
在水中溶解度小。回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧的目的是
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为
(3)“洗脱”时,加入最佳“试剂Y”的名称是
 的目的是
的目的是(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为
 ,则调pH的范围为
,则调pH的范围为 。
。
您最近一年使用:0次
4 . 从钒铬锰矿渣(主要成分为V2O5、Cr2O3、MnO)中提铬的一种工艺流程如下:
下列说法错误的是

下列说法错误的是
| A.Cr元素位于元素周期表第四周期 VIB 族 |
| B.“沉钒”过程利用了 Fe(OH)3(胶体)的吸附性,使含钒微粒与胶体共沉降 |
| C.“转化”过程中生成MnO2的离子方程式为Mn2++H2O2+2OH-=MnO2+2H2O |
| D.“提纯”过程中Na2S2O3的作用是还原含铬元素的物质 |
您最近一年使用:0次
5 .  俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备
俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备 并测定摩尔盐中
并测定摩尔盐中 的含量。已知:
的含量。已知:
三种盐的溶解度(单位为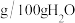 )
)
回答下列问题:
(1)制备硫酸亚铁(装置如图所示):称取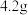 洗净的铁粉(含
洗净的铁粉(含 质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入
质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入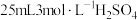 溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入
溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入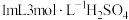 溶液,趁热过滤得
溶液,趁热过滤得 溶液。
溶液。______________________ ;装置b中所盛试剂的作用是______________________ 。
②若不及时向锥形瓶中补加水,导致硫酸浓度过大,可能造成的不良后果为______________________ 。
(2)在 的条件下,称取
的条件下,称取 晶体
晶体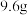 ,将其溶于
,将其溶于___________________  (结果保留一位小数,此温度下的水的密度近似为
(结果保留一位小数,此温度下的水的密度近似为 )水中,配成饱和溶液。
)水中,配成饱和溶液。
(3)将(2)中所配的 饱和溶液加入(1)所得
饱和溶液加入(1)所得 溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到
溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到 晶体,抽滤、洗涤得产品.洗涤的具体操作为
晶体,抽滤、洗涤得产品.洗涤的具体操作为_____________ 。
(4)测定产品中 的含量:称取
的含量:称取 产品,溶于水配成溶液并加入稀硫酸,用
产品,溶于水配成溶液并加入稀硫酸,用 的
的 标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗
标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗 标准溶液的体积为
标准溶液的体积为 。
。
①滴定反应的离子方程式为___________________ 。
②产品中 的质量分数为
的质量分数为____________________ 。
③若滴定终点时俯视读数,会使测定结果_____________ (填“偏低”或“偏高”)。
 俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备
俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备 并测定摩尔盐中
并测定摩尔盐中 的含量。已知:
的含量。已知:三种盐的溶解度(单位为
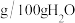 )
)温度/℃ |
|
|
|
10 | 20.0 | 73 | 17.2 |
20 | 26.5 | 75.4 | 21.6 |
30 | 32.9 | 78 | 28.1 |
(1)制备硫酸亚铁(装置如图所示):称取
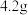 洗净的铁粉(含
洗净的铁粉(含 质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入
质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入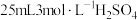 溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入
溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入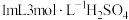 溶液,趁热过滤得
溶液,趁热过滤得 溶液。
溶液。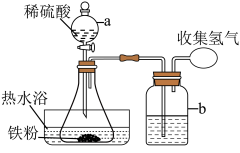
②若不及时向锥形瓶中补加水,导致硫酸浓度过大,可能造成的不良后果为
(2)在
 的条件下,称取
的条件下,称取 晶体
晶体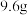 ,将其溶于
,将其溶于 (结果保留一位小数,此温度下的水的密度近似为
(结果保留一位小数,此温度下的水的密度近似为 )水中,配成饱和溶液。
)水中,配成饱和溶液。(3)将(2)中所配的
 饱和溶液加入(1)所得
饱和溶液加入(1)所得 溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到
溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到 晶体,抽滤、洗涤得产品.洗涤的具体操作为
晶体,抽滤、洗涤得产品.洗涤的具体操作为(4)测定产品中
 的含量:称取
的含量:称取 产品,溶于水配成溶液并加入稀硫酸,用
产品,溶于水配成溶液并加入稀硫酸,用 的
的 标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗
标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗 标准溶液的体积为
标准溶液的体积为 。
。①滴定反应的离子方程式为
②产品中
 的质量分数为
的质量分数为③若滴定终点时俯视读数,会使测定结果
您最近一年使用:0次
6 . 硅酸盐锆矿的主要成分为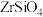 ,还含有
,还含有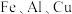 的氧化物,以该矿石为原料生产
的氧化物,以该矿石为原料生产 的工艺流程如图所示:
的工艺流程如图所示: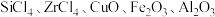 。
。
回答下列问题:
(1)“加热转化”时 发生反应的化学方程式为
发生反应的化学方程式为__________________ 。
(2) 易水解可生成硅酸,
易水解可生成硅酸, 溶于水,试剂X为
溶于水,试剂X为_____________ 。
(3)常温下, ,测得“除铜”后溶液中
,测得“除铜”后溶液中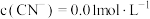 ,通过计算判断溶液中
,通过计算判断溶液中 是否除尽:
是否除尽:__________________ (写出计算过程,溶液中离子浓度低于 即可认为该离子已被除尽)。
即可认为该离子已被除尽)。
(4) 难溶于有机溶剂;
难溶于有机溶剂;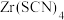 易溶于有机溶剂
易溶于有机溶剂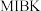 (密度小于水),微溶于水。若可选试剂为
(密度小于水),微溶于水。若可选试剂为 和有机溶剂
和有机溶剂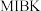 ,则从除铜后的溶液中“除铁”的具体操作为
,则从除铜后的溶液中“除铁”的具体操作为_______________ ,再用硫酸将含有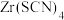 的有机层反萃取,得到含
的有机层反萃取,得到含 的溶液进入下一步流程(补全操作)。
的溶液进入下一步流程(补全操作)。
(5)常温下, ,“沉锆”后
,“沉锆”后 的溶液中,
的溶液中,
__________ 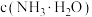 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
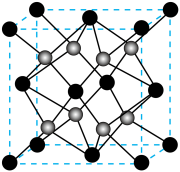
(6) 的立方晶胞结构如图所示,
的立方晶胞结构如图所示, 是阿伏加德罗常数的值,晶胞参数为
是阿伏加德罗常数的值,晶胞参数为 。
。__________________ 。
②与O配位的 围成的立体结构为
围成的立体结构为__________________ 。
③该晶体密度为_____________  (用含a、
(用含a、 的代数式表示,不用化简)。
的代数式表示,不用化简)。
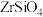 ,还含有
,还含有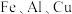 的氧化物,以该矿石为原料生产
的氧化物,以该矿石为原料生产 的工艺流程如图所示:
的工艺流程如图所示: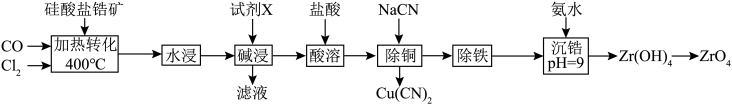
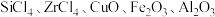 。
。回答下列问题:
(1)“加热转化”时
 发生反应的化学方程式为
发生反应的化学方程式为(2)
 易水解可生成硅酸,
易水解可生成硅酸, 溶于水,试剂X为
溶于水,试剂X为(3)常温下,
 ,测得“除铜”后溶液中
,测得“除铜”后溶液中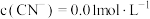 ,通过计算判断溶液中
,通过计算判断溶液中 是否除尽:
是否除尽: 即可认为该离子已被除尽)。
即可认为该离子已被除尽)。(4)
 难溶于有机溶剂;
难溶于有机溶剂;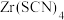 易溶于有机溶剂
易溶于有机溶剂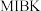 (密度小于水),微溶于水。若可选试剂为
(密度小于水),微溶于水。若可选试剂为 和有机溶剂
和有机溶剂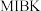 ,则从除铜后的溶液中“除铁”的具体操作为
,则从除铜后的溶液中“除铁”的具体操作为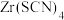 的有机层反萃取,得到含
的有机层反萃取,得到含 的溶液进入下一步流程(补全操作)。
的溶液进入下一步流程(补全操作)。(5)常温下,
 ,“沉锆”后
,“沉锆”后 的溶液中,
的溶液中,
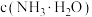 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(6)
 的立方晶胞结构如图所示,
的立方晶胞结构如图所示, 是阿伏加德罗常数的值,晶胞参数为
是阿伏加德罗常数的值,晶胞参数为 。
。
②与O配位的
 围成的立体结构为
围成的立体结构为③该晶体密度为
 (用含a、
(用含a、 的代数式表示,不用化简)。
的代数式表示,不用化简)。
您最近一年使用:0次
7 . 钪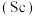 是一种稀土金属元素,在国防、航天,核能等领域具有重要应用。氯化钪
是一种稀土金属元素,在国防、航天,核能等领域具有重要应用。氯化钪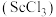 是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有
是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有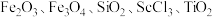 等)中回收
等)中回收 的工艺流程如下:
的工艺流程如下: 难溶于盐酸。
难溶于盐酸。
②常温下,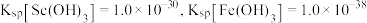 。
。
回答下列问题:
(1)某次实验中需要使用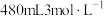 的盐酸,用浓盐酸(密度为
的盐酸,用浓盐酸(密度为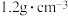 ,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为
,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为___________  。
。
(2)滤渣1的主要成分是______________ (填化学式)。“酸浸”时温度过高,酸浸速率反而减慢,其原因是__________ 。
(3)常温下,“调 ”时,溶液中
”时,溶液中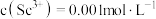 ,为除去杂质离子,应控制的
,为除去杂质离子,应控制的 范围是
范围是___________ (当溶液中某离子浓度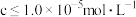 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(4)“氧化”时反应的离子方程式为________________ 。
(5)实验室模拟流程中“灼烧”得到 ,用来盛放被灼烧物的仪器为
,用来盛放被灼烧物的仪器为___________ ,“加热氯化”步骤中所加入焦炭过量,写出由 制备三氯化钪反应的化学方程式:
制备三氯化钪反应的化学方程式:________________ 。
(6) 的一种氢化物的晶胞结构如图所示,已知晶胞的边长为
的一种氢化物的晶胞结构如图所示,已知晶胞的边长为 。
。_______________ 。
②设 表示阿伏加德罗常数的值,则钪晶体的密度为
表示阿伏加德罗常数的值,则钪晶体的密度为___________  。
。
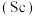 是一种稀土金属元素,在国防、航天,核能等领域具有重要应用。氯化钪
是一种稀土金属元素,在国防、航天,核能等领域具有重要应用。氯化钪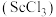 是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有
是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有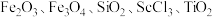 等)中回收
等)中回收 的工艺流程如下:
的工艺流程如下: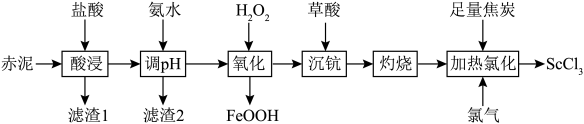
 难溶于盐酸。
难溶于盐酸。②常温下,
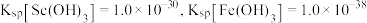 。
。回答下列问题:
(1)某次实验中需要使用
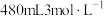 的盐酸,用浓盐酸(密度为
的盐酸,用浓盐酸(密度为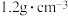 ,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为
,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为 。
。(2)滤渣1的主要成分是
(3)常温下,“调
 ”时,溶液中
”时,溶液中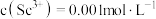 ,为除去杂质离子,应控制的
,为除去杂质离子,应控制的 范围是
范围是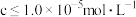 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。(4)“氧化”时反应的离子方程式为
(5)实验室模拟流程中“灼烧”得到
 ,用来盛放被灼烧物的仪器为
,用来盛放被灼烧物的仪器为 制备三氯化钪反应的化学方程式:
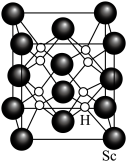
制备三氯化钪反应的化学方程式:(6)
 的一种氢化物的晶胞结构如图所示,已知晶胞的边长为
的一种氢化物的晶胞结构如图所示,已知晶胞的边长为 。
。
②设
 表示阿伏加德罗常数的值,则钪晶体的密度为
表示阿伏加德罗常数的值,则钪晶体的密度为 。
。
您最近一年使用:0次
7日内更新
|
24次组卷
|
2卷引用:黑龙江省部分学校2024届高三下学期第三次模拟化学试题
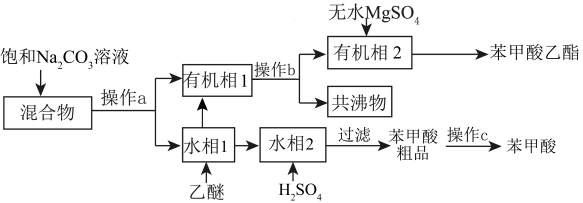
8 . 实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下: ,“乙醚—环己烷—水共沸物”的沸点为
,“乙醚—环己烷—水共沸物”的沸点为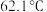 。
。
下列说法错误的是
 ,“乙醚—环己烷—水共沸物”的沸点为
,“乙醚—环己烷—水共沸物”的沸点为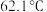 。
。下列说法错误的是
| A.操作a为分液 |
| B.操作b中需用到直形冷凝管 |
C.无水 的作用是干燥有机相2 的作用是干燥有机相2 |
| D.“洗涤”苯甲酸,用乙醇的效果比用蒸馏水好 |
您最近一年使用:0次
7日内更新
|
70次组卷
|
2卷引用:黑龙江省部分学校2024届高三下学期第三次模拟化学试题
名校
9 . 实验室中初步分离环己醇、苯酚、苯甲酸混合液的流程如下。下列说法错误的是
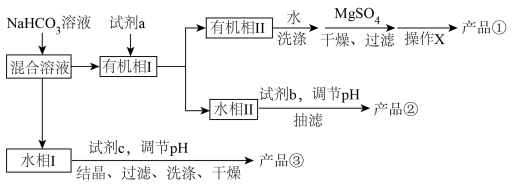
| A.环己醇、苯酚、苯甲酸粗产品依次由①、②、③获得 |
| B.若试剂a为碳酸钠,可以通过观察气泡现象控制试剂用量 |
C.“操作X”为蒸馏,“试剂b”可选用盐酸或 |
| D.试剂c可以选用盐酸或硫酸 |
您最近一年使用:0次
7日内更新
|
493次组卷
|
3卷引用:黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期阶段考试(八)化学试题
名校
解题方法
10 . 某矿石主要成分为 ,含有
,含有 、
、 等杂质。以该矿石为原料制备
等杂质。以该矿石为原料制备 的工艺流程如下图所示:
的工艺流程如下图所示:
 ,含有
,含有 、
、 等杂质。以该矿石为原料制备
等杂质。以该矿石为原料制备 的工艺流程如下图所示:
的工艺流程如下图所示:
| A.在实验室模拟进行“焙烧”可以选用石英坩埚 |
B.滤渣1只含有 |
C.物质Y可选用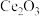 ,也可选用氨水 ,也可选用氨水 |
D.“沉铈”时消耗的 与 与 物质的量之比为2∶3 物质的量之比为2∶3 |
您最近一年使用:0次
7日内更新
|
263次组卷
|
2卷引用:黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期阶段考试(八)化学试题



