1 . 钴基变形高温合金是指含钴40%~70%的铸造合金,具有较好的抗氧化和抗热腐蚀性。制备某钴基变形高温合金的废料中主要含有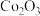 ,还含有少量
,还含有少量 、
、 及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收
及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收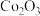 的工业流程如图所示。
的工业流程如图所示。 、
、 、
、 、
、 、
、 、
、 等。
等。
②部分阳离子以氢氧化物形式开始沉淀和沉淀完全(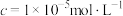 )时的pH见下表。
)时的pH见下表。
(1)“溶浸”前,通常需要将合金废料粉碎,这样做的目的是___________ 。“溶浸”时加入 的作用是
的作用是___________ 。
(2)“滤液1”中加入 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。得到“滤渣2”时需要加 溶液调节溶液的
溶液调节溶液的 范围是
范围是___________ 。
(3)已知:25℃时, 、
、 。向“滤液2”中加入
。向“滤液2”中加入 溶液的目的是将溶液中的
溶液的目的是将溶液中的 与
与 转化为氮化物沉淀。如果“滤液2”中的
转化为氮化物沉淀。如果“滤液2”中的 ,则开始滴加
,则开始滴加 溶液时,首先析出的沉淀是
溶液时,首先析出的沉淀是___________ (填化学式),已知当加入过量 溶液后,所得滤液中
溶液后,所得滤液中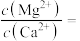
___________ 。
(4) 在空气中充分煅烧,除得到产品外,还生成了
在空气中充分煅烧,除得到产品外,还生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(5)若将草酸铵溶液换为碳酸氢钠溶液,可将 转化为
转化为 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为___________ 。
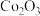 ,还含有少量
,还含有少量 、
、 及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收
及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收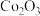 的工业流程如图所示。
的工业流程如图所示。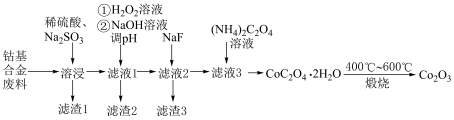
 、
、 、
、 、
、 、
、 、
、 等。
等。②部分阳离子以氢氧化物形式开始沉淀和沉淀完全(
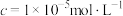 )时的pH见下表。
)时的pH见下表。| 沉淀物 |  |  |  |  |  |
| 开始沉淀时的pH | 6.6 | 7.6 | 2.7 | 3.4 | 9.2 |
| 沉淀完全时的pH | 9.2 | 9.6 | 3.2 | 4.7 | 11.1 |
(1)“溶浸”前,通常需要将合金废料粉碎,这样做的目的是
 的作用是
的作用是(2)“滤液1”中加入
 溶液的作用是
溶液的作用是 溶液调节溶液的
溶液调节溶液的 范围是
范围是(3)已知:25℃时,
 、
、 。向“滤液2”中加入
。向“滤液2”中加入 溶液的目的是将溶液中的
溶液的目的是将溶液中的 与
与 转化为氮化物沉淀。如果“滤液2”中的
转化为氮化物沉淀。如果“滤液2”中的 ,则开始滴加
,则开始滴加 溶液时,首先析出的沉淀是
溶液时,首先析出的沉淀是 溶液后,所得滤液中
溶液后,所得滤液中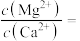
(4)
 在空气中充分煅烧,除得到产品外,还生成了
在空气中充分煅烧,除得到产品外,还生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(5)若将草酸铵溶液换为碳酸氢钠溶液,可将
 转化为
转化为 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 铍是航天航空、火箭导弹和原子能工业不可替代的材料,有“超级金属”之称。某厂以硅铍石(主要含有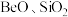 ,还有少量
,还有少量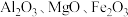 )为原料提取铍,具体流程如图。
)为原料提取铍,具体流程如图。 为两性氢氧化物,在强碱溶液中以
为两性氢氧化物,在强碱溶液中以 的形式存在;
的形式存在;
②氯化铍在熔融态时较难电离;
③ 为离子化合物,熔点为
为离子化合物,熔点为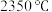 ,等物质的量的
,等物质的量的 和
和 的固体混合物在
的固体混合物在 即可熔化;
即可熔化;
④不同金属离子在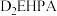 中的溶解性如表所示:
中的溶解性如表所示:
(1)“滤渣”的主要成分为_______ (填化学式)。
(2)“萃取分液”除去的离子主要是_______ 。若铍的萃取按如下反应式进行: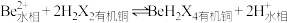 ,则“反萃取”时要加入足量
,则“反萃取”时要加入足量 溶液,发生的主要反应的化学方程式为
溶液,发生的主要反应的化学方程式为_______ 。
(3)“煮沸”时,发生反应的离子方程式为_______ 。
(4)写出高温条件下“转化”的化学方程式:_______ 。
(5)“电解”制铍时,加入与 等物质的量的
等物质的量的 的作用是
的作用是_______ ,不用电解 的方法制金属铍的原因是
的方法制金属铍的原因是_______ 。
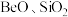 ,还有少量
,还有少量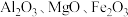 )为原料提取铍,具体流程如图。
)为原料提取铍,具体流程如图。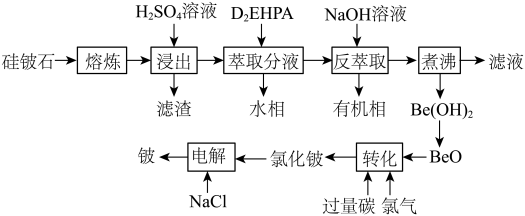
 为两性氢氧化物,在强碱溶液中以
为两性氢氧化物,在强碱溶液中以 的形式存在;
的形式存在;②氯化铍在熔融态时较难电离;
③
 为离子化合物,熔点为
为离子化合物,熔点为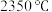 ,等物质的量的
,等物质的量的 和
和 的固体混合物在
的固体混合物在 即可熔化;
即可熔化;④不同金属离子在
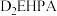 中的溶解性如表所示:
中的溶解性如表所示:金属离子 |
|
|
|
|
| 易溶 | 难溶 | 微溶 | 微溶 |
(1)“滤渣”的主要成分为
(2)“萃取分液”除去的离子主要是
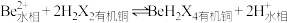 ,则“反萃取”时要加入足量
,则“反萃取”时要加入足量 溶液,发生的主要反应的化学方程式为
溶液,发生的主要反应的化学方程式为(3)“煮沸”时,发生反应的离子方程式为
(4)写出高温条件下“转化”的化学方程式:
(5)“电解”制铍时,加入与
 等物质的量的
等物质的量的 的作用是
的作用是 的方法制金属铍的原因是
的方法制金属铍的原因是
您最近一年使用:0次
解题方法
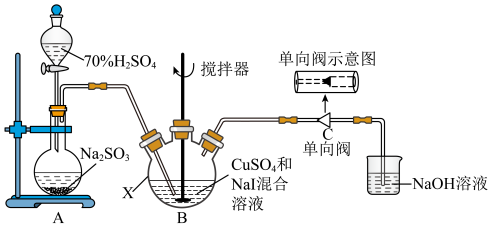
3 . 碘化亚铜(CuI)可用作有机合成催化剂,是一种白色粉末,不溶于水,在空气中相对稳定。实验室制备碘化亚铜的装置如图(部分夹持及加热装置已略去):
I.取50.0g 、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
Ⅱ.打开分液漏斗,将A中产生的 通向B中的黄色沉淀,充分反应后得到白色沉淀;
通向B中的黄色沉淀,充分反应后得到白色沉淀;
Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前,必需进行的操作是___________ 。仪器X的名称是___________ 。
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为___________ 。
(3)步骤Ⅱ通入 的主要目的是
的主要目的是___________ 。写出通入 所发生的离子反应方程式
所发生的离子反应方程式___________ 。
(4)下图中能起到与单向阀C相同作用的是___________ (填字母)。(下图容器中未标注的液体均为氢氧化钠溶液) 浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为___________ %,据此推算CuI的产率接近于___________ (填字母)。
I.取50.0g
 、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;Ⅱ.打开分液漏斗,将A中产生的
 通向B中的黄色沉淀,充分反应后得到白色沉淀;
通向B中的黄色沉淀,充分反应后得到白色沉淀;Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前,必需进行的操作是
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为
(3)步骤Ⅱ通入
 的主要目的是
的主要目的是 所发生的离子反应方程式
所发生的离子反应方程式(4)下图中能起到与单向阀C相同作用的是

 浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
您最近一年使用:0次
名校
解题方法
4 . 四氯化碳( )主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
)主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
① 与溴水反应生成硫酸和氢溴酸等,可用溴水吸收
与溴水反应生成硫酸和氢溴酸等,可用溴水吸收 ;
;
② 与
与 在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
③硫单质的沸点445℃, 的沸点46.5℃,
的沸点46.5℃, 沸点76.8℃、密度1.6
沸点76.8℃、密度1.6 。
。
回答下列问题:
(1)装置A中仪器a的名称是___________ ,用浓盐酸与 反应制取
反应制取 ,发生反应的离子方程式为
,发生反应的离子方程式为____________ (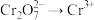 )。
)。
(2)装置的连接顺序为___________ 。
A→_______→________→_______→_____→E。
(3)为使冷凝效果较好,应选用的冷凝管为_______ (填编号);装置C中冷凝管的作用是____________ ,冷水从_________ 口通入。 、
、 ,此时装置F的作用为
,此时装置F的作用为_________________ 。
(5)反应一段时间后,装置C中出现淡黄色固体,写出装置C中发生反应的化学方程式:_________ 。
(6)装置C中反应结束后,先过滤除去固体_________ (填名称),再经过_________ (填操作名称)可得到 。
。
 )主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
)主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。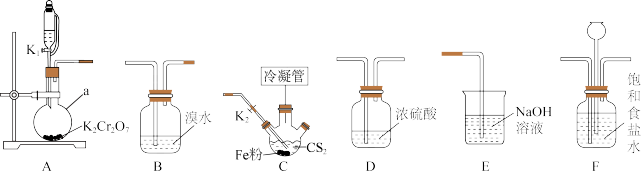
①
 与溴水反应生成硫酸和氢溴酸等,可用溴水吸收
与溴水反应生成硫酸和氢溴酸等,可用溴水吸收 ;
;②
 与
与 在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;③硫单质的沸点445℃,
 的沸点46.5℃,
的沸点46.5℃, 沸点76.8℃、密度1.6
沸点76.8℃、密度1.6 。
。回答下列问题:
(1)装置A中仪器a的名称是
 反应制取
反应制取 ,发生反应的离子方程式为
,发生反应的离子方程式为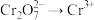 )。
)。(2)装置的连接顺序为
A→_______→________→_______→_____→E。
(3)为使冷凝效果较好,应选用的冷凝管为

 、
、 ,此时装置F的作用为
,此时装置F的作用为(5)反应一段时间后,装置C中出现淡黄色固体,写出装置C中发生反应的化学方程式:
(6)装置C中反应结束后,先过滤除去固体
 。
。
您最近一年使用:0次
7日内更新
|
48次组卷
|
2卷引用:2024届陕西省铜川市王益中学高三下学期模拟预测理综试题-高中化学
解题方法
5 . BeO广泛用于电子、半导体和光学领域。工业上以绿柱石(主要成分为 ,还含有少量铁元素)和方解石(主要成分为
,还含有少量铁元素)和方解石(主要成分为 )为原料制备BeO的流程如图所示:
)为原料制备BeO的流程如图所示: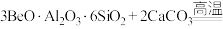
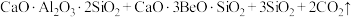 ;
;
②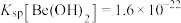 。
。
(1)“滤渣1”的主要成分为___________ (填化学式)。
(2)被浸物料和浸出试剂的流动方向相同时称为“顺流浸出”,相反则为“逆流浸出”,该流程采用“逆流浸出”的优点是___________ 。
(3)“结晶”过程中,铝会以铝铵矾[ ]的形式析出,写出该反应的离子方程式:
]的形式析出,写出该反应的离子方程式:___________ 。
(4)“转化”时加入 的作用是
的作用是___________ 。
(5)“调pH”除铁,利用平衡移动原理解释“调pH”过程中加入 可得到“滤渣2”的原因:
可得到“滤渣2”的原因:___________ 。
(6)“滤液”的主要成分为___________ (填化学式),可以返回___________ 工序循环使用。
(7)常温下,“沉淀”过程中加入 调节pH=5,溶液中的铍离子是否沉淀完全
调节pH=5,溶液中的铍离子是否沉淀完全___________ [列式计算,溶液中c(Mn+)≤1×10-5mol/L时,可认为该离子沉淀完全]。
 ,还含有少量铁元素)和方解石(主要成分为
,还含有少量铁元素)和方解石(主要成分为 )为原料制备BeO的流程如图所示:
)为原料制备BeO的流程如图所示:
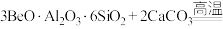
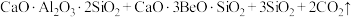 ;
;②
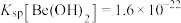 。
。(1)“滤渣1”的主要成分为
(2)被浸物料和浸出试剂的流动方向相同时称为“顺流浸出”,相反则为“逆流浸出”,该流程采用“逆流浸出”的优点是
(3)“结晶”过程中,铝会以铝铵矾[
 ]的形式析出,写出该反应的离子方程式:
]的形式析出,写出该反应的离子方程式:(4)“转化”时加入
 的作用是
的作用是(5)“调pH”除铁,利用平衡移动原理解释“调pH”过程中加入
 可得到“滤渣2”的原因:
可得到“滤渣2”的原因:(6)“滤液”的主要成分为
(7)常温下,“沉淀”过程中加入
 调节pH=5,溶液中的铍离子是否沉淀完全
调节pH=5,溶液中的铍离子是否沉淀完全
您最近一年使用:0次
解题方法
6 . 检验新鲜芹菜中铁元素的实验操作有:(1)剪碎芹菜,研磨;(2)加入蒸馏水,搅拌,过滤;(3)取少量滤液,滴加稀 ;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
 ;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
| A.②⑤⑥⑦⑧⑨ | B.③⑥⑦⑧⑨⑩ |
| C.①②③⑥⑨⑩ | D.①④⑤⑥⑦⑧ |
您最近一年使用:0次
解题方法
7 . 高砷烟尘(主要成分有 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下: 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;
② 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;
③ 。
。
回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为________ ,滤渣的主要成分为________ (填化学式)。 ,发生反应的离子方程式为
,发生反应的离子方程式为________ 。已知 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
________ 。
(3)“还原”后溶液酸性增强,主要原因是________ (用离子方程式表示)。
(4)“结晶”操作为________ 、过滤、洗涤、干燥。
(5)“萃余液”中含有的金属阳离子为________ (填离子符号),将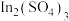 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为________ 。
 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下:
 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;②
 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;③
 。
。回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为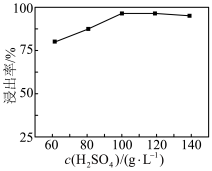
 ,发生反应的离子方程式为
,发生反应的离子方程式为 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
(3)“还原”后溶液酸性增强,主要原因是
(4)“结晶”操作为
(5)“萃余液”中含有的金属阳离子为
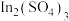 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为
您最近一年使用:0次
2024-06-01更新
|
74次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
解题方法
8 . 下列仪器在相应实验中选用合理的是

| A.蒸馏海水:①②③⑤ |
| B.实验室分离碘单质和氯化钠的混合物:③⑦ |
C.用碳酸钠和稀硫酸制备 :⑥ :⑥ |
D.用酸性高锰酸钾标准溶液测定溶液中 含量:④⑤ 含量:④⑤ |
您最近一年使用:0次
2024-06-01更新
|
35次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
解题方法
9 .  -呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下:
-呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下: -呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。
-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。___________ 。
(2)与酒精灯加热相比,使用油浴加热的优点是___________ 。
(3)三颈烧瓶中反应已完成的标志是___________ 。
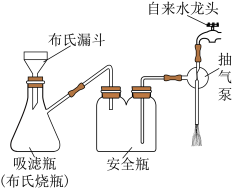
(4)分离出晶体时需减压抽滤,装置如图所示,抽滤的优点是___________ 。
称取mg -呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为
-呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为 的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。
的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为___________ 。
②产品的纯度是___________ (以质量分数表示)。
③下列操作会使测定结果偏大的是___________ (填标号)。
A.称量样品时,将样品放在托盘天平的右盘
B.加热回流阶段,油浴时没有搅拌,出现焦化现象
C.滴定过程中,读数时,滴定前仰视,滴定后俯视
D.滴定前,尖嘴管有气泡,滴定后无气泡
 -呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下:
-呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下: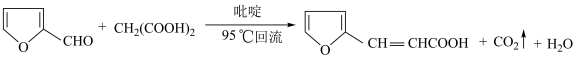
 -呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。
-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。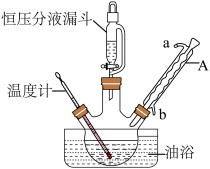
(2)与酒精灯加热相比,使用油浴加热的优点是
(3)三颈烧瓶中反应已完成的标志是
(4)分离出晶体时需减压抽滤,装置如图所示,抽滤的优点是
称取mg
 -呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为
-呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为 的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。
的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为
②产品的纯度是
③下列操作会使测定结果偏大的是
A.称量样品时,将样品放在托盘天平的右盘
B.加热回流阶段,油浴时没有搅拌,出现焦化现象
C.滴定过程中,读数时,滴定前仰视,滴定后俯视
D.滴定前,尖嘴管有气泡,滴定后无气泡
您最近一年使用:0次
2024-06-01更新
|
140次组卷
|
3卷引用:2024届陕西省商洛市高三下学期第五次模拟检测理综试题-高中化学
名校
解题方法
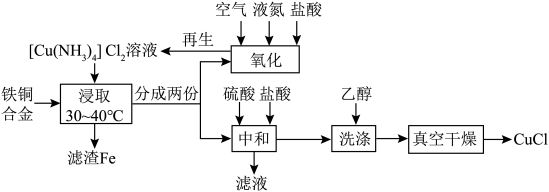
10 . CuCl为白色固体,难溶于水和乙醇,潮湿时易被氧化,常用作催化剂、杀菌剂、媒染剂、脱色剂。以废弃铁铜合金为原料制备CuCl的流程如图所示: ;②常温下,
;②常温下, 。
。
请回答下列问题:
(1)用再生液“浸取”铁铜合金不需要额外加热的原因可能为________ ;该阶段被氧化的铜元素与被还原的铜元素的质量之比为________ 。
(2)“氧化”阶段中最适宜的投料比为________ (填字母)。
a. b.
b. c.
c. d.
d.
(3)“中和”阶段的离子方程式为________ 。
(4)为了防止CuCl被氧化,上述流程中采取的两个措施是________ 。
(5)“中和”阶段会有部分铜元素被氧化。为了综合利用滤渣Fe和滤液,以提高CuCl的产率,试简述其方案:________ 。
(6)常温下, 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应的平衡常数为K,
,其反应的平衡常数为K, 的平衡常数为
的平衡常数为________ (用含K的代数式表示)。
 ;②常温下,
;②常温下, 。
。请回答下列问题:
(1)用再生液“浸取”铁铜合金不需要额外加热的原因可能为
(2)“氧化”阶段中最适宜的投料比为
a.
 b.
b. c.
c. d.
d.
(3)“中和”阶段的离子方程式为
(4)为了防止CuCl被氧化,上述流程中采取的两个措施是
(5)“中和”阶段会有部分铜元素被氧化。为了综合利用滤渣Fe和滤液,以提高CuCl的产率,试简述其方案:
(6)常温下,
 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应的平衡常数为K,
,其反应的平衡常数为K, 的平衡常数为
的平衡常数为
您最近一年使用:0次
2024-06-01更新
|
96次组卷
|
2卷引用:陕西省西安市第一中学2023-2024学年高三下学期4月二模考试化学试题





