名校
解题方法
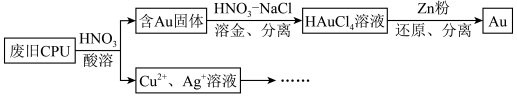
1 . 用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。
(1)酸溶后经______ 操作、将混合物分离。
(2)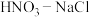 与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。
与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。
①Au溶于稀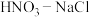 溶液会生成
溶液会生成 ,试写出此溶液中所发生的离子方程式:
,试写出此溶液中所发生的离子方程式:______ 。
②关于溶金的下列说法正确的是______ 。
a.用到了 的氧化性
的氧化性
b.王水中浓盐酸的主要作用是增强溶液的酸性
c.用浓盐酸与 也可使Au溶解
也可使Au溶解
(3)若用Zn粉将溶液中的1mol 完全还原,则参加反应的Zn的物质的量是
完全还原,则参加反应的Zn的物质的量是______ mol。
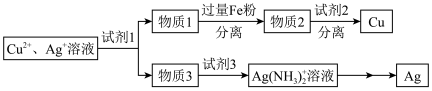
(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。______ ,物质2是______ 。

(1)酸溶后经
(2)
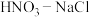 与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。
与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。①Au溶于稀
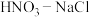 溶液会生成
溶液会生成 ,试写出此溶液中所发生的离子方程式:
,试写出此溶液中所发生的离子方程式:②关于溶金的下列说法正确的是
a.用到了
 的氧化性
的氧化性b.王水中浓盐酸的主要作用是增强溶液的酸性
c.用浓盐酸与
 也可使Au溶解
也可使Au溶解(3)若用Zn粉将溶液中的1mol
 完全还原,则参加反应的Zn的物质的量是
完全还原,则参加反应的Zn的物质的量是(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。
您最近一年使用:0次
名校
解题方法
2 . 下列实验装置使用正确的是
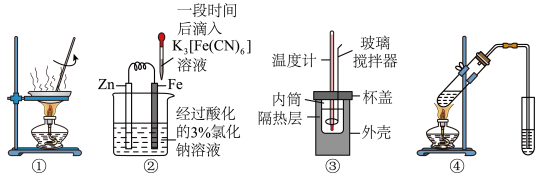
| A.图①装置用于苯甲酸溶液蒸发浓缩 | B.图②装置用于验证金属锌保护铁 |
| C.图③装置用于测定中和反应的反应热 | D.图④装置用于制备乙酸乙酯 |
您最近一年使用:0次
解题方法
3 . 镍主要用于合金及用作催化剂,也可用来制造货币等。以镍废渣(主要成分为 ,还含有
,还含有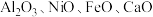 和
和 为原料制备纯镍的流程如图,回答下列问题:
为原料制备纯镍的流程如图,回答下列问题:_____________ (填化学式):常温下,“酸浸”中硫酸浓度与镍浸出率的关系如图所示,硫酸浓度大于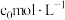 后,镍浸出率降低的可能原因是
后,镍浸出率降低的可能原因是_____________ 。_________________________________________________ (用离子方程式表示)。
(3)请设计实验确认“氧化”过程中的杂质离子已经被完全转化_____________________________________ 。
(4)“沉铝”时 的作用是
的作用是_________________ ,“操作 ”包括蒸发浓缩、
”包括蒸发浓缩、_____________ 、过滤、洗涤。
 ,还含有
,还含有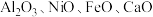 和
和 为原料制备纯镍的流程如图,回答下列问题:
为原料制备纯镍的流程如图,回答下列问题: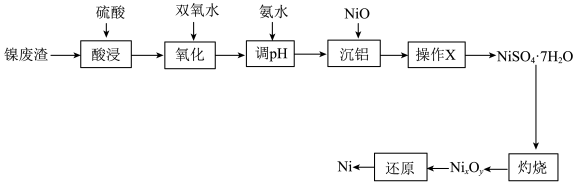
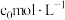 后,镍浸出率降低的可能原因是
后,镍浸出率降低的可能原因是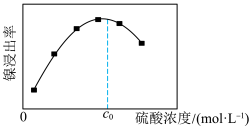
(3)请设计实验确认“氧化”过程中的杂质离子已经被完全转化
(4)“沉铝”时
 的作用是
的作用是 ”包括蒸发浓缩、
”包括蒸发浓缩、
您最近一年使用:0次
名校
解题方法
4 . 氧化钇( )广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、
)广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、 ,还含有一定量的
,还含有一定量的 、
、 、MgO)等)为原料生产
、MgO)等)为原料生产 的工艺流程如图所示:
的工艺流程如图所示: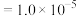 mol⋅L
mol⋅L 时,认为已沉淀完全。
时,认为已沉淀完全。
②常温下,相关金属离子开始沉淀和沉淀完全时的pH如图所示:
(1)“酸浸”时需适当提高浸取液的温度,其目的是_______ ;
采用离子浓度传感器测得相同时间内 的浸取率与浸取溶液温度的关系如图所示,
的浸取率与浸取溶液温度的关系如图所示, ℃后,
℃后, 的浸取率随温度升高而减小的原因是
的浸取率随温度升高而减小的原因是_______ 。_______ (填化学式)。
(3)“沉钇”后的滤液中浓度最大的金属离子是_______ (填离子符号);若常温下测得 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中 mol⋅L
mol⋅L ,则
,则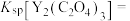
_______ mol⋅L (保留两位有效数字)。
(保留两位有效数字)。
(4)“沉钇”后所得晶体为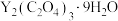 ,其中C元素的化合价为
,其中C元素的化合价为_______ 。
(5)“焙烧”时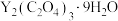 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
 )广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、
)广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、 ,还含有一定量的
,还含有一定量的 、
、 、MgO)等)为原料生产
、MgO)等)为原料生产 的工艺流程如图所示:
的工艺流程如图所示: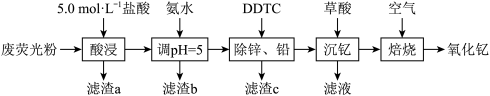
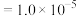 mol⋅L
mol⋅L 时,认为已沉淀完全。
时,认为已沉淀完全。②常温下,相关金属离子开始沉淀和沉淀完全时的pH如图所示:

(1)“酸浸”时需适当提高浸取液的温度,其目的是
采用离子浓度传感器测得相同时间内
 的浸取率与浸取溶液温度的关系如图所示,
的浸取率与浸取溶液温度的关系如图所示, ℃后,
℃后, 的浸取率随温度升高而减小的原因是
的浸取率随温度升高而减小的原因是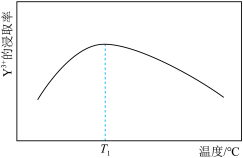
(3)“沉钇”后的滤液中浓度最大的金属离子是
 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中 mol⋅L
mol⋅L ,则
,则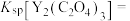
 (保留两位有效数字)。
(保留两位有效数字)。(4)“沉钇”后所得晶体为
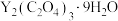 ,其中C元素的化合价为
,其中C元素的化合价为(5)“焙烧”时
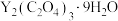 发生反应的化学方程式为
发生反应的化学方程式为
您最近一年使用:0次
2024-05-07更新
|
129次组卷
|
3卷引用:2024届海南省琼海市嘉积中学高三下学期模拟预测化学试题
解题方法
5 . 下列有关实验仪器与实验操作的叙述正确的是
| A.蒸馏完毕后,应先停止通冷凝水,再停止加热 |
| B.滴定接近终点时,滴定管尖嘴不能触碰锥形瓶内壁 |
| C.粗盐提纯过程中,需要用到的实验仪器有坩埚、漏斗、玻璃棒等 |
| D.用NaOH固体配制一定物质的量浓度溶液时,溶解后冷却至室温再转移到容量瓶中 |
您最近一年使用:0次
6 . 纳米级硒化锰(MnSe)是一种半导体材料,难溶于水。以锰渣(主要成分是 ,含少量
,含少量 、CuO)为原料制备硒化锰的流程如图所示:
、CuO)为原料制备硒化锰的流程如图所示:
(1)为了提高“酸溶”速率,宜采取的措施有___________ (填两条)。
(2)滤渣1的主要成分之一是单质,“还原”得到的滤液中溶质为 和
和 。写出“还原”反应的离子方程式:
。写出“还原”反应的离子方程式:___________ 。
(3)“氧化”中还原剂、氧化剂的物质的量之比为___________ 。
(4)滤渣2的主要成分是___________ (填化学式)。常温下,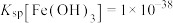 。离子浓度
。离子浓度 时认为该离子已沉淀完全。“除铁”调节pH的最小值为
时认为该离子已沉淀完全。“除铁”调节pH的最小值为___________ 。
(5)“合成”中分离MnSe的操作名称是___________ 。
 ,含少量
,含少量 、CuO)为原料制备硒化锰的流程如图所示:
、CuO)为原料制备硒化锰的流程如图所示: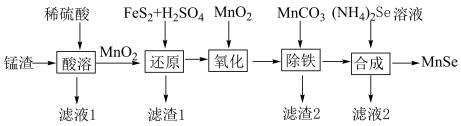
(1)为了提高“酸溶”速率,宜采取的措施有
(2)滤渣1的主要成分之一是单质,“还原”得到的滤液中溶质为
 和
和 。写出“还原”反应的离子方程式:
。写出“还原”反应的离子方程式:(3)“氧化”中还原剂、氧化剂的物质的量之比为
(4)滤渣2的主要成分是
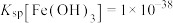 。离子浓度
。离子浓度 时认为该离子已沉淀完全。“除铁”调节pH的最小值为
时认为该离子已沉淀完全。“除铁”调节pH的最小值为(5)“合成”中分离MnSe的操作名称是
您最近一年使用:0次
解题方法
7 .  是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺流程如图所示。
水合物的工艺流程如图所示。
 是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺流程如图所示。
水合物的工艺流程如图所示。
| A.反应釜1需在隔绝空气条件下进行 |
| B.适当升温和搅拌,可提高反应釜中的反应速率 |
C.进入反应釜1和2的 的物质的量之比宜为2∶1 的物质的量之比宜为2∶1 |
D.实验室进行“滤液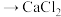 水合物”的操作为加热浓缩、冷却结晶、过滤等 水合物”的操作为加热浓缩、冷却结晶、过滤等 |
您最近一年使用:0次
8 . 下列有关化学实验安全以及基本操作的叙述正确的是
| A.皮肤溅上碱液,立即涂擦稀盐酸 |
| B.在烧杯中做钠与水反应的实验时,钠块要切成绿豆大小 |
| C.蒸馏近沸腾时,忘加沸石,应立即打开瓶盖追加 |
| D.常压蒸馏时,加入液体的体积不超过蒸馏烧瓶容积的三分之一 |
您最近一年使用:0次
9 . 氯化亚铜(CuCl)是一种易水解的白色固体。以低品位铜矿砂(主要成分CuS)为原料制备CuCl的工艺流程如图所示。
(1)“酸溶1”时,CuS作_______ (填“氧化剂”或“还原剂”)。
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为_______ 。将生成的MnCO3分离出来的实验操作为_______ 。
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有_______ (只答一种方法)。
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生_______ 气体。
(5)“洗涤”应先用稀盐酸洗涤,其目的是_______ 。

(1)“酸溶1”时,CuS作
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生
(5)“洗涤”应先用稀盐酸洗涤,其目的是
您最近一年使用:0次
名校
10 . 对废催化剂进行回收可有效利用金属资源。某废催化剂主要含 、
、 、
、 。一种回收利用废催化剂的工艺流程如下图。
。一种回收利用废催化剂的工艺流程如下图。
(1)“焙烧”时, 转化为
转化为 ,
, 中Mo的化合价为
中Mo的化合价为_______ ,出该步骤相应的化学方程式_______ 。
(2)溶浸后的溶液中,铝元素以 的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为
的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为_______ 。
(3)“沉钼”后,滤液X的溶质主要是_______ (写化学式)。
(4)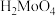 在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是
在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是_______ 。
(5)已知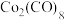 中
中 元素的化合价为0价。
元素的化合价为0价。
①在“反应”中的氧化剂和还原剂物质的量之比为_______ 。
② 是一种可以循环利用的物质,
是一种可以循环利用的物质, 是
是_______ (填化学式)。
 、
、 、
、 。一种回收利用废催化剂的工艺流程如下图。
。一种回收利用废催化剂的工艺流程如下图。 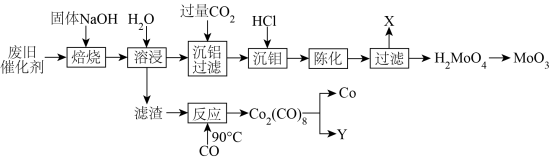
(1)“焙烧”时,
 转化为
转化为 ,
, 中Mo的化合价为
中Mo的化合价为(2)溶浸后的溶液中,铝元素以
 的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为
的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为(3)“沉钼”后,滤液X的溶质主要是
(4)
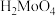 在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是
在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是(5)已知
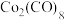 中
中 元素的化合价为0价。
元素的化合价为0价。①在“反应”中的氧化剂和还原剂物质的量之比为
②
 是一种可以循环利用的物质,
是一种可以循环利用的物质, 是
是
您最近一年使用:0次



