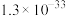1 . 为了除去某NaCl固体样品中含有的 、
、 和
和 杂质,某化学小组选用
杂质,某化学小组选用 溶液、稀盐酸、
溶液、稀盐酸、 溶液三种试剂设计了如下流程。
溶液三种试剂设计了如下流程。______ 、____ 、____ 。
(2)沉淀C的成分是____ 。
(3)写出加入碳酸钠溶液后发生反应的化学方程式________ 。(写出一个即可)
 、
、 和
和 杂质,某化学小组选用
杂质,某化学小组选用 溶液、稀盐酸、
溶液、稀盐酸、 溶液三种试剂设计了如下流程。
溶液三种试剂设计了如下流程。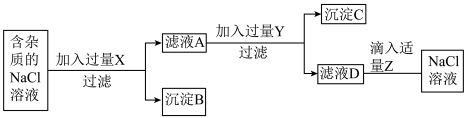
(2)沉淀C的成分是
(3)写出加入碳酸钠溶液后发生反应的化学方程式
您最近一年使用:0次
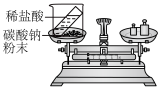
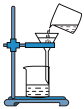
2 . 化学基本实验操作是学好化学的基本技能之一。下列选项中操作正确的是
| A | B | C | D |
|
|
|
|
| 稀释浓硫酸 | 验证质量守恒定律 | 闻药品气味 | 过滤液体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 以废旧镍氢电池的金属电极芯[主要成分为 和
和 ,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
②酸性条件下的氧化性: >
> 。
。
回答下列问题:
(1)“氧化”时 作
作_____ (填“氧化剂”或“还原剂”,下同),“浸出”时 作
作______ 。
(2)写出“沉钴1”中 转化为
转化为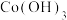 的离子方程式:
的离子方程式:_______ 。
(3)设计“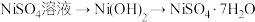 ”的目的是
”的目的是_______ 。
(4)“沉钴2”中发生反应的离子方程式为_______ ,_______ (填“能”或“不能”)用 替代
替代 ,理由是
,理由是_______ 。
(5)设计实验检验 是否洗净:
是否洗净:_______ 。
(6)水溶液中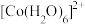 、
、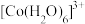 的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能:
的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能: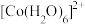
_______ (填“>”“<”或“=”)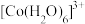 。
。
(7)镍单质晶胞有两种形式,如图所示。已知:图1晶胞棱长为acm,图2中晶胞底边长为bcm,高为ccm。图1、图2(正六棱柱)镍晶体密度之比为_______ 。
 和
和 ,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
| 离子 |  |  |  |  |  |  |
| 开始沉淀的pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.2 | |
| 完全沉淀的pH | 8.3 | 2.8 | 4.7 | 8.9 | 9.2 | 1.1 |
 >
> 。
。回答下列问题:
(1)“氧化”时
 作
作 作
作(2)写出“沉钴1”中
 转化为
转化为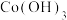 的离子方程式:
的离子方程式:(3)设计“
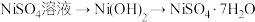 ”的目的是
”的目的是(4)“沉钴2”中发生反应的离子方程式为
 替代
替代 ,理由是
,理由是(5)设计实验检验
 是否洗净:
是否洗净:(6)水溶液中
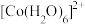 、
、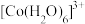 的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能:
的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能: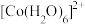
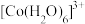 。
。(7)镍单质晶胞有两种形式,如图所示。已知:图1晶胞棱长为acm,图2中晶胞底边长为bcm,高为ccm。图1、图2(正六棱柱)镍晶体密度之比为

您最近一年使用:0次
7日内更新
|
40次组卷
|
3卷引用:2024届河南省百所名校仿真模拟大联考三模考试理综试题-高中化学
名校
解题方法
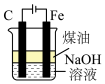
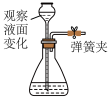
4 . 下列实验装置或操作能达到相应实验目的的是
| 实验装置或操作 |
|
|
| 实验目的 | A.测量氨水浓度 | B.制备Fe(OH)2 |
| 实验装置或操作 |
|
|
| 实验目的 | C.检查装置气密性 | D.测量CCl4沸点 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
50次组卷
|
2卷引用:2024届湘豫名校高三下学期考前保温卷理综试题-高中化学
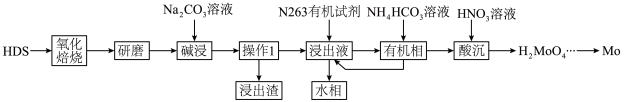
5 . HDS废催化剂是石油精炼加工产生的废弃物,但富含Mo、Ni等元素,是重要的二次资源。一种从HDS中回收Mo的工艺流程如图所示。 、
、 、
、 ;
;
②“浸出渣”的成分为 、
、 ;
;
③常温下, 易溶于水。
易溶于水。
(1)钼酸镍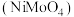 中
中 元素的化合价为
元素的化合价为_____ 价。
(2)“操作1”为_____ ,在化学实验室中“操作1”用到的玻璃仪器有烧杯、_____ 和_____ 。
(3)结合下图,碱浸时选择的 最佳添加量为
最佳添加量为_____ wt%,最佳浸出温度为_____ ℃。 在碱浸时有
在碱浸时有 和
和 生成,该反应化学方程式为
生成,该反应化学方程式为_____ 。
(5)采用碳酸根类型的N263萃取钼的反应为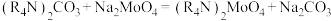 。已知一些离子被
。已知一些离子被 萃取的先后顺序为
萃取的先后顺序为 ,则加入
,则加入 反萃取发生反应的离子方程式为
反萃取发生反应的离子方程式为_____ 。萃取后有机相为 型,加入
型,加入 处理后可实现萃取剂再生。
处理后可实现萃取剂再生。
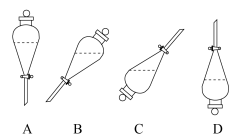
(6)在实验室进行萃取操作时,需要打开分液漏斗活塞放气,正确的放气图示为_____ (填标号)。_____ 和_____ 。
 、
、 、
、 ;
;②“浸出渣”的成分为
 、
、 ;
;③常温下,
 易溶于水。
易溶于水。(1)钼酸镍
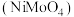 中
中 元素的化合价为
元素的化合价为(2)“操作1”为
(3)结合下图,碱浸时选择的
 最佳添加量为
最佳添加量为
 在碱浸时有
在碱浸时有 和
和 生成,该反应化学方程式为
生成,该反应化学方程式为(5)采用碳酸根类型的N263萃取钼的反应为
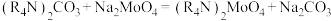 。已知一些离子被
。已知一些离子被 萃取的先后顺序为
萃取的先后顺序为 ,则加入
,则加入 反萃取发生反应的离子方程式为
反萃取发生反应的离子方程式为 型,加入
型,加入 处理后可实现萃取剂再生。
处理后可实现萃取剂再生。(6)在实验室进行萃取操作时,需要打开分液漏斗活塞放气,正确的放气图示为
您最近一年使用:0次
7日内更新
|
20次组卷
|
2卷引用:2024届河南省郑州市名校教研联盟高三下学期模拟预测理综试题-高中化学
6 . 物质的鉴别和除杂是化学学习的重要内容之一,则下列鉴别和除杂的方法错误的是
| A.用熟石灰鉴别尿素和氯化铵 | B.用水鉴别氢氧化钠和氯化钠 |
C.点燃的方法除去 中的CO 中的CO | D.用碳酸钠鉴别氯化钙溶液和稀盐酸 |
您最近一年使用:0次
名校
解题方法
7 . 中国文化博大精深,许多文献记载中蕴含丰富的化学知识,下列有关说法错误的是
| A.《茶疏》中对泡茶过程有如下记载:“治壶、投茶、出浴、淋壶、烫杯、酾茶、品茶……”,泡茶过程涉及的操作有溶解、过滤等。 |
| B.《天工开物》记载“人贱者短褐、梟裳,冬以御寒,夏以蔽体,其质造物之所具也。属草木者,为梟、麻、苘、葛……”文中的“臬、麻、苘、葛”属于纤维素。 |
| C.《千里江山图》中的颜料来自于矿物质,并经研磨、溶解、过滤这三道工序获得,这三道工序涉及的均是物理变化。 |
| D.《傅鹑觚集·太子少傅箴》中写道:“夫金木无常,方园应行,亦有隐括,习与性形。故近朱者赤,近墨者黑。”这里的“朱”指的是Fe2O3。 |
您最近一年使用:0次
7日内更新
|
267次组卷
|
3卷引用:2024届河南省信阳高级中学高三下学期考前最后一卷理科综合试题-高中化学
8 . 层状LiMnO2在电动车、空间技术等范畴具有十分广阔的应用前景。LiMnO2可由软锰矿(主要成分是MnO2,含少量Fe2O3、Al2O3、SiO2、MgO等)制备,其制备流程如图:
回答下列问题:
(1) LiMnO2中锰元素的化合价为______ ;“酸浸”后过滤,所得滤液中主要含有的金属阳离子有______ 。
(2)为了提高“酸浸”的浸取速率,可采取的措施有______ (写出两点)。
(3)“氧化”步骤需要加入过量MnO2,该步反应的离子方程式为______ 。
(4)常温下,“调pH”后溶液pH=5,则滤渣2的主要成分是______ 。
(5)滤渣3与浓H2SO4反应可以释放HF,同时得到的副产物是______ 。
(6)测定 LiMnO2样品中锰含量:取10g LiMnO2样品,粉碎后加入浓盐酸、30%H2O2溶液,充分反应,生成Mn(Ⅱ)。加入蒸馏水标定溶液体积为250mL,移取25mL后加入KB指示剂,用0.15mol/L的EDTA标准溶液滴定,平均消耗60mL标准溶液。样品中锰含量为______ %(已知:EDTA与Mn2+反应的化学计量数之比为1∶1)。
物质 |
|
|
|
|
|
|
|
|
|
|
|
(1) LiMnO2中锰元素的化合价为
(2)为了提高“酸浸”的浸取速率,可采取的措施有
(3)“氧化”步骤需要加入过量MnO2,该步反应的离子方程式为
(4)常温下,“调pH”后溶液pH=5,则滤渣2的主要成分是
(5)滤渣3与浓H2SO4反应可以释放HF,同时得到的副产物是
(6)测定 LiMnO2样品中锰含量:取10g LiMnO2样品,粉碎后加入浓盐酸、30%H2O2溶液,充分反应,生成Mn(Ⅱ)。加入蒸馏水标定溶液体积为250mL,移取25mL后加入KB指示剂,用0.15mol/L的EDTA标准溶液滴定,平均消耗60mL标准溶液。样品中锰含量为
您最近一年使用:0次
2024-06-04更新
|
273次组卷
|
5卷引用:2024届河南省周口市西华县第一高级中学高三下学期信息押题模拟训练理综卷(3)-高中化学
2024届河南省周口市西华县第一高级中学高三下学期信息押题模拟训练理综卷(3)-高中化学2024届河南省许昌部分高中高三下学期模拟考试(三)理科综合试题-高中化学2024届河北省部分高中高三下学期二模化学试题(已下线)T16-工业流程题(已下线)2024届四川省成都外国语学校高三下学期冲刺练习(五)理科综合试题-高中化学
名校
解题方法
9 . 钴广泛应用于机械制造、电子电器、航空航天、电池制造等行业,是国家重要的战略资源。用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题:
① 具有强氧化性。
具有强氧化性。
② ,
, 。
。
(1)为提高含钴废料的浸出效率,可采取的措施是___________ (任写一条)。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ ;浸出渣的主要成分为___________ (填化学式)。
(3)向“浸出液”中加入适量的 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)①“除钙镁”后,滤液中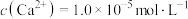 时,
时,
___________  。
。
②若“调pH”时溶液的pH偏低,将会导致 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
(5)将 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: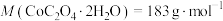 ,曲线中330℃及以上所得固体均为钴氧化物]
,曲线中330℃及以上所得固体均为钴氧化物] ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为___________ 。
 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题: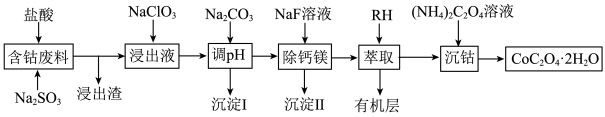
①
 具有强氧化性。
具有强氧化性。②
 ,
, 。
。(1)为提高含钴废料的浸出效率,可采取的措施是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)向“浸出液”中加入适量的
 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为(4)①“除钙镁”后,滤液中
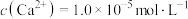 时,
时,
 。
。②若“调pH”时溶液的pH偏低,将会导致
 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是(5)将
 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: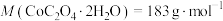 ,曲线中330℃及以上所得固体均为钴氧化物]
,曲线中330℃及以上所得固体均为钴氧化物]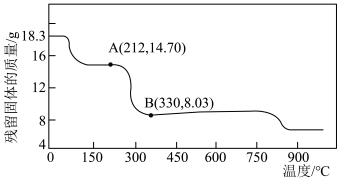
 ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为
您最近一年使用:0次
2024-06-02更新
|
175次组卷
|
5卷引用:河南省许昌高级中学2023-2024学年高三下学期5月月考化学试题
10 . 以金红石(主要成分为 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: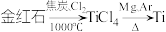 。下列叙述错误的是
。下列叙述错误的是
 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: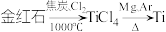 。下列叙述错误的是
。下列叙述错误的是A.利用碳氯化工艺制备 的化学方程式为 的化学方程式为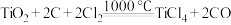 |
B.粗 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 |
C.制备Ti的主要过程中的 用 用 代替,会影响 代替,会影响 的产率和纯度 的产率和纯度 |
| D.将金红石和焦炭充分混合研磨后,再通入氯气可以提高反应速率 |
您最近一年使用:0次