1 . 一种工业上利用废旧三元锂离子电池正极材料(主要成分为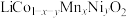 ,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示:
,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示: 的溶解度随温度升高而减小;
的溶解度随温度升高而减小;
②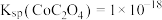 ,
,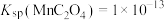 ,
,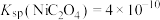 。
。
回答下列问题:
(1)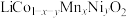 中
中 、
、 元素的化合价分别为+2价、+3价,若
元素的化合价分别为+2价、+3价,若 ,则
,则 元素的化合价为
元素的化合价为___________ 。锂离子电池中的电解质 与水相遇会生成
与水相遇会生成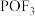 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“酸浸”时,下列试剂中最适宜替换 的是
的是___________ 。
a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓盐酸
溶液 d.浓盐酸
(3)若“酸浸”后溶液中 、
、 、
、 浓度均为
浓度均为 ,欲使
,欲使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而不沉淀
)而不沉淀 、
、 ,理论上需调节溶液
,理论上需调节溶液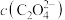 范围为
范围为___________ ;实际“沉钴”时,在加入 之后溶液中
之后溶液中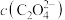 超出
超出 完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为
完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为___________ 。
(4)“沉锰”过程中加入 溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为
溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为___________ (用离子方程式表示)。
(5)“沉锂”操作中需将温度升高到 ,原因是:①加快反应速率;②
,原因是:①加快反应速率;②___________ 。
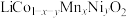 ,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示:
,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示: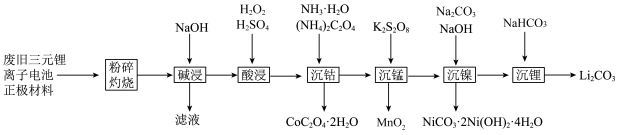
 的溶解度随温度升高而减小;
的溶解度随温度升高而减小;②
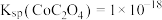 ,
,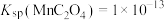 ,
,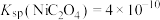 。
。回答下列问题:
(1)
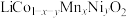 中
中 、
、 元素的化合价分别为+2价、+3价,若
元素的化合价分别为+2价、+3价,若 ,则
,则 元素的化合价为
元素的化合价为 与水相遇会生成
与水相遇会生成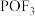 ,该反应的化学方程式为
,该反应的化学方程式为(2)“酸浸”时,下列试剂中最适宜替换
 的是
的是a.
 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓盐酸
溶液 d.浓盐酸(3)若“酸浸”后溶液中
 、
、 、
、 浓度均为
浓度均为 ,欲使
,欲使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而不沉淀
)而不沉淀 、
、 ,理论上需调节溶液
,理论上需调节溶液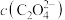 范围为
范围为 之后溶液中
之后溶液中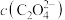 超出
超出 完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为
完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为(4)“沉锰”过程中加入
 溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为
溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为(5)“沉锂”操作中需将温度升高到
 ,原因是:①加快反应速率;②
,原因是:①加快反应速率;②
您最近一年使用:0次
解题方法
2 . 硫代硫酸钠具有较强的还原性和配位能力,可用于造纸业的脱氯剂、定量分析中的还原剂。硫代硫酸钠晶体 于
于 熔化,
熔化,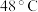 分解,易溶于水,难溶于乙醇,在酸性条件下极不稳定,易分解;该物质可由硫化钠、碳酸钠和二氧化硫制取,其制备过程如下:
分解,易溶于水,难溶于乙醇,在酸性条件下极不稳定,易分解;该物质可由硫化钠、碳酸钠和二氧化硫制取,其制备过程如下:
步骤一:将硫化钠粗品用重结晶法提纯
硫化钠粗品含有煤灰和重金属硫化物。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。取 粉碎的硫化钠粗品,加入一定体积的水(或工业酒精),在圆底烧瓶中于
粉碎的硫化钠粗品,加入一定体积的水(或工业酒精),在圆底烧瓶中于 下水浴回流
下水浴回流 ,装置如图1所示,通过改变工业酒精(或水)的用量,得出如下结果:
,装置如图1所示,通过改变工业酒精(或水)的用量,得出如下结果:
表1工业酒精的用量对提纯产品的影响(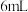 水)
水)
表2水的用量对提纯产品的影响( 工业酒精)
工业酒精)
实验室制备装置如图2所示。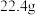 ,再称取
,再称取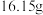 碳酸钠一起加入三颈烧瓶中,加水溶解,圆底烧瓶中产生的二氧化硫气体通入三颈烧瓶中,发生反应:①
碳酸钠一起加入三颈烧瓶中,加水溶解,圆底烧瓶中产生的二氧化硫气体通入三颈烧瓶中,发生反应:①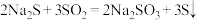 、②……、③
、②……、③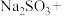
 ,有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行
,有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行 时溶液的
时溶液的 接近7,停止通入二氧化硫,过滤,将所得硫代硫酸钠溶液转移到蒸发皿中加热,浓缩到刚有晶体析出时停止加热,冷却析出晶体,抽滤得到
接近7,停止通入二氧化硫,过滤,将所得硫代硫酸钠溶液转移到蒸发皿中加热,浓缩到刚有晶体析出时停止加热,冷却析出晶体,抽滤得到 晶体。请回答下列问题:
晶体。请回答下列问题:
(1)图1中甲仪器的名称是______ ;重结晶法提纯硫化钠选用的试剂最好是______ (填字母)。
A.纯水 B.无水酒精
C.水与工业酒精体积比为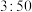 D.水与工业酒精体积比为
D.水与工业酒精体积比为
(2)实验过程中产生硫单质的离子方程式为______ 。
(3)实验过程中保证溶液的 接近7,控制通入
接近7,控制通入 的量很关键。开始有大量的浅黄色的硫析出,而后由黄变浅时严格控制通入
的量很关键。开始有大量的浅黄色的硫析出,而后由黄变浅时严格控制通入 的量,并且随时取样监测三颈烧瓶中溶液的
的量,并且随时取样监测三颈烧瓶中溶液的 。结合本实验装置,合理的取样操作是
。结合本实验装置,合理的取样操作是______ 。
(4)将硫代硫酸钠溶液转移到蒸发皿中加热浓缩,不能浓缩过度的理由是______ 。
(5)间接法测定产品的含量。
准确称量产品 溶于水,加入
溶于水,加入 甲醛(
甲醛( ),转移到
),转移到 容量瓶中,用水稀释到刻度,摇匀。准确称取
容量瓶中,用水稀释到刻度,摇匀。准确称取 于
于 碘量瓶中,加入
碘量瓶中,加入 蒸馏水溶解,再加入
蒸馏水溶解,再加入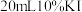 溶液(足量)和
溶液(足量)和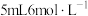 硫酸,盖上塞子置于阴暗处
硫酸,盖上塞子置于阴暗处 ,用
,用 水稀释,加入指示剂,用待测的
水稀释,加入指示剂,用待测的 溶液滴定到终点,消耗待测液
溶液滴定到终点,消耗待测液 。
。 的质量分数是
的质量分数是______ (用含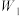 、
、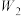 、
、 的式子表示,不用化简)。
的式子表示,不用化简)。
②若制取的产品中含有 ,实验中没有用甲醛掩蔽处理,测得样品的质量分数
,实验中没有用甲醛掩蔽处理,测得样品的质量分数______ (填“偏高”“偏低”或“无影响”)。
 于
于 熔化,
熔化,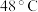 分解,易溶于水,难溶于乙醇,在酸性条件下极不稳定,易分解;该物质可由硫化钠、碳酸钠和二氧化硫制取,其制备过程如下:
分解,易溶于水,难溶于乙醇,在酸性条件下极不稳定,易分解;该物质可由硫化钠、碳酸钠和二氧化硫制取,其制备过程如下:步骤一:将硫化钠粗品用重结晶法提纯
硫化钠粗品含有煤灰和重金属硫化物。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。取
 粉碎的硫化钠粗品,加入一定体积的水(或工业酒精),在圆底烧瓶中于
粉碎的硫化钠粗品,加入一定体积的水(或工业酒精),在圆底烧瓶中于 下水浴回流
下水浴回流 ,装置如图1所示,通过改变工业酒精(或水)的用量,得出如下结果:
,装置如图1所示,通过改变工业酒精(或水)的用量,得出如下结果:表1工业酒精的用量对提纯产品的影响(
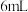 水)
水)工业酒精用量 | 60 | 80 | 100 | 120 | 140 |
粗产品量 | 6.6 | 9.6 | 13.4 | 12.3 | 11.0 |
结晶速度 | 慢 | 较慢 | 适中 | 较快 | 快 |
 工业酒精)
工业酒精)水的用量 | 2 | 4 | 6 | 8 | 10 |
粗产品量 | 10.0 | 11.4 | 13.4 | 9.6 | 6.2 |
结晶速度 | 快 | 较快 | 适中 | 较慢 | 慢 |

实验室制备装置如图2所示。

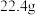 ,再称取
,再称取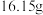 碳酸钠一起加入三颈烧瓶中,加水溶解,圆底烧瓶中产生的二氧化硫气体通入三颈烧瓶中,发生反应:①
碳酸钠一起加入三颈烧瓶中,加水溶解,圆底烧瓶中产生的二氧化硫气体通入三颈烧瓶中,发生反应:①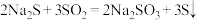 、②……、③
、②……、③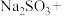
 ,有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行
,有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行 时溶液的
时溶液的 接近7,停止通入二氧化硫,过滤,将所得硫代硫酸钠溶液转移到蒸发皿中加热,浓缩到刚有晶体析出时停止加热,冷却析出晶体,抽滤得到
接近7,停止通入二氧化硫,过滤,将所得硫代硫酸钠溶液转移到蒸发皿中加热,浓缩到刚有晶体析出时停止加热,冷却析出晶体,抽滤得到 晶体。请回答下列问题:
晶体。请回答下列问题:(1)图1中甲仪器的名称是
A.纯水 B.无水酒精
C.水与工业酒精体积比为
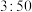 D.水与工业酒精体积比为
D.水与工业酒精体积比为
(2)实验过程中产生硫单质的离子方程式为
(3)实验过程中保证溶液的
 接近7,控制通入
接近7,控制通入 的量很关键。开始有大量的浅黄色的硫析出,而后由黄变浅时严格控制通入
的量很关键。开始有大量的浅黄色的硫析出,而后由黄变浅时严格控制通入 的量,并且随时取样监测三颈烧瓶中溶液的
的量,并且随时取样监测三颈烧瓶中溶液的 。结合本实验装置,合理的取样操作是
。结合本实验装置,合理的取样操作是(4)将硫代硫酸钠溶液转移到蒸发皿中加热浓缩,不能浓缩过度的理由是
(5)间接法测定产品的含量。
准确称量产品
 溶于水,加入
溶于水,加入 甲醛(
甲醛( ),转移到
),转移到 容量瓶中,用水稀释到刻度,摇匀。准确称取
容量瓶中,用水稀释到刻度,摇匀。准确称取 于
于 碘量瓶中,加入
碘量瓶中,加入 蒸馏水溶解,再加入
蒸馏水溶解,再加入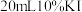 溶液(足量)和
溶液(足量)和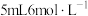 硫酸,盖上塞子置于阴暗处
硫酸,盖上塞子置于阴暗处 ,用
,用 水稀释,加入指示剂,用待测的
水稀释,加入指示剂,用待测的 溶液滴定到终点,消耗待测液
溶液滴定到终点,消耗待测液 。
。反应原理是 、
、 。用甲醛掩蔽
。用甲醛掩蔽 :
: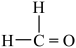
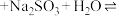

 。
。
 的质量分数是
的质量分数是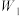 、
、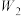 、
、 的式子表示,不用化简)。
的式子表示,不用化简)。②若制取的产品中含有
 ,实验中没有用甲醛掩蔽处理,测得样品的质量分数
,实验中没有用甲醛掩蔽处理,测得样品的质量分数
您最近一年使用:0次
3 . 环戊酮是合成新型降压药物的中间体,实验室制备环戊酮(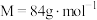 )的反应原理如下:
)的反应原理如下: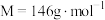 ,熔点为
,熔点为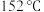 ,
, 左右升华;
左右升华;
b.环戊酮沸点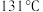 ,着火点
,着火点 。
。
步骤如下:
I.将 己二酸和适量
己二酸和适量 置于蒸馏烧瓶中,维持温度
置于蒸馏烧瓶中,维持温度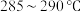 ,均匀加热20分钟;
,均匀加热20分钟;
Ⅱ.在馏出液中加入适量的 浓溶液,振荡锥形瓶、分液除去水层;向有机层中加入
浓溶液,振荡锥形瓶、分液除去水层;向有机层中加入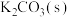 ,振荡分离出有机层;
,振荡分离出有机层;
Ⅲ.对Ⅱ所得有机层进行蒸馏,收集馏分,称量获得产品 ,计算产率。
,计算产率。
对于上述实验,下列说法正确的是
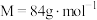 )的反应原理如下:
)的反应原理如下:
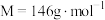 ,熔点为
,熔点为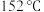 ,
, 左右升华;
左右升华;b.环戊酮沸点
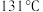 ,着火点
,着火点 。
。步骤如下:
I.将
 己二酸和适量
己二酸和适量 置于蒸馏烧瓶中,维持温度
置于蒸馏烧瓶中,维持温度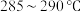 ,均匀加热20分钟;
,均匀加热20分钟;Ⅱ.在馏出液中加入适量的
 浓溶液,振荡锥形瓶、分液除去水层;向有机层中加入
浓溶液,振荡锥形瓶、分液除去水层;向有机层中加入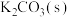 ,振荡分离出有机层;
,振荡分离出有机层;Ⅲ.对Ⅱ所得有机层进行蒸馏,收集馏分,称量获得产品
 ,计算产率。
,计算产率。对于上述实验,下列说法正确的是
| A.步骤I中,为增强冷凝效果应选用球形冷凝管 |
| B.步骤I中,为保证受热均匀应采取水浴加热的方式 |
| C.步骤Ⅱ中,分液操作需要的玻璃仪器有:分液漏斗、烧杯、玻璃棒 |
D.步骤Ⅲ中,应收集 范围内的馏分 范围内的馏分 |
您最近一年使用:0次
名校
解题方法
4 . 二氧化氯的制备及由二氧化氯制备一种重要的含氯消毒剂—亚氯酸钠(NaClO2)的工艺流程如图,下列说法正确的是

| A.“滤渣”的成分为MgCO3、CaCO3 | B.两处HCl的作用相同 |
| C.H2O2可以用KMnO4代替 | D.理论上,产生气体A、B的物质的量之比为1∶1 |
您最近一年使用:0次
昨日更新
|
164次组卷
|
2卷引用:2024届山东省日照市五莲县第一中学高三下学期模拟预测化学试题
5 . 实验室中初步分离环己醇、苯酚、苯甲酸混合液的流程如下。下列说法错误的是
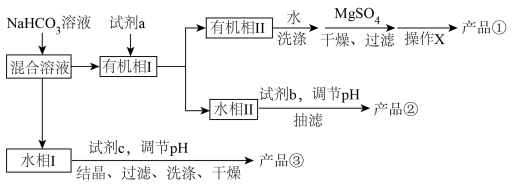
| A.环己醇、苯酚、苯甲酸粗产品依次由①、②、③获得 |
| B.若试剂a为碳酸钠,可以通过观察气泡现象控制试剂用量 |
C.“操作X”为蒸馏,“试剂b”可选用盐酸或 |
| D.试剂c可以选用盐酸或硫酸 |
您最近一年使用:0次
6 . 《天工开物》有如下叙述:“凡硝刮扫取时(墙中亦或进出),入缸内水浸一宿,秽杂之物浮于面上,掠取去时,然后入釜,注水煎炼,硝化水干,倾于器内,经过一宿,即结成硝……欲去杂还纯,再入水煎炼”。文中不涉及的操作方法是
| A.分液 | B.溶解 | C.蒸发结晶 | D.重结晶 |
您最近一年使用:0次
7 . 实验室中常使用Na、NaOH和Na2CO3,下列有关试剂的使用错误的是
| A.氢氧化钠:除去乙酸乙酯中的乙酸 |
| B.钠:比较乙醇、水、乙酸分子中羟基的活泼性 |
| C.碳酸钠:清洗附有油脂的试管 |
| D.氢氧化钠和碳酸钠:区分乙酸、乙醇、乙酸乙酯和环己烷 |
您最近一年使用:0次
8 . 化学与传统文化密不可分。下列说法错误的是
| A.药酒的制作利用了萃取原理 |
| B.青釉陶罐的主要成分是二氧化硅 |
| C.丝绸因富含氨基而具有良好的吸湿性 |
D.青铜器上的铜锈[ ]可用明矾水去除 ]可用明矾水去除 |
您最近一年使用:0次
7日内更新
|
58次组卷
|
2卷引用:2024届山东省烟台市招远市高三下学期三模化学试题
名校
解题方法
9 . 从硝酸铜和硝酸银的混合溶液中回收铜和银的流程如图所示。

| A.试剂Ⅰ可以是稀盐酸或稀硫酸 |
| B.流程中涉及的反应均是氧化还原反应 |
C.生成银氨溶液的离子方程式为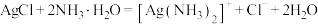 |
D.若试剂Ⅱ是甲醛, 甲醛参加反应最多生成 甲醛参加反应最多生成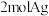 |
您最近一年使用:0次
7日内更新
|
68次组卷
|
3卷引用:山东省日照市五莲天立学校2024届高三(高复)下学期二模前模拟考试化学试题
10 . 下列有关实验及试剂的使用正确的是
A.用酸性 溶液鉴别苯和环己烷 溶液鉴别苯和环己烷 | B.加入 溶液,分液分离苯和溴苯 溶液,分液分离苯和溴苯 |
| C.加入生石灰,蒸馏除去乙醇中的水 | D.用 溶液除去 溶液除去 中的 中的 |
您最近一年使用:0次





